合并肝硬化的糖尿病性肌坏死:病例报告及文献综述
2011-06-09 MedSci原创 MedSci原创
Angervall和Stener于1965年首次报道了糖尿病性肌肉坏死[1]。其发病常见于1型糖尿病伴有长期代谢紊乱与晚期慢性微血管并发症的患者。典型的临床表现为受累部位肌肉部位(通常是股四头肌)突剧烈疼痛。磁共振成像(MRI)可确诊。在不能确诊的情况下,可能需要进行肌肉活组织检查。糖尿病性肌肉坏死的治疗包括卧床休息、止痛和改善糖尿病代谢。本病预后差,且预示着
Angervall和Stener于1965年首次报道了糖尿病性肌肉坏死[1]。其发病常见于1型糖尿病伴有长期代谢紊乱与晚期慢性微血管并发症的患者。典型的临床表现为受累部位肌肉部位(通常是股四头肌)突剧烈疼痛。磁共振成像(MRI)可确诊。在不能确诊的情况下,可能需要进行肌肉活组织检查。糖尿病性肌肉坏死的治疗包括卧床休息、止痛和改善糖尿病代谢。本病预后差,且预示着出现了严重的和全身性血管病变,可能在短期出现危急和致命性并发症 [2]。
病情介绍
一位来自墨西哥的患有酒精性肝硬化(Child-Pugh C/MELD 45)和2型糖尿病的38岁西班牙裔男性因不断恶化的脑病被送进急诊室。患者于10年前被确诊患有糖尿病。这期间由于长期饮酒,代谢控制非常差。被送进急诊室前一个月,该患者在静息时左大腿突发局部疼痛而且越来越严重。期间患者无发热或寒战。据亲属描述,患者未出现创伤、皮肤病损和蚊虫叮咬。口服常规镇痛药只能轻微缓解疼痛。在随后的几周,患者无法行走。口服常用镇痛药不再能缓解疼痛,且疼痛越来越严重。直到入院前3天患者的脑病恶化时患者一直在休息。体格检查期间,患者无发热,血压为110/70 mmHg,脉率为112,呼吸速率为每分钟24次。患者意识清醒且定为II级脑病。检查左大腿时发现在大腿中部前外侧可见一10×
血液检测(见表1)表明为大红细胞、正色素性贫血、嗜中性白细胞增多、血小板减少和凝血时间延长。患者非空腹血糖值升高。血培养及抗磷脂抗体呈阴性。X射线成像仅显示为左大腿软组织水肿;多普勒超声排除了深静脉血栓形成,核磁共振检查在T2加权信号图像上显示为股四头肌水肿和炎性改变。患者为亚急性血肿(图1)。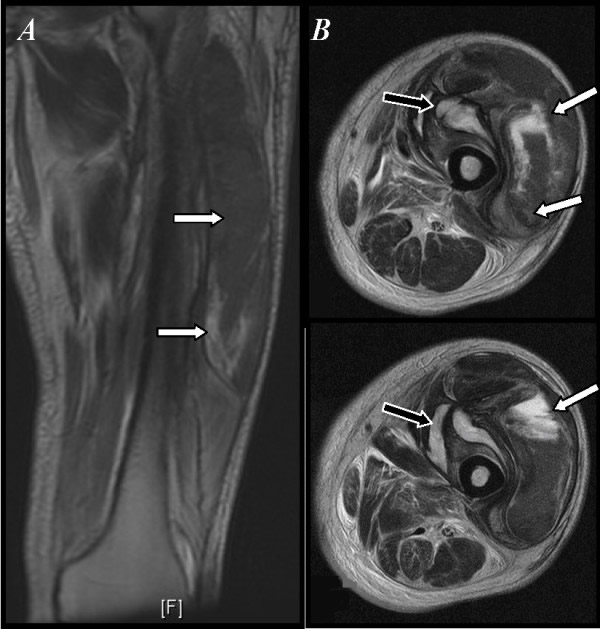
图1. 左大腿的磁共振图像。
A) T-2序列的冠状层面:与炎症变化和坏死相关的四头肌的高强度成像(箭头)。B)T-2
序列的纵向层面:四头肌的高强度成像(白箭头),脉管束的侧面出现流动性集积(黑箭头)。
一旦确诊为糖尿病性肌坏死和亚急性血肿,那么应开始进行保守治疗。治疗应包括绝对卧床休息、服用安泰乐镇痛药并应用抗生素预防特发性细菌性腹膜炎。也应进行肝性脑病、失代偿性肝硬化和糖尿病治疗。患者疼痛得到迅速控制、水肿消退和蜂窝组织炎得到改善。然而,5天后,大腿红斑部位疼痛加剧。并伴有低热。超声引导下肌肉活组织检查表明为坏死。革兰氏染色和培养结果表明厌氧和需氧菌以及真菌均为阴性。在此过程中,进行亚急性血肿病灶的局部清理。肿块和水肿得到了缓慢而渐进性改善后,患者出院。3周后,患者因出现IV级脑病而再次被送进急诊室。四肢检查未见任何异常情况。肝功能进行性恶化导致患者严重的肝功能不全并于入院后4天死亡。
讨论
糖尿病相关的肌肉坏死是一种罕见疾病。到目前为止,仅报告了约100例相关病例。严重的糖尿病性微血管病变被认为是自发性、非坏疽性和局部肌肉梗死的根本机制。也有证据表明纤维蛋白溶解和凝固异常、栓塞现象以及血管炎是少数病例发病的原因。此例伴有肝硬化的糖尿病性肌坏死病例值得关注。这是首次关于两种病变相关的病例报告。继发于严重肝功能损伤的凝血时间延长几乎肯定是形成血肿的原因,血肿是糖尿病性肌肉坏死患者先前未发现的一个并发症。这种并发症导致了感染风险的存在。住院期间在患者已出现低热的情况下清理血肿病灶以防止出现感染。尽管该病变和脑病都得到了改善,但是某些隐性或无症状感染可能导致肝功能迅速恶化,从而导致不可逆转的且致命性肝功能不全。糖尿病性肌坏死是一种鲜为人知的糖尿病并发症,预后差,且需要有高度警惕性。
糖尿病性肌坏死是一种偶发性微血管并发症,易于发生于代谢控制不佳的患者,并且与肾病(71%)、视网膜病变(56%)和神经病变(54%)等其它糖尿病并发症相关[1-3]。长期糖尿病性血管病变是糖尿病性肌坏死发生的必要条件[4]。一般认为,在长期患有糖尿病的女性患者中已有报道(确诊为糖尿病后15年);大多数病例见于1型糖尿病患者(71%)[1,2,5]。在2型糖尿病患者中多见于老年患者。
虽然没有明确界定,但是小血管的动脉粥样硬化栓塞也被认为是该病的发病机制。由于存在多条并行血管,因此该病易发于大腿肌肉。另一种机制被认为是与凝血纤溶系统相关的凝血级联系统[2,6]。
患者受累肌肉突发剧烈疼痛通常是该病的首发症状。最易受累部位为大腿肌肉;通常为单侧肌肉受累。在大多数情况下,弥漫性、迅速进展的疼痛向腰背部、膝和脚放射,因此不能进行日常活动。仅有3%的患者出现发热[1-7]。首见临床体征为大腿体积的增加。开始时改变不明显,但此后病变集中于受累肌肉。可能会伴有关节积液。目前40%的患者会出现明显肿块。罕见神经压迫,剧烈疼痛会导致肢体活动受限[5,7]。股四头肌是最常受累肌肉(87%),股外侧肌和股内侧肌受累率分别24%和22%。外展肌、髋屈肌和上肢肌肉很少受累。在约10%的病例中报告出现了双侧受累病变[6]。
实验室检验对于确诊没有帮助。在52%的病例出现肌酸磷酸激酶水平正常或略有升高;14%的病例出现白细胞增多。大多数情况下,AST、ALT、LDH水平和红细胞沉降率是正常的[8,5]。深静脉血栓形成是主要的鉴别诊断。其次需要排除的是实体性病变,如血肿、假血栓性静脉炎、急性动脉闭塞、脓肿、蜂窝组织炎、筋膜炎、滑囊炎和糖尿病脓性肌炎。有时很难区分糖尿病性肌坏死和腰骶神经根病变、糖尿病骨髓炎、肌肉撕裂、肿瘤、多发性肌炎或增生性肌炎。
需要有高度警惕性。此疾病很难通过进行体格检查确诊。检查(如X-射线成像、多普勒超声、对比的CT扫描、血管造影和MRI)通常能排除其他病因。MRI通常能确定糖尿病性肌肉坏死诊断。磁共振成像表明所受累肌肉的T2序列为高强度信号。常见肌肉周围或皮下组织水肿。可能是由于出血继发坏死,有时发现T1序列高强度信号[9,10]。在极少数情况下,主要是由于对标准疗法缺乏应答,故需要进行活组织检来确诊[8,6,10]。
活组织检查是诊断本病的金标准。由于考虑到出现并发症的风险,在进行活检之前必须确定有明确的适应症。基于感染或形成血肿的风险,细针穿刺活组织检查优于切开活组织检查[10,3]。通过对活检结果的审查表明在变性-再生的不同阶段会出现出血性坏死和肌纤维性肌炎。小血管壁为透明状且部分或全部血管腔闭塞。在中等大小的血管中,可观察到动脉粥样硬化病灶[4,2,6,3] 。应进行细菌、真菌和抗酸杆菌的培养,但是除非出现了肌肉坏死,否则培养结果应为阴性。
疼痛和炎症的控制是主要治疗措施。绝对卧床休息、非甾体抗炎药物或麻醉药的使用具有缓慢而逐步的改善症状。联合应用抗血小板和抗发炎药物可减少整体康复时间(从8周缩短为5周)[4,3]。虽然没有任何证据表明此方法将预防发病率或死亡率,但williamhill asia 仍推荐糖尿病患者进行更好的代谢控制。应考虑高凝状态,如果确诊,那么应开始抗凝[6,3]。建议采用手术疗法治疗动脉妥协情况下的减压[8]。
在大多数情况下,短期预后良好。疼痛和炎症至少需要8周才能消失。主要的潜在问题是导致短期内出现危及生命并发生的晚期全身性微血管病变[2,11]。高达50%的病例可能出现复发,其中大部分发生在先前受累的肌肉部位[2,6]。几乎一半的复发事件在2个月内出现[12]。
结论
这是伴有晚期肝硬化的糖尿病性肌坏死的首例文献报道。
参考文献
[1] Angervall L, Stener B: Tumoriform focal muscle degeneration in two diabetic patients.Diabetologia 1965 , 1:39-42.
[2] Wintz RL, Pimstone KR, Nelson SD: Detection of diabetic myonecrosis: complication is often-missed sign of underlying disease. Postgrad Med 2006 , 119(3):66-9.
[3] Scully RE, Mark EJ, McNeely WF, Ebeling SH, Phillips LD: Case 29-1997. Case records of the Massachusetts General Hospital.N Engl J Med 1997 , 337:839-45.
[4] Woolley SL, Smith DRK: Acute compartment syndrome secondary to diabetic muscle infarction: case report and literature review. European Journal of Emergency Medicine 2006 , 13:113-16.
[5] Rajiv R, Davidson MB: Diabetic muscle infarction: a rare complication of diabetes mellitus.The Endocrinologist 2004 , 14:167-70.
[6] Trujillo-Santos AJ: Diabetic muscle infarction: an underdiagnosed complication of long-standing diabetes.
Diabetes Care 2003 , 26:211-15.
[7] Umpierrez GE, Stiles RG, Kleinbart J, Krendel DA, Watts NB: Diabetic muscle infarction. Am J Med 1996 , 101:245-50.
[8] Kapur S, McKendry RJ: Treatment and outcomes of diabetic muscle infarction. J Clin Rheumatol 2005 , 11:8-12.
[9] Jacobs-Kosmin D, DeHoratius RJ: Musculoskeletal manifestations of endocrine disorders.Curr Opin Rheumatol 2005 , 17:64-9.
[10] Jelinek JS, Murphey MD, Aboulafia AJ, Dussault RG, Kaplan PA, Snearly WN: Muscle infarction in patients with diabetes mellitus: MR imaging findings. Radiology 1999 , 211:241-47.
[11] Bunch TJ, Birskovich LM, Eiken PW: Diabetic myonecrosis in a previously healthy woman and review of a 25-year Mayo Clinic experience. Endocr Pract 2002 , 8:343-6.
[12] Hachwi RN, Whitaker CH, Felice KJ: Multiple recurrences of diabetic muscle infarction.
J Clin Neuromusc Dis 2003, 5:96-102.
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言








#文献综述#
76
#坏死#
56
#病例报告#
111