首都医科大学柳柯/清华大学尹斓ACS Nano: 中耳递送载药水凝胶
2024-02-15 BioMed科技 BioMed科技 发表于陕西省
这种定制的中耳给药系统在治疗NIHL和耳蜗突触病变方面具有实现理想临床结果的巨大潜力。
噪声诱导的听力损失(NIHL)通常伴随着耳蜗突触病变,这种病变有可能被逆转以恢复听力。然而,以前使用几乎无创的中耳给药方法来实现感音神经性耳聋的完全恢复几乎没有成功案例。在这里,首都医科大学北京友谊医院柳柯、清华大学尹斓证明了使用脑源性神经营养因子(BDNF)-聚(DL-乳酸酸-羟基乙酸)共聚物(PLGA)负载的水凝胶中耳给药系统在逆转突触病变和恢复NIHL小鼠模型听力功能方面的有效性。通过单次噪声暴露(NE,115分贝,4小时)建立的小鼠模型,其听力阈值平均提高了20分贝,耳蜗毛细胞完好无损,但主要由于耳蜗丝带突触的损失导致听力受损。开发了一种BDNF-PLGA负载的热敏水凝胶,通过单次可控注射进入噪声暴露小鼠的鼓室,使其在中耳存在两周。这种干预在点击、4、8、16和32千赫兹的频率下完全恢复了NIHL。此外,耳蜗丝带突触显示出显著的恢复,而其他耳蜗成分(毛细胞和听觉神经)保持不变。此外,NE处理小鼠的耳蜗在暴露于BDNF后显示出肌球蛋白受体激酶B(TRKB)信号的激活。这些发现展示了一种可控且微创的治疗方法,利用BDNF-PLGA负载的水凝胶通过特定修复耳蜗突触病变来恢复NIHL。这种定制的中耳给药系统在治疗NIHL和耳蜗突触病变方面具有实现理想临床结果的巨大潜力。该研究题为“Complete Restoration of Hearing Loss and Cochlear Synaptopathy via Minimally Invasive, Single-Dose, and Controllable Middle Ear Delivery of Brain-Derived Neurotrophic Factor–Poly(dl-lactic acid-co-glycolic acid)-Loaded Hydrogel”发表在《ACS Nano》

图1展示了一种针对噪声诱导性听力损失(NIHL)和耳蜗突触病变的治疗策略,该策略涉及将含有脑源性神经营养因子(BDNF)和聚(DL-乳酸酸-co-羟基乙酸)共聚物(PLGA)的水凝胶通过温度敏感型水凝胶的形式注射到中耳。在室温下,这种水凝胶以液态形式注入,到达小鼠体内后,由于体温的作用,它转变为半固态,从而在中耳内保持较长时间。治疗后,这种水凝胶首先通过降低小鼠体温(低于30.5°C)转变为液态,最终通过咽鼓管完全排出体外。这一过程不仅实现了NIHL的完全恢复,而且在不损害中耳或鼓膜的情况下,显著恢复了耳蜗丝带突触,而其他耳蜗结构如毛细胞和听觉神经保持不变。这些发现表明,通过这种温度敏感型水凝胶的中耳给药,可以有效地修复耳蜗突触病变,为治疗NIHL提供了一种理想且实际的治疗方案。
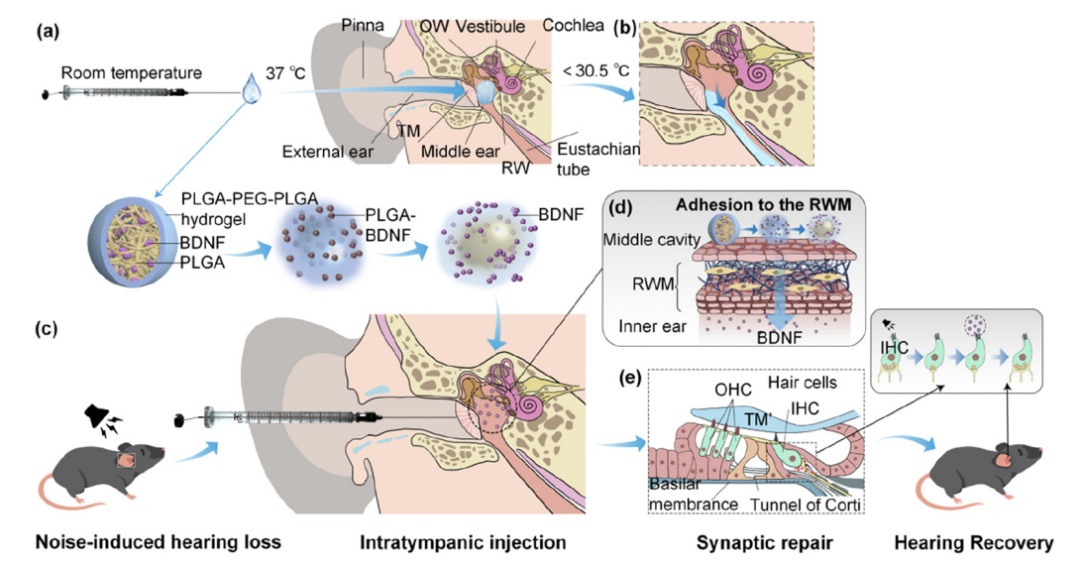
图1.温度敏感型水凝胶负载BDNF-PLGA治疗NIHL和耳蜗突触病变的示意图
【热可逆性水凝胶负载BDNF-PLGA用于治疗NIHL和耳蜗突触病变】
研究者们通过合成PLGA-PEG-PLGA三嵌段共聚物,并研究了其在热转换过程中的相变特性,揭示了水凝胶在室温下呈现液态,便于中耳注射,而在体温下转变为凝胶态,实现在内耳的持续释放。通过动态粘弹性分析,研究者们确定了水凝胶在37°C时的凝胶化时间和粘度变化,证实了其在体内快速凝胶化的特性。这些发现为开发一种能够在中耳内实现长期药物释放的热敏性水凝胶提供了科学依据,这对于治疗NIHL和耳蜗突触病变具有重要意义。
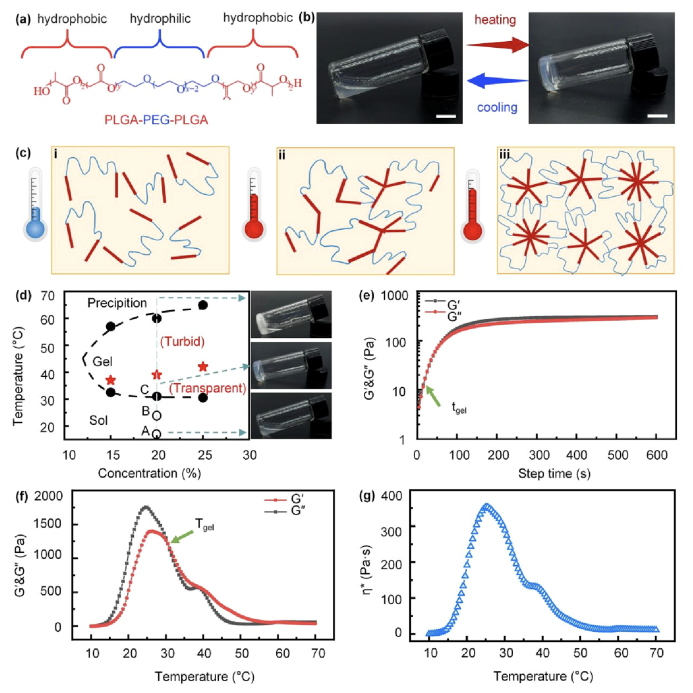
图2.热可逆性水凝胶负载BDNF-PLGA用于治疗NIHL和耳蜗突触病变
【PLGA-PEG-PLGA水凝胶作为药物递送系统的缓释性能】
图3展示了PLGA-PEG-PLGA水凝胶作为药物递送系统的持续释放性能。透射电子显微镜(TEM)图像显示了BDNF-PLGA微球具有良好的球形形态和光滑表面。在37°C的PBS中,PLGA-PEG-PLGA负载的BDNF-PLGA微球在两周内完全降解。通过使用牛血清白蛋白(BSA)作为BDNF的替代品,研究者们评估了药物的累积释放情况,并使用Micro BCA方法生成了标准曲线。结果表明,该药物递送系统展现出稳定、高效、高负载量和长期释放的特性。这些发现强调了PLGA-PEG-PLGA水凝胶在实现稳定和高效持续药物释放方面的潜力,为治疗NIHL提供了一种有前景的药物递送策略。
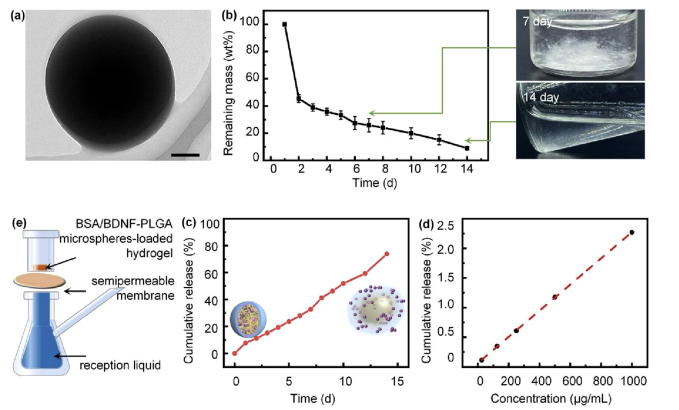
图3.PLGA-PEG-PLGA水凝胶作为药物递送系统的缓慢释放性能
【中耳注射BDNF-PLGA负载水凝胶完全恢复噪声诱导性听力损失】
图4展示了通过中耳注射温度敏感型水凝胶负载的BDNF-PLGA对噪声诱导性耳聋(NIHL)小鼠模型的治疗效果。研究中,小鼠在噪声暴露后,通过中耳注射这种水凝胶,观察到在注射后的第2天、第7天和第14天,小鼠的听觉脑干反应(ABR)阈值在点击声、4 kHz、8 kHz、16 kHz和32 kHz频率下显著降低,特别是在第14天时,与对照组相比,ABR阈值的恢复几乎完全,表明了治疗的有效性。此外,ABR波I的振幅和潜伏期也得到了显著改善,这表明耳蜗丝带突触的功能得到了恢复。这些结果证实了BDNF-PLGA负载的水凝胶通过中耳给药能够有效地治疗NIHL,并且这种治疗方法具有潜在的临床应用价值。
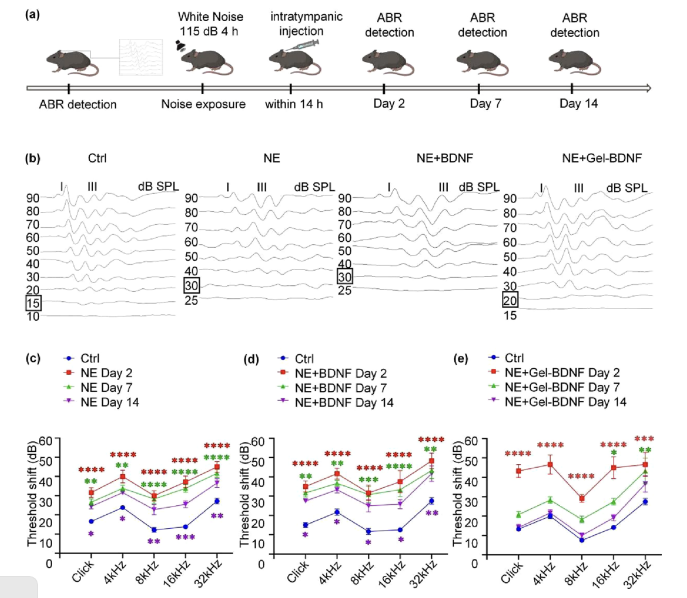
图4. 中耳注射BDNF-PLGA负载水凝胶完全恢复噪声诱导性听力损失(NIHL)
图5展示了在噪声诱导性耳聋(NIHL)小鼠模型中,通过中耳注射温度敏感型水凝胶负载的BDNF-PLGA对听觉脑干反应(ABR)波I的振幅和潜伏期的影响。研究结果显示,在注射后的第14天,与对照组相比,接受BDNF-PLGA水凝胶治疗的小鼠组(NE + Gel-BDNF组)在所有测试频率下的ABR波I振幅显著增加,潜伏期显著缩短,这表明治疗有效地改善了耳蜗丝带突触的功能,促进了听觉功能的恢复。这些发现强调了BDNF-PLGA水凝胶在修复噪声引起的耳蜗突触病变和恢复听力方面的有效性,为治疗NIHL提供了一种有前景的微创治疗方法。
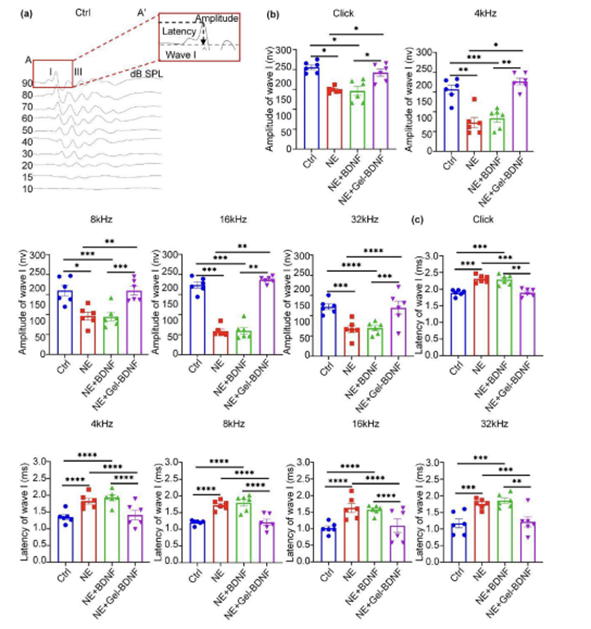
图5.中耳注射负载BDNF-PLGA水凝胶恢复噪声诱导性耳聋小鼠的ABR波I振幅和潜伏期
【中耳注射BDNF-PLGA负载水凝胶显著修复噪声诱导的耳蜗突触病变】
图6展示了在噪声诱导性耳聋(NIHL)小鼠模型中,通过中耳注射温度敏感型水凝胶负载的BDNF-PLGA对耳蜗丝带突触的修复效果。研究通过定量分析发现,在噪声暴露后第14天,与对照组相比,接受BDNF-PLGA水凝胶治疗的小鼠组(NE + Gel-BDNF组)在耳蜗的顶端、中部和基部回旋处的丝带突触数量显著增加,且突触的大小也得到了恢复。这些结果表明,BDNF-PLGA水凝胶的持续释放能够有效地促进耳蜗丝带突触的再生,从而实现对噪声诱导的耳蜗突触病变的完全修复。
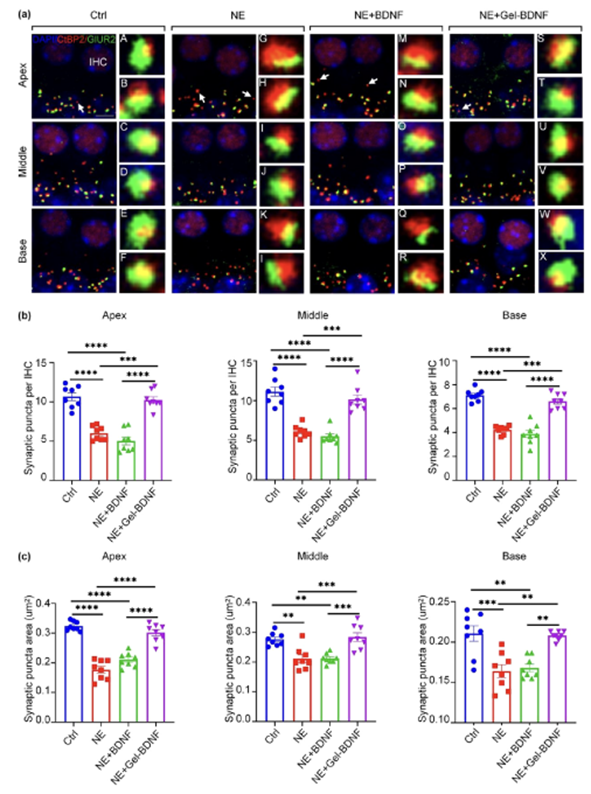
图6.中耳注射BDNF-PLGA负载水凝胶显著修复噪声诱导的耳蜗突触病变
【通过BDNF-PLGA负载水凝胶的递送激活TRKB信号通路】
图7展示了BDNF-PLGA负载的水凝胶通过中耳给药系统在内耳的递送效率,以及对TRKB信号通路激活的影响。研究通过Western blot分析证实,在接受BDNF-PLGA水凝胶治疗的小鼠耳蜗组织中,TRKB的表达显著增加,这表明水凝胶有效地将BDNF递送到内耳,并激活了下游的TRKB信号通路。此外,通过使用绿色荧光标记的C6染料,研究者们可视化了水凝胶在内耳的渗透情况,发现水凝胶在内耳中的分布与直接通过半圆管给药的C6染料相似,显示出良好的渗透性。这些结果证实了BDNF-PLGA水凝胶在中耳给药后能够实现高剂量的BDNF释放,激活TRKB信号通路,从而促进耳蜗突触的修复,为治疗噪声诱导性耳聋提供了一种有效的治疗策略。
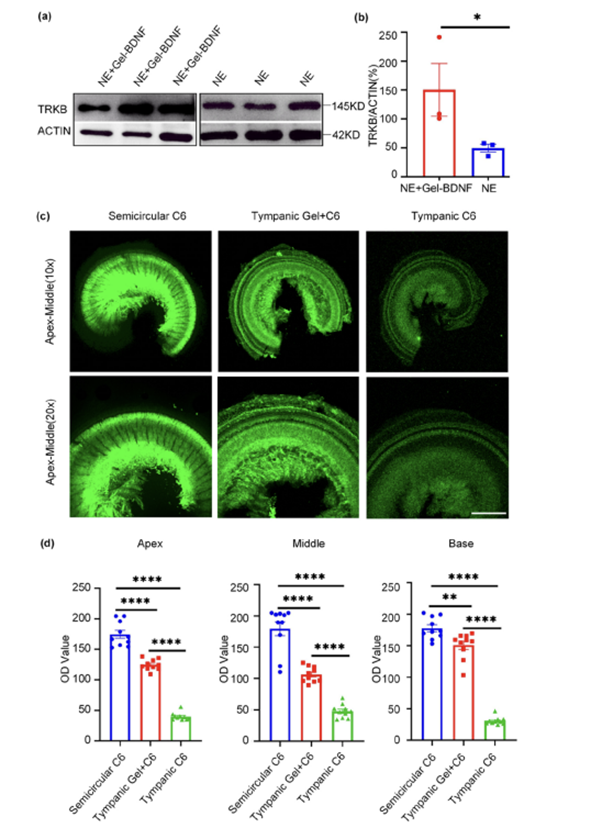
图7. 通过BDNF-PLGA负载水凝胶的递送激活TRKB信号通路
【温度敏感型水凝胶负载的BDNF-PLGA通过咽鼓管的完全排泄】
图8展示了温度敏感型水凝胶负载的BDNF-PLGA在中耳的排泄过程。研究通过在水凝胶中加入SUGARMAN食品色素(果绿色),并在中耳注射后观察其在不同温度和时间点下的排泄情况。结果显示,在30.5°C至37°C的温度范围内,水凝胶由于其凝胶状态无法通过咽鼓管排出。然而,通过间歇性冰敷(低于30.5°C)处理,水凝胶在8至12小时内被完全代谢并通过咽鼓管排出。这一过程的动态图像捕捉和剩余质量百分比的量化分析表明,通过温度控制,可以有效地促进水凝胶的排泄,从而确保治疗后中耳的清洁,避免长期残留。这些发现支持了这种中耳给药系统在治疗噪声诱导性耳聋时的安全性,因为它能够在不损害中耳结构的情况下,实现药物的有效递送和随后的完全排泄。
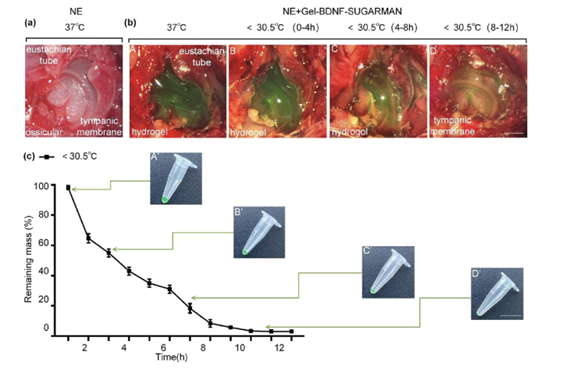
图8. 温度敏感型水凝胶负载的BDNF-PLGA通过咽鼓管的完全排泄
【小结】
该研究展示了一种微创、单剂量、可控的中耳给药系统,该系统使用脑源性神经营养因子(BDNF)-聚(DL-乳酸酸-羟基乙酸)共聚物(PLGA)负载的水凝胶,能够有效逆转耳蜗突触病变并恢复因噪声暴露引起的听力损失(NIHL)小鼠模型的听力功能。这种治疗方法通过在中耳注射BDNF-PLGA负载的水凝胶,实现了在特定频率下的听力完全恢复,并且耳蜗丝带突触得到了显著恢复,而其他耳蜗结构(如毛细胞和听觉神经)保持不变。此外,研究还发现BDNF能够激活耳蜗中的肌球蛋白受体激酶B(TRKB)信号通路。这些发现表明,这种定制的中耳给药系统在治疗NIHL和耳蜗突触病变方面具有巨大的临床应用潜力。
原文链接:
https://doi.org/10.1021/acsnano.3c11049
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言
















#水凝胶# #NIHL# #耳蜗突触病变#
50