Alzheimer's & Dementia:早发性与晚发性阿尔茨海默病患者的神经精神症状负担
2024-07-05 xiongjy MedSci原创 发表于上海
尽管EOAD患者的NPS负担较重,但这种负担在一定程度上可能由年龄因素驱动。
阿尔茨海默病是一种常见的神经退行性疾病,表现为认知功能的逐渐丧失,并伴有多种神经精神症状。这些症状不仅影响患者的生活质量,也给护理人员带来巨大负担。早发性阿尔茨海默病通常在65岁之前发病,而晚发性则在65岁之后发病。尽管已有研究表明EOAD患者的NPS负担可能更重,但这种差异是否由年龄因素引起尚不明确。

本研究纳入了NACC数据库中2940名EOAD患者、8665名LOAD患者以及8775名CU个体。CU个体分为早期认知正常(early-CU)组和晚期认知正常(late-CU)组,以匹配EOAD和LOAD患者的年龄段。使用Neuropsychiatric Inventory Questionnaire(NPI-Q)评估NPS的存在性和严重程度,采用多元逻辑回归模型分析NPS在EOAD和LOAD患者中的差异,并调整性别、教育水平、疾病严重程度和精神药物使用等协变量。
表1:参与者的人口统计学特征
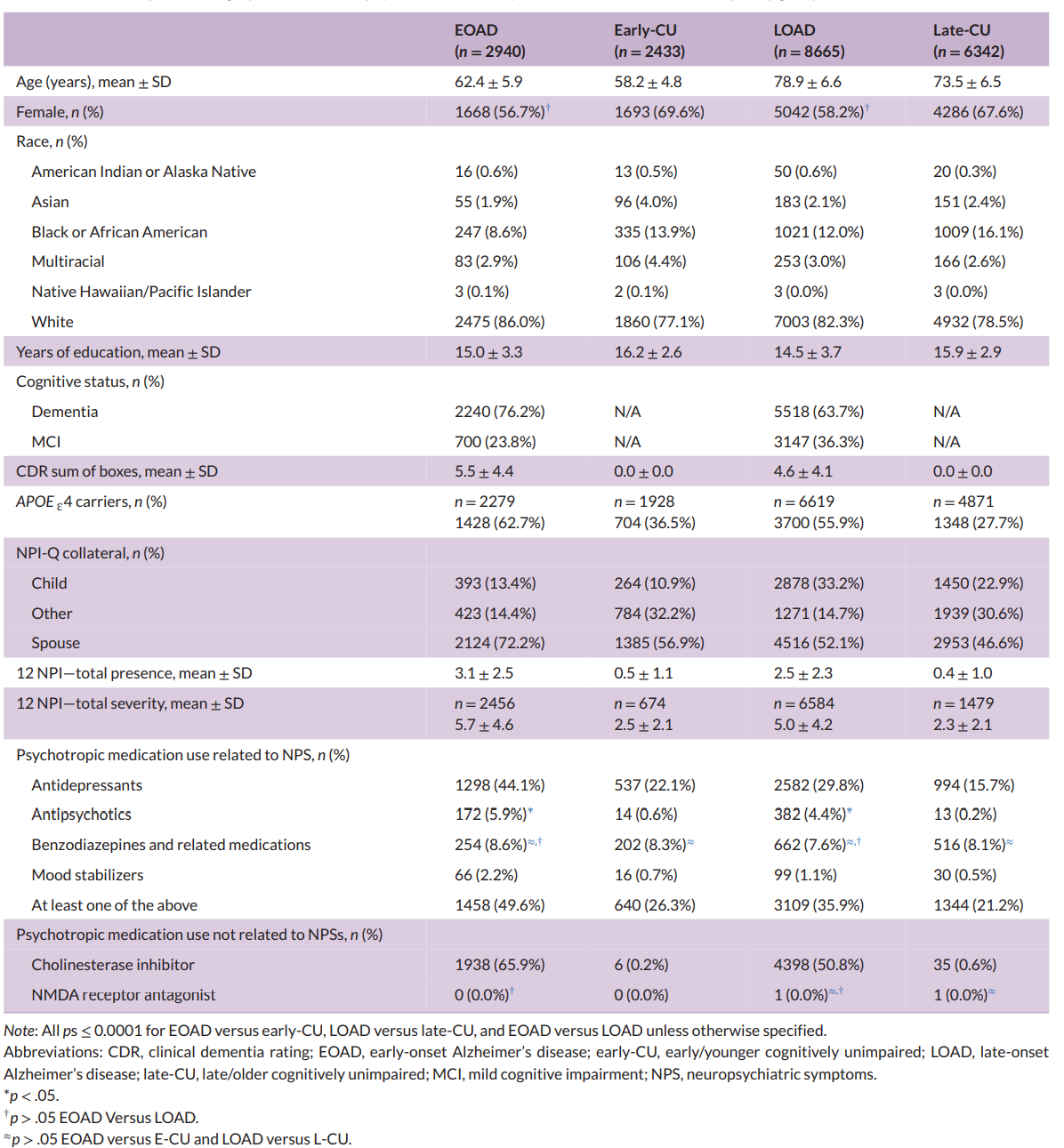
结果显示,EOAD患者的NPS存在率显著高于LOAD患者,尤其是在欣快、夜间行为和食欲/进食行为方面。具体而言,EOAD患者的欣快症状发生率是LOAD患者的3.41倍(95%CI:1.39-8.33),食欲/进食行为问题的发生率是1.36倍(95%CI:1.04-1.78),而夜间行为问题的发生率则低于LOAD患者(OR=0.77,95%CI:0.64-0.93)。

图1:不同组别参与者报告的各项神经精神症状的发生率
在症状严重程度方面,EOAD患者的焦虑和易怒症状显著严重于LOAD患者。然而,调整协变量后,除了夜间行为问题外,其他症状的严重程度在EOAD和LOAD患者之间无显著差异。进一步分析发现,EOAD和LOAD患者在轻度认知障碍(MCI)和痴呆阶段的NPS模式也存在类似的年龄和诊断组别交互作用。
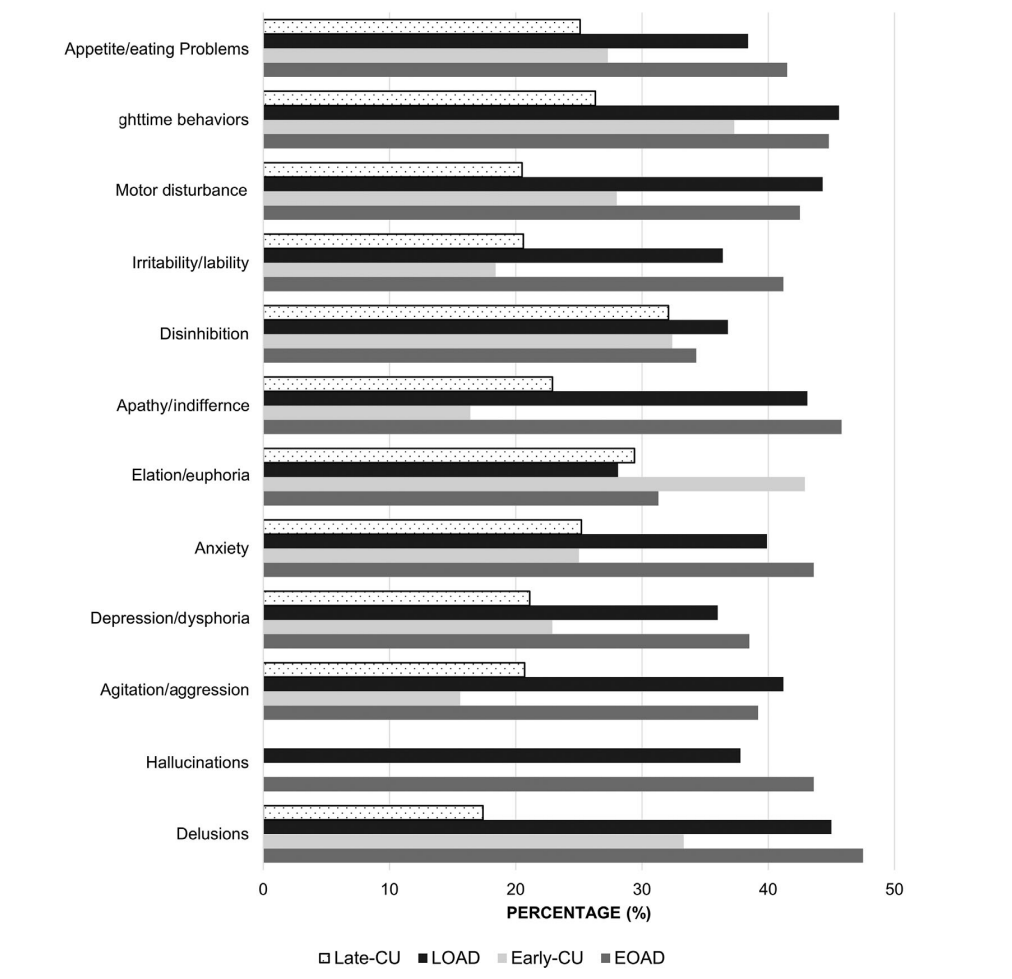
图2:仅限于报告了某项神经精神症状的参与者,不同组别中报告中度或重度症状的比例
本研究表明,尽管EOAD患者的NPS负担较重,但这种负担在一定程度上可能由年龄因素驱动。具体来说,较年轻的个体无论是否患有认知障碍,都更容易出现NPS。尽管如此,EOAD患者的较高NPS负担仍对患者及其护理人员的健康和心理社会结果产生了负面影响。因此,迫切需要探索症状管理策略,并为EOAD患者的护理人员开发心理教育干预措施。
原始出处:
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言
















#阿尔茨海默病#
20