强生单剂新冠疫苗综合有效率达66%,康希诺继续推进Ad5-nCoV的III期临床试验
2021-02-01 JACKZHAO MedSci原创
美国强生公司29日表示,旗下杨森研发的JNJ-78436735也称为Ad26.COV2.S对中重度新冠病例的预防总有效率达66%,对严重病例的有效预防则达85%。

美国强生公司29日表示,旗下杨森研发的JNJ-78436735也称为Ad26.COV2.S名为ENSEMBLE超过4万人的三期临床研究中,显示该疫苗对中重度新冠病例的预防总有效率达66%,对严重病例的有效预防则达85%。
但强生疫苗数据也呈现一个令人担忧的现象。其中期分析发现该疫苗的有效率在研究中的不同地区有差异,在美国的有效率为72%,在拉丁美洲的有效率为66%,南非为57%,这意味着该疫苗对新的病毒变种效果不佳。
强生公司新闻稿中表示,在三期临床试验中,这款疫苗在44325名18岁及以上成年志愿者当中似乎显出总体上的安全性以及良好的耐受性,尽管一些志愿者报告了发烧等副作用。其研发的单剂量新冠疫苗满足了所有主要和主要要求次要终点。最早在第14天就观察到了保护作用的开始。共同主要终点分别为疫苗接种后14天和28天。随着时间的流逝,针对严重疾病的效力不断提高,在接种疫苗的参与者中,第49天之后没有病例报告。
疫苗接种后28天,JNJ-78436735候选疫苗表现出了针对新冠肺炎患者相关住院和死亡的完全保护。疫苗对需要医疗干预的新冠肺炎病例有明显效果(住院,ICU入院,机械通气,体外膜氧合(ECMO))。

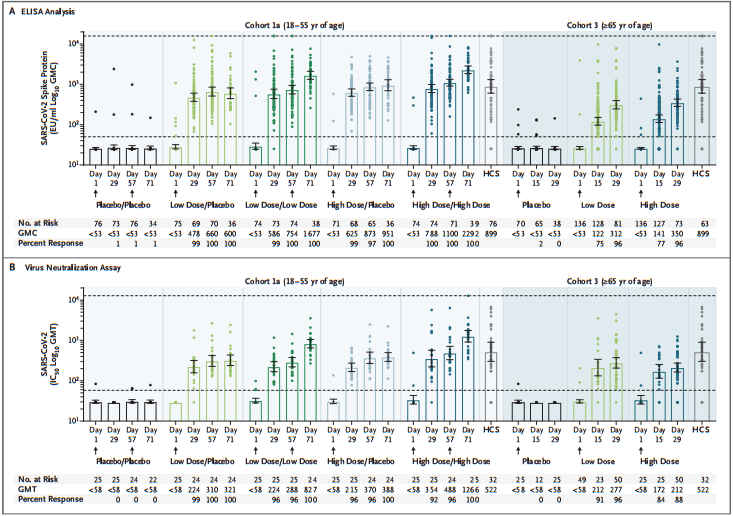
Ad26.COV2.S免疫原性
Jerald Sadoff et al. Interim Results of a Phase 1-2a Trial of Ad26.COV2.S Covid-19 Vaccine. N Engl J Med,January 13,2021.DOI: 10.1056/NEJMoa2034201
其试验中期结果已于本月1月13日)发表在《新英格兰医学杂志》(NEJM)上,共有805位18岁及以上的人群参与了1-2a期试验。结果显示,其开发的试验性新冠疫苗(Ad26.cov2-s)在早期安全性试验研究中已显示出持久的免疫反应,在单剂接种后至少能诱发71天的免疫反应,这可能意味着一剂疫苗就足以预防新冠病毒。
有别于辉瑞和莫德纳所研发的疫苗,强生疫苗目前是市面上唯一的单剂新冠疫苗。该疫苗可以在一般冰箱中保存3个月,而来自辉瑞和莫德纳的疫苗则必须保持冷冻状态。由于强生疫苗有可能成为第一种仅需一剂就有成效的冠病疫苗,从而使大规模疫苗接种活动变得更加简易,顶级传染病专家一直密切关注其疫苗的进展。
强生公司计划于2月初在美国申请紧急使用授权,有望在3月获得许可,此前强生称,美国将在今年上半年获得1亿剂疫苗。

http://www.cansinotech.com.cn/upload/1/editor/1612147168553.pdf
今日早间,我国疫苗公司也传出利好消息,康希诺生物在港交所早间发布公告称:公司已接获IDMC的通知,在本次中期分析中,重组新型冠状病毒疫苗(腺病毒5型载体)Ad5-nCoV成功达到预设的主要安全性及有效性标准,无任何与疫苗相关的严重不良事件发生,因此公司可继续推进Ad5-nCoV的III期临床试验。
公告称,Ad5-nCoV的III期临床试验已在三个大洲中的五个国家之78家临床研究中心完成对4万余受试者的接种,该试验由来自七个国家的全球主要研究者(global PI)、全球协同主要研究者(global co-PI)及各国协同主要研究者(country co-PI)共同领导,并遵循严格的伦理标准及严谨的科学准则。
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言











#I期临床试验#
72
#II期临床试验#
55
#III#
55
#I期临床#
47
#强生#
71
#II期临床#
54
#III期临床试验#
60
#III期#
44
怎么比辉瑞的低了这么多
113
新冠肺炎,疫情何时才能消失
61