Science:癌症纳米医学新突破,大规模筛选揭示决定纳米颗粒递送效率的基因组因素
2022-07-25 王聪 “生物世界”公众号
虽然使用纳米颗粒作为载体递送抗癌药物是治疗癌症有潜力的方式,还能避免化疗导致的副作用,但到目前为止,只有少数基于纳米颗粒的抗癌药物获得FDA批准上市。
两款新冠mRNA疫苗的获批上市和大规模接种,让所有人看到了脂质纳米颗粒(LNP)作为递送载体的巨大潜力。除了用来递送疫苗,基于纳米颗粒(NP)的疗法在个性化癌症治疗方面同样潜力巨大,纳米颗粒能够封装一系列货物,包括小分子、生物制剂、核酸等。因此,可以设计装载治疗药物的纳米颗粒,用于防止治疗药物在递送过程中的意外降解,增加其在体内的循环时间,以及将药物特异性递送到肿瘤等特定组织中。
虽然使用纳米颗粒作为载体递送抗癌药物是治疗癌症有潜力的方式,还能避免化疗导致的副作用,但到目前为止,只有少数基于纳米颗粒的抗癌药物获得FDA批准上市。
成功的纳米颗粒靶向递送面临的一大挑战是对靶标部位的纳米-生物相互作用的理解还不够深入,而癌症类型和靶点的多样性意味着全面理解哪些纳米颗粒特性决定成功的递送和靶向是一个艰巨的挑战。
2022年7月22日,麻省理工学院(MIT)和Broad研究所的研究人员在 Science 期刊发表了题为:Massively parallel pooled screening reveals genomic determinants of nanoparticle delivery 的研究论文。
该研究分析了35种不同类型的纳米颗粒与近500种癌细胞之间的相互作用,进而揭示了影响这些癌细胞吸收不同类型纳米颗粒的数千种生物学特征。该研究发现了SLC46A3蛋白是细胞对基于脂质的纳米颗粒的吸收的负调节剂和潜在生物标志物。
这些发现有助于更好地针对特定癌症类型定制药物递送纳米颗粒载体,或利用特定癌症的细胞生物学特征定制新型纳米颗粒载体,以克服当前开发基于纳米颗粒的药物所面临的障碍。

该论文的通讯作者、麻省理工学院教授、化学工程系主任 Paula Hammond 表示对于这些发现感到兴奋,可以用这种方法来确定哪种类型的纳米颗粒最适合靶向某些细胞类型,从癌细胞到免疫细胞以及其他类型的健康或患病器官的细胞,而这只是一个开始。
Paula Hammond 实验室此前已经开发出了多种类型的纳米颗粒,这些纳米颗粒可用于将药物递送到细胞中。在进一步研究中,他们发现,不同类型的癌细胞通常对同一种纳米粒颗粒表现出不同的反应。他们认为,细胞之间的生物学差异可能是导致这种不同反应的原因。
为了搞清楚这些不同反应背后真正的原因,研究团队进行了一项大规模研究,以观察大量不同的细胞与多种不同类型的纳米颗粒之间的相互作用。
研究团队借助Broad研究所的PRISM平台,该平台可以同时在数百种不同癌细胞类型中快速筛选数千种药物。研究团队对PRISM平台进行了调整,将细胞-药物相互作用改为筛选用细胞-纳米颗粒相互作用,用来评估细胞的基因型特征是否可以预测细胞对纳米颗粒的吸收效果。
研究团队使用了来自22个不同组织的488种癌细胞系。每种癌细胞类型都带有独特的DNA序列“条形码”,因此可以在后续筛选中识别这些细胞。对于每种癌细胞类型,还提供有关其基因表达谱和其他生物学特征的大量数据集。
研究人员构建了35种不同类型的纳米颗粒,每种纳米颗粒的核心由脂质体、PLGA或聚苯乙烯组成。研究团队还用不同类型的保护或靶向分子包裹这些纳米颗粒,例如聚乙二醇、抗体或多糖等聚合物,从而能够研究纳米颗粒核心成分和纳米颗粒表面化学的影响。
研究团队将这数百种不同的癌细胞暴露于35种不同纳米颗粒中的一种,每种纳米颗粒都有一个荧光标签,从而可以使用细胞分选技术在暴露后4小时或24小时后发出的荧光量来分选细胞。基于这些测量,每种癌细胞系被分配一个分数,代表其对每种纳米颗粒的亲和力。然后,研究团队使用机器学习算法来分析这些分数以及每种癌细胞系可用的所有其他生物学数据,进而确定了介导纳米颗粒运输的细胞特征。
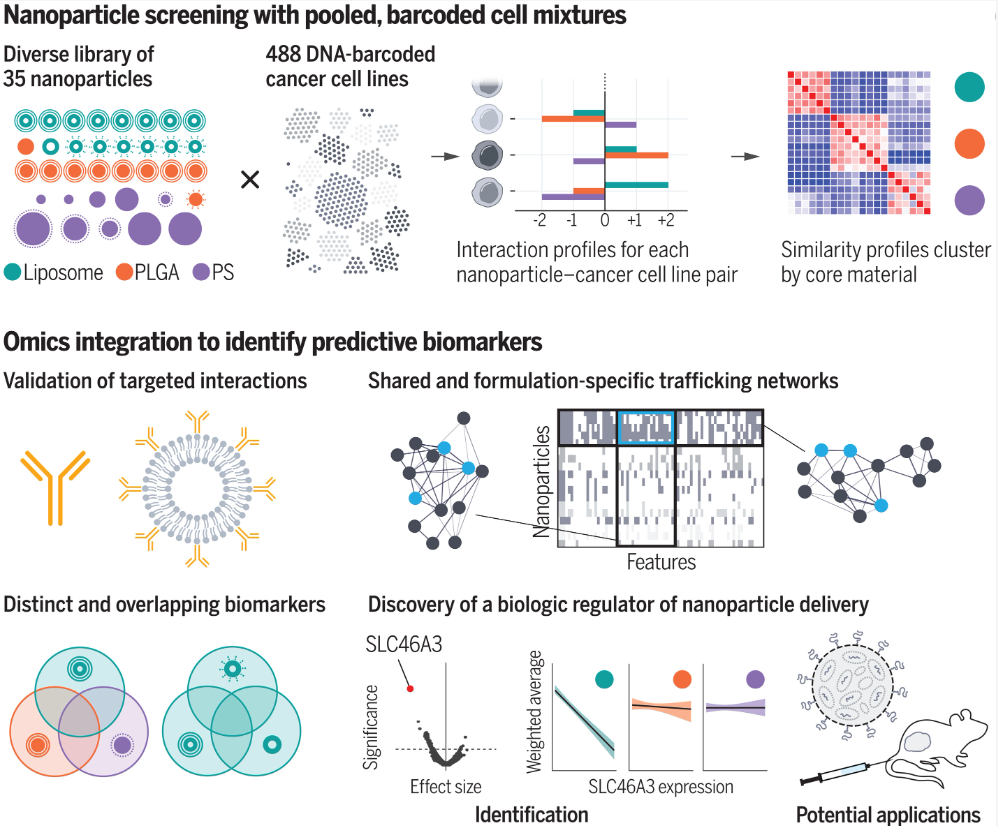
这些分析产生了数千个与不同类型纳米颗粒的亲和力相关的特征或生物标志物。该研究发现,决定癌细胞对纳米颗粒的摄取的主要因素是纳米颗粒的核心组分,而不是过去认为的表面材料和修饰。
而在这些癌细胞的生物标志物中,有许多是编码结合纳米颗粒、将它们带入细胞或处理它们所需的细胞机制的基因。已知其中一些基因与纳米颗粒的转运有关,但大多数相关基因是新发现的。
研究团队从中挑选了一种新发现的生物标志物——SLC46A3,进行进一步研究。SLC46A3是一种溶酶体转运蛋白,这种蛋白的高水平表达与细胞对纳米颗粒的低摄取量相关。这项研究表明,SLC46A3蛋白是细胞对基于脂质的纳米颗粒的吸收的负调节剂和潜在生物标志物。
研究团队在黑色素瘤小鼠模型中进一步验证了这一点,因此,SLC46A3蛋白的表达水平可以作为一种生物标志物,帮助判断癌症患者是否会对基于纳米颗粒的疗法产生治疗反应。
目前FDA批准的用于抗癌治疗的纳米颗粒都是脂质体制剂,因此,SLC46A3蛋白作为一种生物标志物具有巨大潜力,能够帮助加速现有纳米颗粒的临床试验。
研究团队表示,目前正在探索SLC46A3蛋白调控细胞对纳米颗粒摄取的机制。如果能够找到好的降低SLC46A3蛋白水平的方法,将有助于提高纳米颗粒向癌细胞递送的效率,从而帮助更好地治疗癌症。
最后,研究团队总结道,这项研究代表了通过多组学探索纳米颗粒-癌细胞相互作用的高通量研究。为科学界提供了一个广阔蓝图,用于研究更多的纳米颗粒和其他未知的生物标志物,促进纳米-生物相互作用研究,推进纳米颗粒载体的合理设计。
原始出处:
NATALIE BOEHNKE, et al. Massively parallel pooled screening reveals genomic determinants of nanoparticle delivery. SCIENCE, 22 Jul 2022, Vol 377, Issue 6604.
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言











#纳米医学#
63
#新突破#
92
#大规模#
73
#纳米颗粒#
85
#SCIE#
79
#筛选#
72