Radiology:基于MRI的阿尔茨海默病谱系中淀粉样蛋白、Tau蛋白和神经退行性变生物标志物状态的深度学习评估
2024-06-13 shaosai MedSci原创 发表于上海
最新研究显示,深度学习技术可以检测MRI数据中的复杂模式,并具有无创表征ATN状态的潜力,已应用于临床多项研究中。
阿尔茨海默病(AD)是一种病理性疾病,目前通常根据淀粉样蛋白、Tau蛋白和核蛋白生成的三种标志性异常的标记物来定义。代表病理学的标志物的组合定义了一个人的淀粉样牛磺酸变性 (ATN)状态,这一研究结构提供了AD的生物学定义以及导致痴呆的病理生理事件和多因素的特征。 随着生物标志物在临床研究中对患者的选择和分类的应用不断增加,对广泛应用的生物标志物的需求也在增加。
ATN系统是通过将三种病理类型的中阳性或阴性标记状态与脑脊液(CSF)A或B淀粉样蛋白的存在相结合来实现的。
PET可用于阿尔茨海默病的淀粉样蛋白-tau神经变性(ATN)分类,但会产生相当大的成本和暴露于电离辐射。MRI目前在诊断ATN状态方面应用有限。深度学习技术可以检测MRI数据中的复杂模式,并具有无创表征ATN状态的潜力。

近日,发表在Radiology杂志的一项研究利用MRI和现成的诊断数据,评估了使用深度学习预测PET确定的ATN生物标志物状态。
本项研究回顾性收集来自阿尔茨海默病影像学倡议的MRI和PET数据。从2005年8月到2020年9月,PET扫描与30天内获得的MRI扫描配对。对随机分成以下子集:70%用于训练,10%用于验证,20%用于最终测试。使用双峰高斯混合模型将PET扫描阈值划分为正、负标签。MRI数据被输入卷积神经网络生成成像特征。将这些特征与患者人口统计学、APOE基因状态、认知评分、海马体积和临床诊断结合在一个逻辑回归模型中,将每个ATN生物标志物成分分类为阳性或阴性。采用受试者工作特征曲线下面积(AUC)分析对模型进行评价。特征重要性由模型系数和梯度得到。
淀粉样蛋白2099个(患者平均年龄75岁±10岁[SD];1110名男性),557名tau(患者平均年龄75岁±7岁;男性280例),FDG PET 2768例(患者平均年龄75岁±7岁;1645名男性)和MRI配对。测试集的模型AUC如下:淀粉样蛋白,0.79 (95% CI: 0.74, 0.83);tau, 0.73 (95% CI: 0.58, 0.86);神经退行性疾病,0.86 (95% CI: 0.83, 0.89)。在神经网络中,高梯度存在于关键的颞、顶叶、额叶和枕叶皮质区域。认知评分、海马体积和APOE状态的模型系数最高。
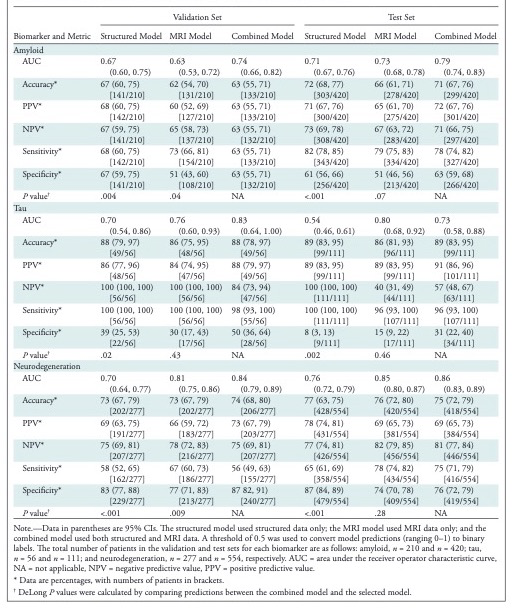
表 在验证集和测试集上使用结构化模型、MRI模型和组合模型确定淀粉样蛋白、Tau蛋白和神经退行性生物标志物阳性的性能
本项研究表明,利用MRI和其他可用的诊断数据,深度学习算法可预测PET确定的ATN状态的各个组成部分,且具有可接受到优异的效果。
原文出处:
Christopher O Lew,Longfei Zhou,Maciej A Mazurowski,et al.MRI-based Deep Learning Assessment of Amyloid, Tau, and Neurodegeneration Biomarker Status across the Alzheimer Disease Spectrum.DOI:10.1148/radiol.222441
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言
















利用MRI和其他可用的诊断数据,深度学习算法可预测PET确定的ATN状态的各个组成部分。
44
#阿尔茨海默病# #淀粉样蛋白# #tau蛋白#
41