俞飚院士/王婧/房鹏飞/郭敏等报道高效、特异MITF小分子抑制剂,体内有效抑制恶性黑色素瘤的生长和转移
2023-02-08 精准药物 精准药物 发表于上海
1月2日,Cell Research发表了中国科学院上海有机化学研究所王婧研究员、俞飚院士研究团队等合作的最新研究成果“特异靶向恶性黑色素瘤关键转录因子MITF的小分子化合物研发”。
1月2日,Cell Research发表了中国科学院上海有机化学研究所王婧研究员、俞飚院士研究团队、房鹏飞研究员、郭敏研究员、哈佛大学麻省总医院David E. Fisher教授、复旦大学附属肿瘤医院陈勇主任合作的最新研究成果“特异靶向恶性黑色素瘤关键转录因子MITF的小分子化合物研发”。这项工作首次报道了具有明确靶向机理,高效特异的恶性黑色素瘤关键致癌因子MITF小分子抑制剂。

恶性黑色素瘤是起源于黑色素细胞的肿瘤,是最难以治疗的恶性肿瘤之一,90%的靶向治疗患者会在治疗5~7月后出现耐药性。寻找高效的恶性黑色素瘤治疗靶点,同时结合免疫、靶向方案提高治疗响应率,降低复发率是恶性黑色素瘤治疗的重大问题。
MITF(Microphthalmia transcription factor)是恶性黑色素瘤发生、转移、以及耐药性形成起关键作用的转录因子,是黑色素瘤最为重要的直系致癌基因,也是治疗恶性黑色素瘤最具突破性的靶点之一。然而,作为转录因子,由于缺少配体结合口袋, MITF长期以来被认为是“不可靶向的”,直接、高效、特异靶向MITF的小分子化合物目前没有被报道过。
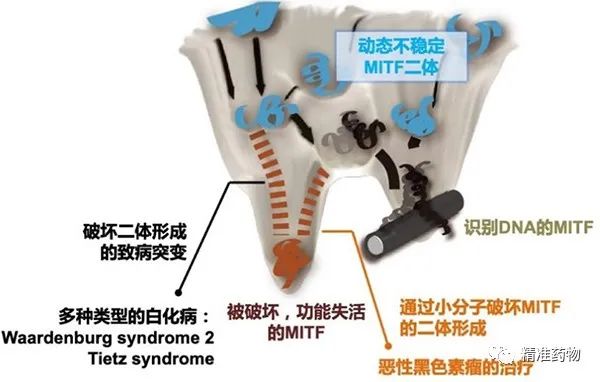
图1 基于MITF的“动态不稳定性”,建立特异靶向机制
MITF的功能发挥依赖于其二体“亮氨酸拉链”的形成。通过对MITF功能缺失导致的白化病突变进行分析,研究团队发现该二体具有独特的动态不稳定性且对内外干扰非常敏感,并由此提出了小分子破坏MITF二体形成来特异抑制MITF的靶向机制。基于上述机制,团队进一步发现了小分子化合物TT012,在生化和细胞水平高效破坏MITF的二体形成,在全基因组水平特异抑制MITF转录活性,在多种动物模型中对MITF高表达的肿瘤表现良好肿瘤抑制活性。综上,团队首次研发了具有明确靶向机理,高效特异的MITF小分子抑制剂,为恶性黑色素瘤治疗提供全新的潜在靶向新药。
该项工作在Cell Research 杂志在线发表(https://doi.org/10.1038/s41422-022-00744-5),化合物获美国专利授权一项(US 11077097B2)。在对该项工作的亮点点评中,Sanford Burnham Prebys研究所Ze’ev A. Ronai教授指出,“Liu等人的研究代表了黑素瘤靶向治疗的重要进展,新发现的化合物可能具有重要的临床意义。鉴于关键调控基因的遗传扰动在癌症中很常见,目前的研究可能还具有超越MITF的重要意义。”(https://doi.org/10.1038/s41422-022-00762-3)。
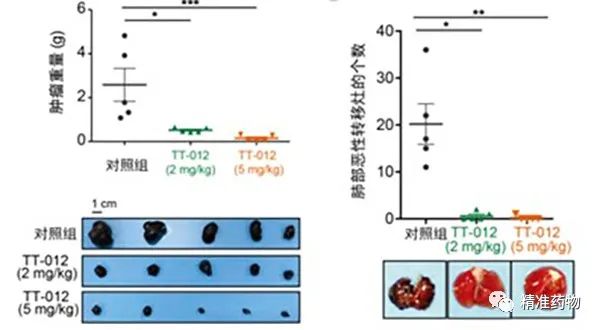
图2 MITF小分子抑制剂TT012高效抑制恶性黑色素瘤生长和转移
上海有机所博士生刘载舟、华南理工大学博士生陈凯歌为该论文的第一作者,上海有机所王婧研究员、房鹏飞研究员、郭敏研究员、俞飚院士、哈佛大学麻省总医院David E. Fisher教授、复旦大学附属肿瘤医院陈勇主任为该论文的共同通讯作者。这项工作得到了华南理工大学王均教授,上海有机所董家佳研究员、曹春阳研究员,潘李锋研究员的大力支持。该研究得到了国家自然科学基金委、中国科学院、上海市科委的项目资助。
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言