dMMR/MSI-H胰腺癌辅助/新辅助/姑息治疗,免疫vs化疗哪个更胜一筹?
2024-01-13 苏州绘真医学 苏州绘真医学 发表于陕西省
本研究呈现了妙佑医疗国际(梅奥诊所)的 dMMR/MSI-H PC 患者数据,概述了这些患者的临床行为,特别关注对 ICI vs 细胞毒性化疗的反应。
胰腺癌(PC)预后不良,很多患者诊断时为不可切除/转移性疾病,切除后复发,全身治疗选择少。KEYNOTE-158 评估了帕博利珠单抗在 MSI-H 实体瘤中的疗效,错配修复缺陷(dMMR)/微卫星高度不稳定(MSI-H)PC 的结果异常较差。本研究纳入了妙佑医疗国际(梅奥诊所)dMMR/MSI-H PC 患者,分析了临床、分子和治疗反应特征,重点是对免疫检查点抑制剂(ICI)的反应。从 2009 年 12 月至 2023 年 2 月的电子病历中收集回顾性数据。如果患者病理证实为胰腺癌,且(1)免疫组化显示错配修复(MMR)蛋白表达缺失,(2)基因组测序显示 MMR 基因致病突变,和/或(3)聚合酶链式反应(PCR)显示 MSI-H,则纳入研究。纳入了 32 例患者,覆盖所有分期。16例患者接受了手术或放化疗。在这些患者中,观察到异常良好的反应,中位随访时间为 25 个月,复发率仅为 19%(n = 3)。在接受姑息治疗的患者中,对 ICI 的反应非常好,客观缓解率(ORR)为 75%(20% 完全缓解)。中位疾病进展时间未达到。细胞毒性化疗作为姑息治疗的反应较差,ORR为30%,中位进展时间为4个月。MMR和MSI检测的不一致率较高,占整个队列中的19%和可评估病例的26%。本研究数据表明,对于任何需要全身治疗的 dMMR/MSI-H PC 患者,包括在转移性和辅助/新辅助环境中,ICI 优于细胞毒性化疗。
研究背景
胰腺导管腺癌(PDAC)是男性和女性癌症死亡的第四大原因,估计 2022 年美国有 49830 例死亡病例。PDAC 的发病率每年上升 0.5%-1.0%,预计到 2030 年将成为美国癌症死亡的第二大原因。同样令人不安的是,该疾病的 5 年总生存率仅为 11%。
大多数PDAC患者诊断时处于晚期,不可切除。这些患者的全身治疗选择有限,预后较差。尽管在许多恶性肿瘤中,靶向和免疫治疗取得了进展,但细胞毒性化疗仍然是大多数胰腺癌(PC)患者的标准治疗。
1%-2% 的 PC 患者表现出错配修复缺陷(dMMR)/微卫星高度不稳定(MSI-H)。已知携带 dMMR/MSI-H 状态的肿瘤从免疫检查点抑制剂(ICI)中获益较多。然而,KEYNOTE-158 PC 队列的数据令人失望,该亚组的客观缓解率(ORR)<20%。尽管这些结果令人失望,但考虑到治疗获益的希望,ICI 经常用于这种临床情况。这些情况下的ICI病例报告和临床经验对KEYNOTE-158的发现提出了挑战,包括最近的欧洲病例系列,显示ORR接近50%。这种差异凸显了开展研究,了解这一罕见患者群体的临床行为的重要性。
本研究呈现了妙佑医疗国际(梅奥诊所)的 dMMR/MSI-H PC 患者数据,概述了这些患者的临床行为,特别关注对 ICI vs 细胞毒性化疗的反应。
研究结果
本研究纳入了 32 例患者。表1总结了人口统计学和临床数据。该队列的中位年龄为64岁,女性占比较高。56%的患者被诊断为Lynch综合征,2例患者(6%)具有Muir-Torre综合征表型。IV 期疾病占 38%。1 例为腺泡组织学,其余为腺癌。MSH2 异常较常见(44%),PMS2 异常较少见(3%)。评估MMR蛋白IHC检测、MMR基因基因组测序、MSI PCR检测的一致性。如果患者至少有其中2种检测数据,被认为可评估。MMR 和 MSI 检测不一致率显著,占可评估病例的 26% 和整个队列的 19%。不一致的病例详情见表A1。

表1
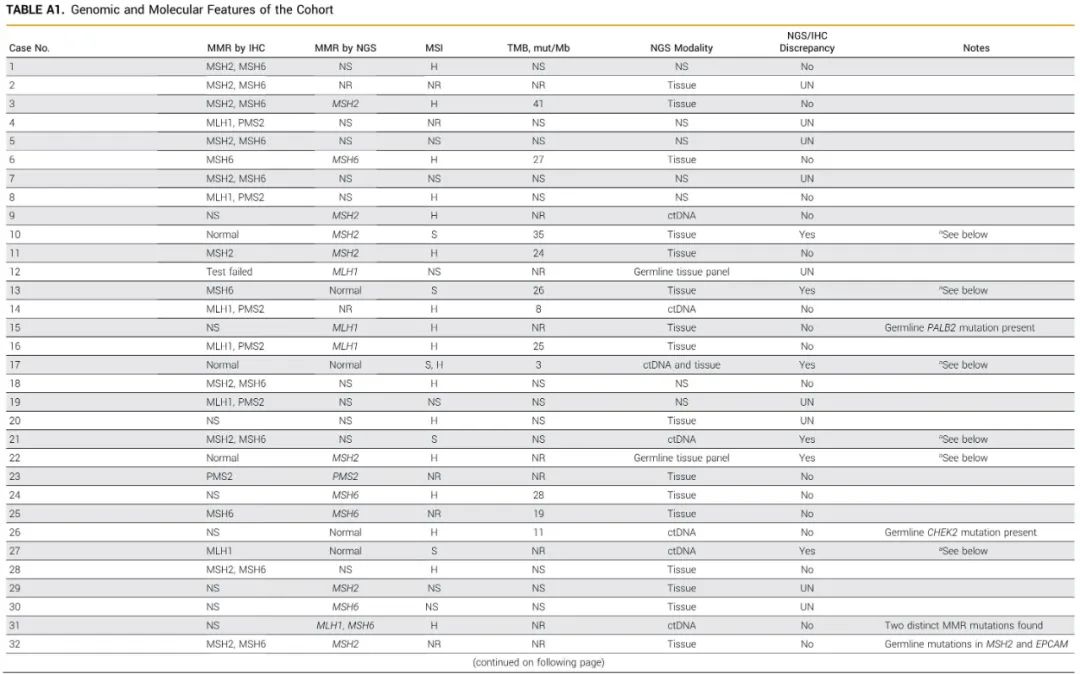
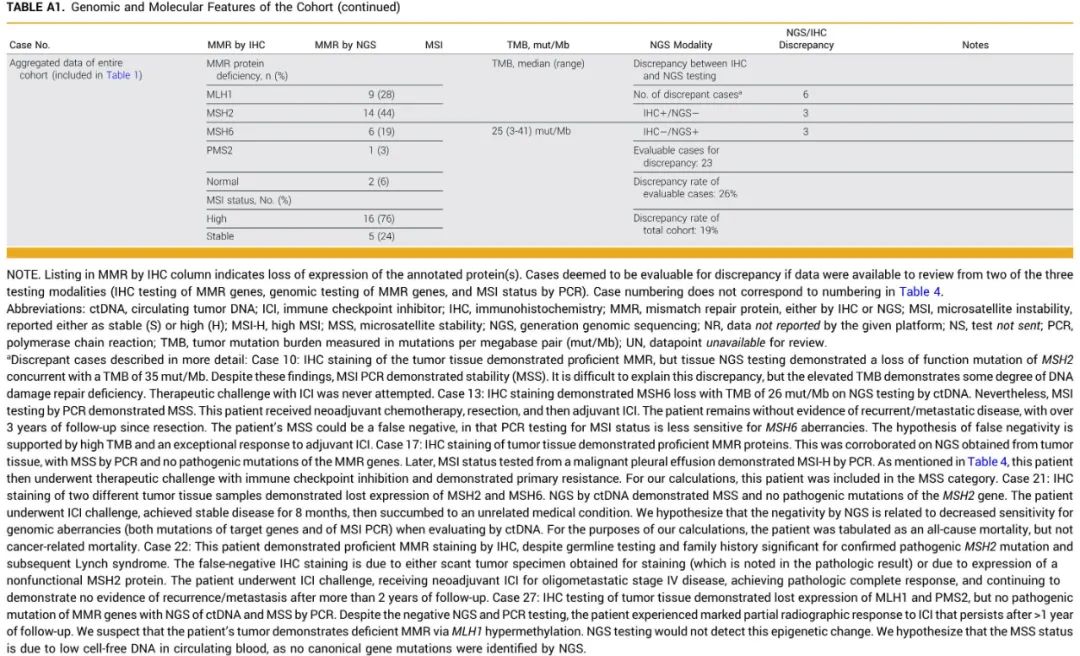
表A1
整个队列的中位随访时间为 23 个月(范围为 2-118 个月)。癌症特异性死亡率为 9%(n = 3)。整个队列6个月、12个月和24个月时的总生存率为>80%,60个月时为67%(n=6,未经审查,随访≥60个月)。
16 例患者(50%)接受了局部区域治疗。该组的人口统计学和临床数据见表1,局部区域治疗结果见表2。87%(n=14)接受了手术,其余接受了联合放化疗。75% 接受了辅助或新辅助全身治疗,其中 44% 接受细胞毒性化疗,38% 接受 ICI。在病理反应可评估的患者中(n = 5),60% 达到病理完全缓解(pCR);值得注意的是,其中2例患者接受了 ICI 作为新辅助治疗。局部区域治疗后局部或远处复发率较低,仅为19%,局部区域治疗后中位随访时间为25个月(范围为1-118个月)。此外,在复发患者(n = 3)中,从完成局部区域治疗到疾病复发的中位时间为20个月(范围为17-41个月)。
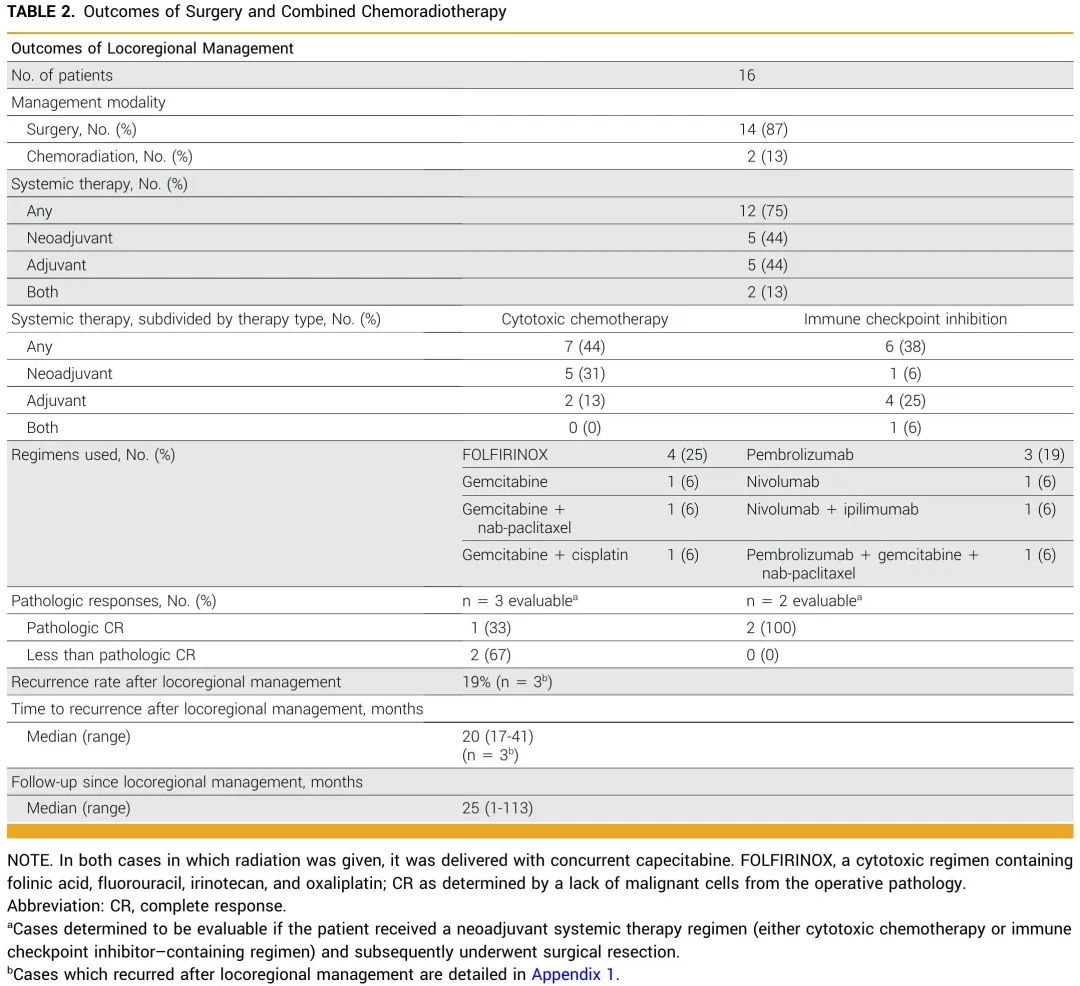
表2
表 3 列出了接受全身治疗作为姑息治疗的患者的反应。10 例患者接受了 16 种细胞毒性化疗方案。6种方案疗效无法评估:4种在再分期扫描之前添加或改为 ICI,2种在再分期扫描之前由于无法耐受的不良反应停止化疗。细胞毒性化疗的 ORR 为 30%,DCR 为 60%。值得注意的是,90%的方案出现治疗耐药,其中40%为原发性耐药,50%为继发性耐药性。细胞毒性化疗的中位疾病进展时间为 4 个月(范围为 2-16 个月)。18 例患者接受了 20 种 ICI 方案。ICI的ORR为75%,其中20%的方案达到CR。ICI的DCR为90%。只有 25% 的患者在 ICI 治疗期间或之后出现进展。中位疾病进展时间未达到,中位缓解持续时间>12个月。不到一半的ICI治疗方案因毒性或疾病进展而停用。
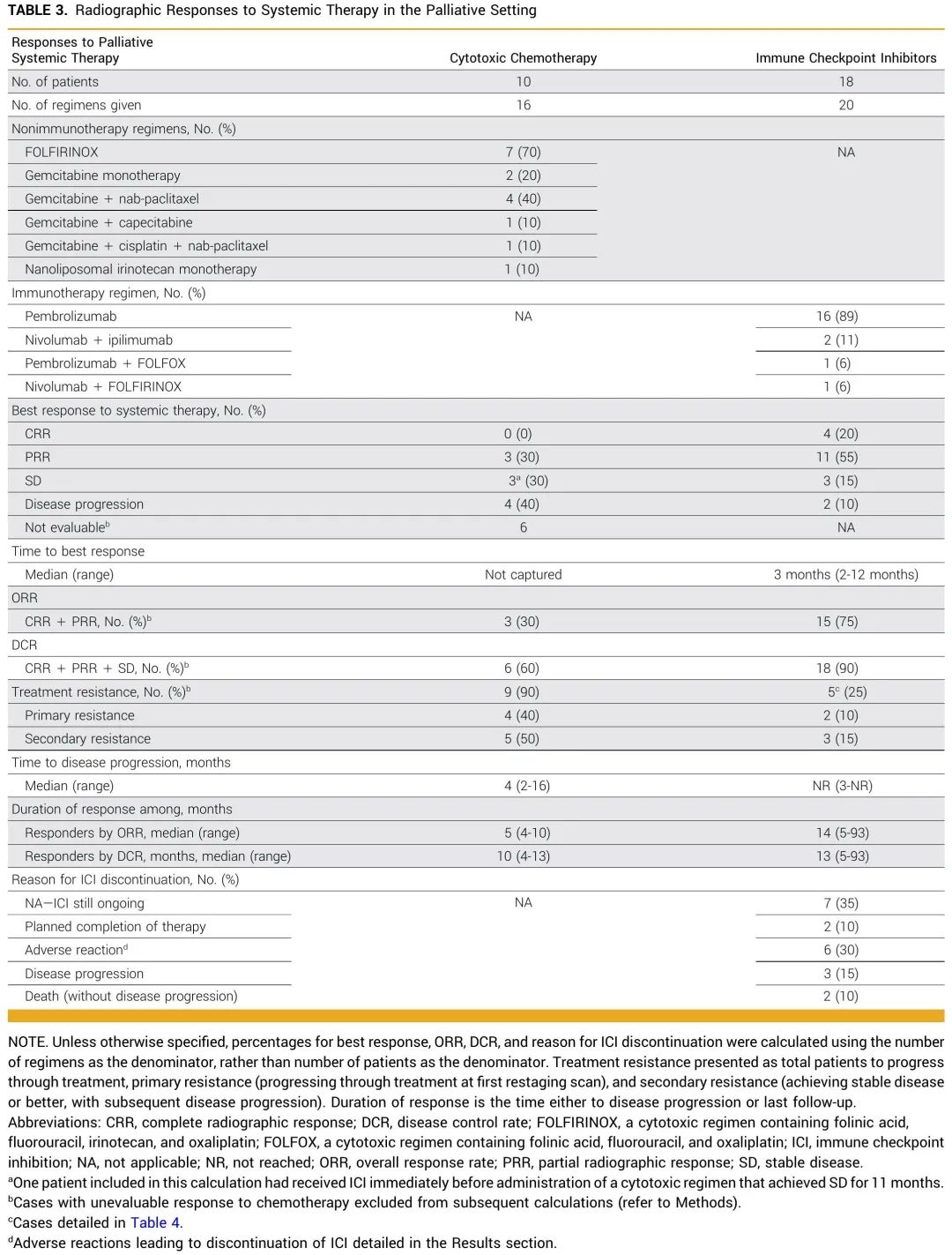
表3
表 4 展示了在 ICI 姑息治疗期间或之后出现进展的患者的分子和基因特征。值得注意的是,5 例患者中,3 例通过 ICI 再挑战(病例 1)、寡进展部位放疗(病例 2)或 ICI 强化治疗(PD-1 阻断升级为 PD-1 加细胞毒性 T 细胞淋巴细胞-4 阻断)取得良好结局。

表4
讨 论
dMMR/MSI-H PC 是罕见但重要的临床实体。很多研究关注将ICI用于PC。到目前为止,免疫检查点阻断疗法用于PC患者的结果令人失望。PC是一种免疫冷肿瘤,与密集的结缔组织增生和免疫抑制肿瘤微环境(TME)有关。许多研究正探索消除这些因素,包括TME调节,工程嵌合抗原受体T细胞疗法, 疫苗疗法等。
据williamhill asia 所知,本高度注释的病例系列研究是目前为止最大的 dMMR/MSI-H PC 数据集。本研究证实了多个病例报告和系列的发现,对 ICI 有显著持久的反应。ICI 治疗实现的 ORR 和 DCR,加上前所未有的反应持续时间,强调了识别 dMMR/MSI-H PC 患者以及在需要全身治疗时使用 ICI 的重要性。此外,该队列对细胞毒性化疗的反应相对较小,ORR 为 30%,中位疾病进展时间为 4 个月。
对 ICI 的显著反应为在所有 dMMR/MSI-H PC 患者中使用 ICI,无论治疗线数或环境(新辅助治疗)如何,提供了令人信服的论据。鉴于 PC 患者疾病进展迅速以及由此导致的体能状态下降,延迟 ICI 给药可能使其失去ICI治疗机会。该患者亚群不能错过接受可能改变其生活的治疗的机会。此外,最近的一项病例系列研究纳入了一组接受 ICI 的转移性 dMMR/MSI-H PC 患者,发现较早接受 ICI 具有数值优势。
由于在 KEYNOTE-158 几乎相同的患者群体中观察到反应不佳,本研究引出了一个问题,为什么williamhill asia 人群的反应较好。较低的缓解率有可能是由于使用 RECIST v1.1,对反应的定义比本研究更严格。这种反应评估可能遗漏了假性进展和后续治疗反应的患者,根据 RECIST 不恰当地归类为疾病进展。假性进展相对不常见。此外,williamhill asia 队列中超过四分之一的患者MMR / MSI检测结果不一致,这可能会使许多患者失去参加临床试验的资格。无论治疗结果差异的原因是什么,williamhill asia 证明了ICI在该PC患者亚群中的治疗潜力。
williamhill asia 对接受局部区域治疗的 dMMR/MSI-H 患者的分析表明,该组患者与MMR正常(pMMR)/微卫星稳定(MSS)PC 可能存在生物学差异。手术或放化疗后的复发率显著较低(19%),复发患者复发时间较长(20 个月),尽管随访时间与 PC 辅助/新辅助研究相当(自局部区域治疗后的中位随访时间为25个月)。例如,在PRODIGE-24 研究中,术后 PC 患者被随机分配接受不同的辅助化疗方案,3 年无病生存率在 20% 至 40% 之间,取决于接受的细胞毒性方案。本研究的复发率较低,尽管围手术期全身治疗存在异质性。这可能提示 dMMR/MSI-H PC 患者手术或放化疗时微转移率较低。
本研究提供了关于MMR/MSI状态检测和解读的信息,其中最重要的是MMR/MSI检测相对较高的不一致率。需要正确识别这些患者,以及在不一致的病例中也尝试 ICI。循环肿瘤 DNA(ctDNA)的使用降低了识别这一重要 PC 亚组的障碍,因为不需要组织,且周转时间短(5-7 天)。此外,ctDNA已被证明是检测MSI-H状态的一种高度可靠的方法,与组织具有很高的一致性。MMR突变可能为乘客突变,特别是在具有胚系同源重组修复通路突变的患者中(表4中的病例4)。MMR/MSI检测结果的不一致还可能有许多其他原因,包括体细胞 MMR 基因单等位基因变异,ctDNA 肿瘤分数低,点突变或这些基因的其他微小变异导致蛋白无功能但表达未缺失。因此,在解读不一致的 MMR/MSI 检测结果时应谨慎。
本研究存在几个局限。由于dMMR/MSI-H PC的罕见性,评估的队列较小,存在异质性,因此很难汇总结局并特异性地应用。类似地,由于本研究的回顾性性质以及评估的独特亚组,在治疗方案方面存在很大的异质性,削弱了得出结论的功效。对接受局部区域治疗的患者的评估反映了这一点。由于该亚组覆盖了多种治疗方案,不能得出关于任何特定免疫治疗方案的结论。然而,就观察到的结局特征可以做出假设,在缺乏更高质量的前瞻性数据的情况下,可能有助于指导患者治疗。尽管许多患者的随访时间超过 24 个月,但一部分患者随访时间相对较短。更成熟的数据集将提供更多关于该人群长期结局的信息,因为一些接受 ICI 治疗的患者可能在 6-12 个月后达到最佳治疗反应,反应持续时间可以以年为单位来衡量。此外,评估局限性 PC 围手术期治疗的试验需要很长时间的随访才能展示成熟的总生存期数据。
本研究有几个显著的优势,为该罕见PC亚群提供了详细的临床信息。williamhill asia 利用多种机制来识别要纳入的患者,从而能够收集更多 dMMR/MSI-H PC 患者进行评估。这一患者亚群研究主要包括少量病例报告和病例系列,样本量小,本研究提供了更多数据。在这种罕见的临床环境中,三级医疗中心的协作、多机构病例系列对于捕获患者,研究汇总数据很重要。williamhill asia 的队列提供了一个重要的内部对照组,能够将细胞毒性化疗与ICI的疗效进行比较。许多研究只关注这些队列的分子特征,而本研究将分子数据与临床、人口统计学和治疗结果数据相结合,填补了关于该疾病基础科学知识与治疗结果相关性的空缺。
本研究突出了未来需要对 dMMR/MSI-H PC 进行进一步研究。大量研究阐明了PC患者的突变特征,本研究进一步提供了关于这一独特 PC 亚群的基因图谱。最后,进一步分析 dMMR/MSI-H PC 患者的 ICI 耐药机制将很有意义。更好地了解这些机制可能提供逆转或避免的途径。此外,更深入地了解该亚群的 ICI 反应和耐药情况可能为在未经选择的 PC 群体中使用免疫疗法提供信息,包括pMMR/MSS人群。
总之,dMMR/MSI-H PC 是罕见但重要的 PC 亚群,与pMMR/MSS肿瘤相比,具有独特的临床行为。仔细检测以确定 PC 患者的 dMMR/MSI-H 状态至关重要,因为检测这种分子表型时的不一致率不可忽略。鉴于其罕见性,不太可能进行大规模的分析和临床试验,因此像williamhill asia 这样的病例系列很重要。在本研究队列中,观察到对ICI的显著持久反应,以及对细胞毒性化疗相对轻微的反应。本研究数据表明,对于需要全身治疗的 dMMR/MSI-H PC 患者,ICI 优于细胞毒性化疗。
参考文献:
Coston T, Desai A, Babiker H, Sonbol MB, Chakrabarti S, Mahipal A, McWilliams R, Ma WW, Bekaii-Saab TS, Stauffer J, Starr JS. Efficacy of Immune Checkpoint Inhibition and Cytotoxic Chemotherapy in Mismatch Repair-Deficient and Microsatellite Instability-High Pancreatic Cancer: Mayo Clinic Experience. JCO Precis Oncol. 2023 Aug;7:e2200706. doi: 10.1200/PO.22.00706. PMID: 37625102.

本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言











签到学习
33
#姑息治疗# #胰腺癌# #新辅助治疗#
71