NEJM:浙江大学黄河团队合作开发CAR T新方案,成功治疗难治性白血病
2024-04-27 iNature iNature 发表于上海
该研究在10例复发或难治性CD7阳性白血病或淋巴瘤患者中测试了一种新的“all-in-one”策略,包括序贯CD7 CAR-T细胞治疗和单倍体同种HSCT。
复发或难治性血液癌患者预后较差。嵌合抗原受体(CAR)T细胞治疗作为异基因造血干细胞移植(HSCT)的桥梁,具有长期消除肿瘤的潜力。然而,移植前骨髓消融和移植物抗宿主病(GVHD)预防药物具有毒性作用,可能会根除残留的CAR-T细胞并损害抗肿瘤作用。CAR-T细胞治疗与异体造血干细胞移植的结合是否能保持CAR-T细胞功能并改善肿瘤控制尚不清楚。
2024年4月24日,浙江大学黄河、胡永仙、王东睿及复旦大学张鸿声共同通讯(胡永仙、张明明及杨婷婷是本文并列第一作者)在 New England Journal of Medicine在线发表题为“Sequential CD7 CAR T-Cell Therapy and Allogeneic HSCT without GVHD Prophylaxis”的研究论文,该研究在10例复发或难治性CD7阳性白血病或淋巴瘤患者中测试了一种新的“all-in-one”策略,包括序贯CD7 CAR-T细胞治疗和单倍体同种HSCT。研究结果表明,序贯CD7 CAR-T细胞治疗和单倍体造血干细胞移植是安全有效的,具有缓解和严重但可逆的不良事件。该策略为CD7阳性肿瘤患者提供了一种可行的方法,这些患者不适合进行传统的同种异体造血干细胞移植。

复发或难治性血液癌患者的治疗选择有限,预后差,5年总生存率低于20%。尽管同种异体造血干细胞移植(HSCT)是治疗侵袭性血液病的关键策略,但其应用受到移植物抗宿主病(GVHD)、调节相关毒性作用和长期抗GVHD治疗后严重免疫抑制等并发症的阻碍。此外,有严重生理问题或健康状况不佳的患者通常不适合进行同种异体造血干细胞移植,而那些没有先决条件完全缓解状态的患者只能接受补救性同种异体造血干细胞移植,这与复发发生率增加有关需要额外的治疗方案。
嵌合抗原受体(CAR) T细胞疗法在治疗血液病方面取得了令人兴奋的突破,已经证明了针对CD7阳性癌症的异基因CD7 CAR-T细胞的临床安全性和有效性,包括T细胞急性淋巴细胞白血病(ALL)、T细胞淋巴细胞淋巴瘤和一些CD7表达的急性髓性白血病(AMLs)。在多个临床研究中,异体造血干细胞移植被评价为CAR-T细胞治疗后的巩固治疗,以维持长期肿瘤消除并降低复发风险。然而,这种“桥接”方法包括HSCT前调节化疗和GVHD预防药物,这些药物会消除残留的CAR-T细胞,并带来严重毒性作用的风险,因此可能会影响治疗结果。
研究人员希望通过开发一种新的“all-in-one”策略来解决这些挑战,即序贯CD7 CAR-T细胞治疗和单倍体同种HSCT治疗,而不需要药理学骨髓消融或GVHD预防。该研究表明,序贯同种异体CD7 CAR-T细胞治疗和单倍体造血干细胞移植,无需药物条件或GVHD预防,可以成功地在复发或难治性CD7阳性癌症患者的具有挑战性的队列中进行。截至数据截止日期,10名患者中有6名(60%)保持MRD阴性完全缓解。这种创新的方法利用了同种异体CD7 CAR-T细胞疗法(包括CAR-T细胞输注前的淋巴细胞清除),为同种异体造血干细胞移植的成功、GVHD的控制和CAR-T细胞的持续存在创造了特定的条件,从而为同种异体造血干细胞移植开辟了新的战略途径。
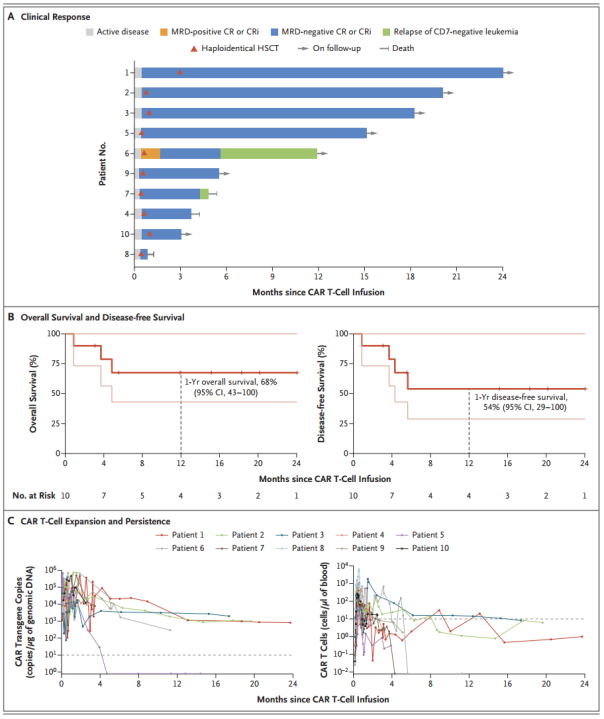
CD7 CAR-T细胞的临床反应、长期生存结果和体内扩增和持久性(图源自 New England Journal of Medicine )
该研究的患者队列主要由老年人(中位年龄56.5岁)组成,入组时基础医疗条件相对较差,长期疗效和安全性与接受常规HSCT的年轻人相似。此外,6例患者既往接触过依托泊苷,这表明依托泊苷作为淋巴消耗剂可能对肿瘤细胞只有轻微的直接影响。总之,该研究为这些以前被认为不适合异体造血干细胞移植的患者提供了一种可行的方法。
该研究的一个关键特征是通过利用CAR-T细胞移植所需的淋巴消耗方案的影响,避免了HSCT前的药理学骨髓消融。这种方法允许在HSCT后CAR-T细胞的长期持续存在,在所有持续完全缓解的患者中,CD7+细胞的根除和可检测的CAR-T细胞的持续存在证明了这一点。9名可评估的患者中有8名在HSCT后有完全的供体嵌合,这表明即使没有药物骨髓消融,CD7 CAR-T细胞治疗可以创造一个有利于同种异体HSPC植入和功能的环境。
这些现象可能是CD7 CAR-T细胞治疗后特别严重的全细胞减少和骨髓发育不全的结果,这可能是由于供体来源的CAR-T细胞的同种异体活性,淋巴细胞消耗相对于自体CAR-T细胞治疗更强,以及细胞因子释放综合征相关的细胞因子也有助于细胞减少。总的来说,该综合策略最大限度地发挥了持续CAR-T细胞和移植物抗白血病潜力的抗白血病功效,为不符合常规同种异体造血干细胞移植条件的复发或难治性CD7阳性癌症患者提供了一种可行的方法。
原文链接:
https://www.nejm.org/doi/full/10.1056/NEJMoa2313812
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言















对复发或难治性CD7阳性#白血病#或#淋巴瘤#患者,序贯#CD7# #CAR-T细胞治疗#和单倍体同种HSCT治疗,而不需要药理学骨髓消融或GVHD预防,这篇研究可以入选2024年#十大#,也是我国#血液病学#领域的重大研究成果。为后续其它类型的白血病的治疗提供新的思路。
38
#白血病# #CAR-T#
36