突破!乳腺癌疫苗GP2研究发现对HER2阳性乳腺癌术后,5年无一复发!
2020-12-12 MedSci原创 MedSci原创
HER2+乳腺癌的标准治疗方案是曲妥珠单抗和帕妥珠单抗。当然,全球治疗HER2+乳腺癌的药物至少获批了9款,除曲妥珠单抗和帕妥珠单抗外,拉帕替尼,T-DM1,奈拉替尼,吡咯替尼,DS-8201,图卡替
HER2+乳腺癌的标准治疗方案是曲妥珠单抗和帕妥珠单抗。当然,全球治疗HER2+乳腺癌的药物至少获批了9款,除曲妥珠单抗和帕妥珠单抗外,拉帕替尼,T-DM1,奈拉替尼,吡咯替尼,DS-8201,图卡替尼,还有今年6月份获批的Phesgo(帕妥珠单抗/曲妥珠单抗/hyaluronidasezzxf)等。这些药物,给HER2乳腺癌患者带来了明确的治疗效果和更多的治疗选择。
即便如此,现有的治疗选择下,仍有八分之一的女性受复发性乳腺癌的影响,约50%的复发性乳腺癌女性对曲妥珠单抗等药物无反应,导致转移性乳腺癌和预后不良,有80~85%的转移性乳腺癌患者无法生存。
2020年11月9日,在著名的圣安东尼奥乳腺癌大会上,一个研究结果让全球震惊!一种被称为GP2的肿瘤疫苗,让乳腺癌患者5年复发率为零,堪称临床治愈!
这来自于一个IIb期临床试验,它是一项前瞻性,随机,安慰剂对照,单盲,多中心临床研究。
研究设计:在16个临床点,纳入了168例患者,随机分为接受GP2+GM-CSF和单独使用 GM-CSF两组。其中,有96例HER2 3+ 的患者,手术后接受曲妥珠单抗治疗联合GP2+GM-CSF或者单独GM-CSF。
研究结果:在5年的随访后,46例接受GP2+GM-CSF治疗的HER2+乳腺癌患者,其5年DFS发生率为100%,而接受GM-CSF治疗的50例安慰剂患者的5年DFS为89.4%。从下面生存曲线的图来看,通俗的说法,治疗组从起始治疗,到治疗5年后,所有病人无一复发!因此,看到的是一条直线。也就是说,GP2组的HER2+乳腺癌患者很有可能就这样被“治愈”了,相信随着随访时间延长,效果可能还会持续更久。
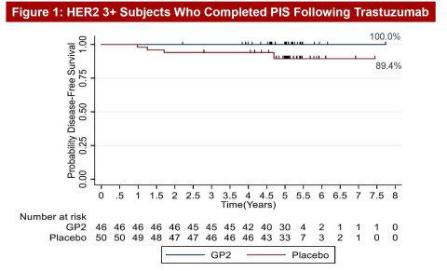
安全性:安全性方面,GP2没有SAEs(严重不良事件),表现出良好的耐受性。GP2通过了局部皮肤试验和免疫试验,获得了强有力的免疫应答,这表明在PIS完成后6个月达到了免疫峰值。
这样的结果表明,HER2+乳腺癌患者在接受了手术和曲妥珠单抗治疗后,再接受GP2+GM-CSF治疗将率先给患者带来被“治愈”的机会。GP2+GM-CSF和曲妥珠单抗之间可能存在一种协同作用。
事实上,在今年4月份发表的一项研究结果,发现AE37和GP2两种疫苗对HER2阳性的乳腺癌患者治疗中,未发现明确的获益。文章发表在Breast Cancer Res Treat上。
AE37和GP2是HER2衍生的肽疫苗。 AE37主要引发CD4应答,而GP2引发针对HER2抗原的CD8应答。这些肽在一项大型随机试验中进行了测试,以评估其在表达HER2的乳腺癌患者中预防复发的能力。初步分析发现5年总无病生存期(DFS)没有差异,但亚组可能获益。
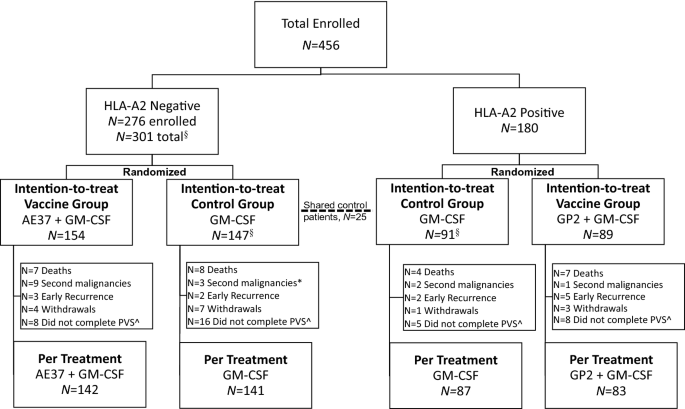
方法 :在这项4臂,前瞻性,随机,单盲,多中心II期临床试验中,无阳性淋巴结和高风险淋巴结阴性的乳腺癌患者均接受标准治疗。疫苗(VG)相对于对照(CG)每月接种六次,作为主要疫苗系列,每6个月间隔接种4次。人口统计学,安全性,免疫学和DFS数据进行了评估。
结果 :456位患者入选; AE37在VG中为154例患者,在CG中为147,GP2在VG中为89例,在CG中为91。与CG相比,AE37组的DFS没有差异,但预先进行的探索性亚组分析显示,晚期阶段有获益的趋势(p = 0.132,HR 0.573 CI 0.275-1.193),HER2表达不足(p = 0.181, HR 0.756 CI 0.499-1.145)和三阴性乳腺癌(p = 0.266,HR 0.443 CI 0.114-1.717)。与CG相比,HER2表达不足和晚期的患者VG显著获益(p = 0.039,HR 0.375 CI 0.142-0.988)。与CG相比,GP2组的DFS没有显着差异,但在亚组分析中,HER2阳性患者无复发,与CG相比,VG的DFS有改善的趋势(p = 0.052)。
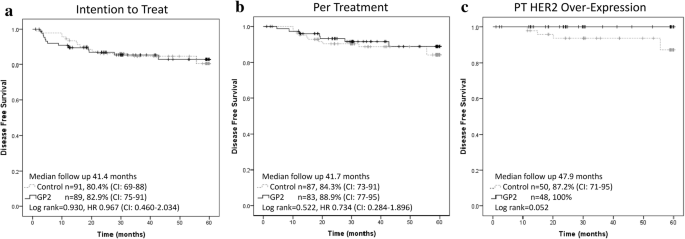
事实上,接受GP2疫苗的HER2过表达患者与对照组相比,有5年估计DFS有明显改善的趋势(100%vs 87.2%,p = 0.052,图3c)。结论与本研究是一致的,即HER2阳性的患者,5年DFS也同样为100%,对照组也是相似的。虽然,在统计学方面,未获得显著性差异,且属于亚组分析的结果。
GP2 final 5-year estimated disease-free survival a Intention to Treat b Per-treatment c Per-treatment subset of HER2 Over-expressing breast cancers
结论 :这项II期临床试验表明,AE37和GP2是安全的,并且可能与某些乳腺癌患者亚组DFS的临床结果改善相关。有了这些发现,就可以根据乳腺癌患者疾病的生物学特性,对组合和/或单独给予的AE37和GP2疫苗进行进一步评估。
但是,williamhill asia 医学认为,二项研究也有不同。本次研究在使用方法上有优化,采用了GP2+GM-CSF,二者可能具有协同作用,从而产生更佳的效果。表明疫苗不是万能的,但是需要恰当地联合治疗。同样,研究设计也十分重要,最新发表的研究仅仅针对HER2+的乳腺癌,这是关键。
有关癌症疫苗
癌症疫苗,是通过利用肿瘤细胞相关抗原,来唤醒人体针对癌症的免疫系统。美国食品及药品管理局(FDA)一个顾问委员会全票通过了允许默沙东公司(Merck)宫颈癌疫苗上市的建议,这意味着人类抗癌战争即将进入一个划时代的新阶段。除了HPV外,还有不少疫苗进入临床,有的虽然鉴于各国巨额的临床试验费用没有获得类似FDA的批准,但依靠患者的口碑相传已经存在市场上长达数年,例如日本的莲见疫苗(Hasumi Vaccine)。
但是,人们最希望看到不仅仅是预防性癌症疫苗,事实上宫颈癌疫苗确切地说是HPV疫苗,预防了这种病毒感染,从而减少了宫颈癌发生。但是,一旦HPV已经感染,或宫颈癌已经发生,这样的疫苗仍然是无效的。
那么,有没有“治疗性疫苗”呢,即已有患有癌症,仍然可以使用疫苗治疗呢?在前20年一直在探索,但是见效甚微。有一些初步的研究成果出现。美国哈佛大学的生物研究所等机构共同研发了一项疫苗。这次的新型抗癌疫苗主要是针对三阴性乳腺癌。在动物研究中发现,注射的小鼠中,100%都能够存活。并且并没有出现复发和转移。通过在肿瘤部位直接注射疫苗,发现此种疫苗能够激活人体内的免疫系统,导致癌细胞死亡。
另外,一种PD-1疫苗PD1-Vaxx,能够同时激活B细胞和T细胞功能,以促进肿瘤清除。其次,该治疗的目标是阻断对于肿瘤生长和维持至关重要的信号通路。11月初,美国食品药品监督管理局批准了PD1-Vaxx进入美国第一阶段人体试验,该试验将集中于非小细胞肺癌患者。今年早些时候,澳大利亚当局也批准在那里开始第一阶段的试验。
乳腺癌疫苗
乳腺癌疫苗的实现需要具备两个条件:一是要有合适、高效的抗原呈递系统;二是要有足够特异和高效的抗原。抗原呈递目前主要通过树突状细胞、全肿瘤细胞、多肽相关抗原和病毒质粒等四种方式进行。
1.树突状细胞疫苗:树突状细胞是目前已知的最具潜力的抗原呈递细胞,它广泛存在于外周组织中,成熟的树突细胞能够将抗原分解为若干多肽片断, 并将多肽片段呈递给原始T细胞,产生CD4辅助T细胞和CD8T细胞介导的细胞免疫;同时树突状细胞还可以诱导体液免疫,激活NK细胞和NK.T细胞。树 突状细胞疫苗的构建首先需要从患者身体取得树突状细胞,在体外培养成熟并将其暴露于肿瘤抗原进行识别,而后将识别肿瘤抗原后的树突细胞注入患者体内,激活 免疫系统。目前在研树突状细胞疫苗有Her-2多位点自身免疫疫苗及P53疫苗,其I期临床试验均已经结束,已进入Ⅱ期临床试验阶段。Her-2多位点自 身免疫疫苗是使树突状细胞识别Her-2多肽E75和E90片段抗原后制成疫苗,对紫杉醇、赫赛汀治疗进展的Her-2过表达转移性乳腺癌进行疫苗、诺维 本、赫赛汀的综合治疗,与无疫苗组进行对比;另一个试验使树突状细胞识别P53野生型基因的多肽片段抗原后制成疫苗,对P53阳性、HLA-A2 、一线内分泌治疗进展的转移性乳腺癌,进行疫苗、依西美坦的综合治疗,与无疫苗组对比,杀伤含有突变P53基因的HLA-A2 的肿瘤细胞。需要指出的是,树突细胞在体外经过识别抗原后,应用于癌症患者的免疫原性已经被证实;但树突细胞疫苗对生产条件要求较高,且目前关于其治疗转 移性实体癌的实验效果不一。
2.多肽疫苗:多肽疫苗的构建相对简单,肿瘤相关抗原的多肽片段易于大量生产和纯化,它们通过与抗原呈递细胞(APC细胞)或T细胞结合来发挥 其免疫原性,诱导细胞免疫和体液免疫。人们通过增加氨基酸增大其分子量,或者免疫佐剂同时应用来提高其免疫原性。粒细胞-巨噬细胞克隆刺激因子(GM- CSF)可促进抗原呈递并增强疫苗诱导的T细胞效应,因此可以加强疫苗的疗效。目前的疫苗试验多集中在Her-2相关多肽疫苗方面 ,一项Ⅱ期研究以Her-2相关抗原多肽GP2和AE37作为疫苗,应用于经标准治疗后未复发的高危患者,对比疫苗、GM.CSF组和单独GM-CSF组 的疗效。另一项Ⅱ期研究为针对ⅢB/1IIC无转移或Ⅳ期仅有稳定骨转移的Her-2阳性患者的Her-2细胞内段抗原(intracelhlar domain,ICD)的多肽疫苗。Disis等证实在该研究的I期研究中,11例患者全部产生了针对接种多肽疫苗的T细胞反应,且其中7例产生了接种多 肽疫苗以外Her-2位点的T细胞反应。经过5年的观察,证实了免疫持续存在。同时Disis也证明了此疫苗与赫赛汀同时应用的安全性。
3.全肿瘤细胞疫苗:自身全肿瘤细胞疫苗3.全肿瘤细胞疫苗:自身全肿瘤细胞疫苗是最早的疫苗制备途径,它拥有肿瘤的全部抗原,理论上可以产生 多克隆的免疫反应,且对肿瘤患者个体具有针对性。全肿瘤细胞通过患者自体肿瘤细胞分离或者由已知同种异体细胞系来获得,自体全肿瘤细胞具有针对单个患者的 特异性,同种异体细胞则针对乳腺癌细胞的共表达部分 .目前有一项Ⅱ期临床试验是针对Her-2阳性的腋下淋巴结或晚期乳腺癌,使用赫赛汀、环磷酰胺、GM.CSF分泌型全细胞疫苗组合,与无疫苗组对比;另 一试验为Her-2阴性晚期乳癌,使用赫赛汀、环磷酰胺、GM.CSF分泌型全细胞疫苗组合,与无赫赛汀组对比。虽然全肿瘤细胞能够提供大量的肿瘤细胞表 面的特异性抗原,但大量自体肿瘤细胞的获取、对众多抗原中特定抗原的免疫原性无有效的评估方法是其不足。由于全细胞疫苗表面存在大量正常细胞抗原,可能导 致免疫耐受,并使肿瘤特异抗原的识别效率降低,需要使用免疫佐剂。
4.病毒载体疫苗:通过病毒的基因转导功能和免疫原性,可以制备病毒载体型疫苗。带有特定抗原基因片段的病毒载体疫苗进入人体后,可以感染抗原 呈递细胞(APC细胞)并使其表达病毒载体疫苗中抗原基因编码的肿瘤相关抗原肽段,从而激活CD4辅助T细胞和CD8T细胞,诱导特异的细胞和体液免疫反 应。病毒载体疫苗的使用依赖于基因重组技术的大量应用。
GP2疫苗
GP2疫苗是什么东西?
GP2是一种短肽,属于上面说的多肽疫苗的一种。AE37和GP2是HER2/neu衍生的肽疫苗。 AE37主要引发CD4应答,而GP2引发针对HER2抗原的CD8应答。其中,GP2含有9个氨基酸的跨膜肽,HER2/neu是一种细胞表面受体蛋白,在75%的乳腺癌和其他各种常见癌症中都有表达,尤其是HER2阳性的乳腺癌。GP2与FDA批准的免疫佐剂粒细胞-巨噬细胞集落刺激因子(GM-CSF)联合使用,可刺激抗原提呈细胞的增殖。
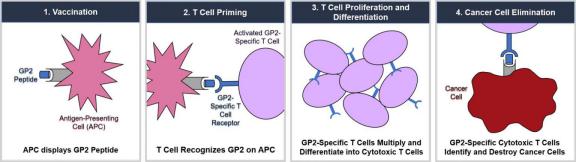
有研究表明,使用GP2治疗后,免疫系统能更好的识别和杀伤表达HER2/neu的癌症细胞,避免了患者的复发。
事实上,从2007年开始,美国就开始研究GP2疫苗了。在2007年一项MD安德森的临床试验目标是找出GP2或AE37作为疫苗联合GM-CSF或GM-CSF单独使用,是否有助于保持淋巴结阳性或高风险淋巴结阴性乳腺癌的复发。
williamhill asia 医学小编进一步检索发现,GP2疫苗已经开展了多项临床试验。
原始出处:
Tommy A. Brown II, et al. Prospective, randomized, single-blinded, multi-center phase II trial of two HER2 peptide vaccines, GP2 and AE37, in breast cancer patients to prevent recurrence.Breast Cancer Res Treat. 2020 Apr 22.
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言










不错
88
有没有最新进展?
79
#研究发现#
74
病人的**
80
居然实现5年的完美曲线,期待公布更多数据!
156
值得学习,解决实际问题
0
#HER2阳性#
88
文末肿瘤疫苗的简单综述不错,肿瘤治疗实体肿瘤的前景越来越光明!
112
这里面缺了一个早期还是晚期呢?具体的类型都没交代,一些细节没说清楚
100
了解
92