【Nat Med】肿瘤微环境影响CAR-T或移植治疗LBCL的疗效
2024-01-21 聊聊血液 聊聊血液 发表于陕西省
学者基于ZUMA-7研究和ZUMA-1研究的队列1+2开展了一项预设的探索性分析,旨在分析治疗前肿瘤特征与axi-cel和SOC疗效之间的关联,以发现可预测axi-cel或SOC疗效的肿瘤特异性特征。
LBCL的肿瘤微环境
在二线大 B 细胞淋巴瘤(LBCL)患者中开展的 III 期 ZUMA-7 研究证明,抗CD19 CAR-T 细胞治疗 (axicabtagene ciloleucel axi-cel]) 优效于标准治疗(SOC;挽救性化疗后进行造血移植)。然而研究证明,仍有相当数量的患者对CAR-T细胞疗法表现出原发性耐药(无应答)或继发性耐药(初始缓解后复发),因此需要对与治疗耐药相关的潜在生物标志物进行进一步研究。
真实世界中接受 CAR-T 细胞疗法治疗的患者的转化数据,进一步强调了肿瘤相关慢性炎症、检查点配体上调、CAR-T细胞功能的骨髓细胞抑制具有较大影响,以及肿瘤基因组复杂性模式与 CAR-T 细胞治疗结局之间具有关联。但CAR-T细胞在干预各线治疗中的预测性生物标志物尚不明确,肿瘤基因表达谱与缓解之间的相关性也尚未得到充分研究,且肿瘤内免疫构成对 CAR-T 细胞治疗的重要性仍不明确。
学者基于ZUMA-7研究和ZUMA-1研究的队列1+2开展了一项预设的探索性分析,旨在分析治疗前肿瘤特征与axi-cel和SOC疗效之间的关联,以发现可预测axi-cel或SOC疗效的肿瘤特异性特征。研究结果近日发表于《Nature Medicine》。

研究结果
B 细胞基因表达签名(GES) 和 CD19 表达与 axi-cel 的无事件生存率改善显著相关(B细胞 GES 的P=0.0002;CD19表达的P=0.0165),但与 SOC 无关(B细胞 GES 的P=0.9374;CD19表达的P=0.5526)。且无论 B 细胞 GES 和 CD19 表达如何,Axi-cel的无事件生存期均优于 SOC(B细胞高 GES的P=8.56 ×10-9;B细胞低 GES的P=0.0019;CD19基因高表达的P=3.85 ×10-9;CD19基因低表达的P=0.0017)。
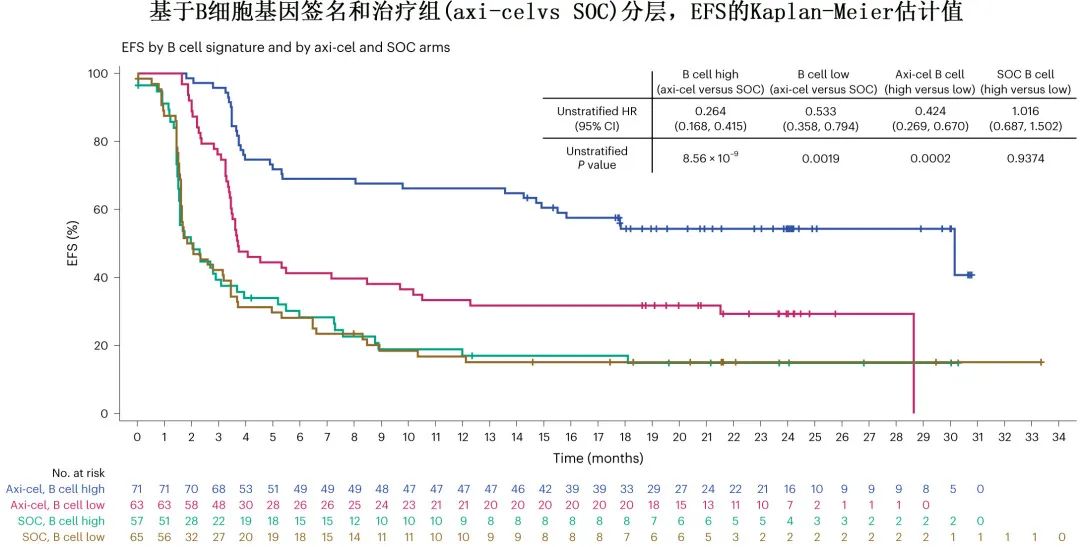
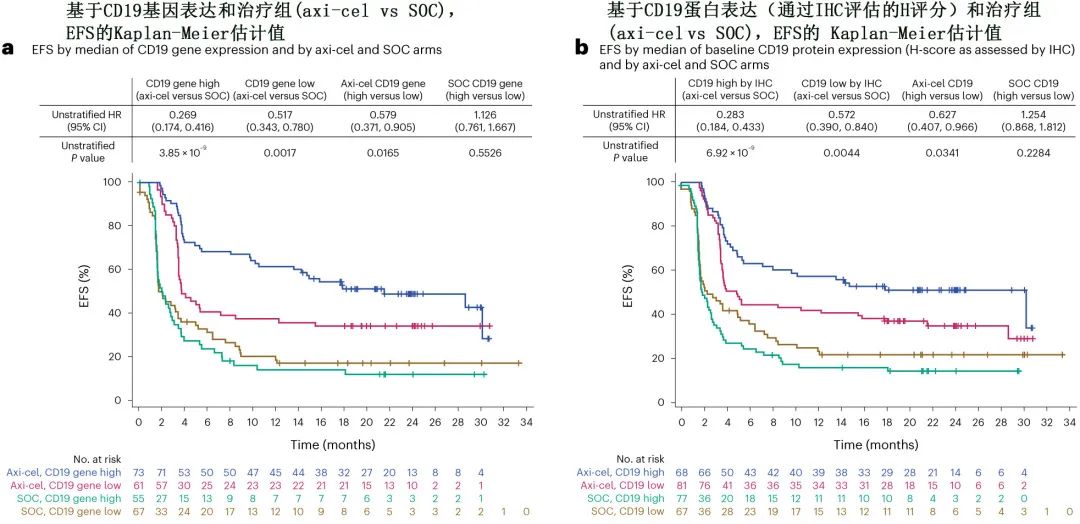
SII(stromal and immunosuppressive index,下图的紫框部分)是个富集基质和免疫抑制特征的cluster,特征基因集包括基质、骨髓细胞和内皮细胞、NOS2、转化生长因子-β(TGFβ)、B7-H3、精氨酸酶 1(ARG1)和缺氧。高SII与 CAR-T细胞治疗结局呈负相关(EFS的P=0.0114,DOR的P=0.0271),但与SOC的结局无关。
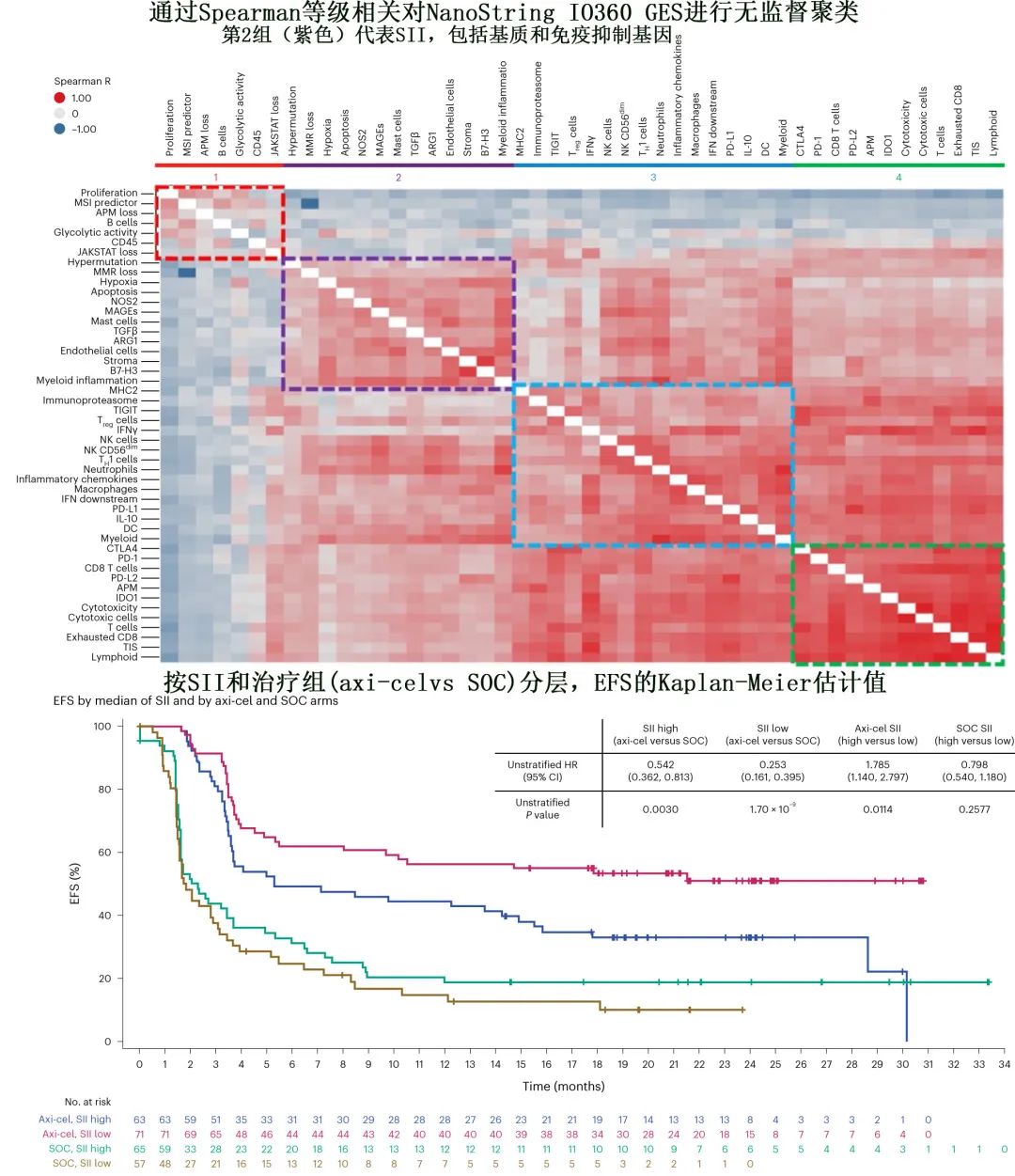
根据产物直径总和 (per sum of product diameters,SPD) 和 LDH 水平评估肿瘤负荷,且SPD 与 LDH 相关 (Spearman R为0.42;P=1.93 ×10-14)。在 axi-cel 组中,结局与 SPD 或 LDH 之间无显著相关性,而 SOC 组结局受到高SPD(>中位值)和 LDH 升高的影响。
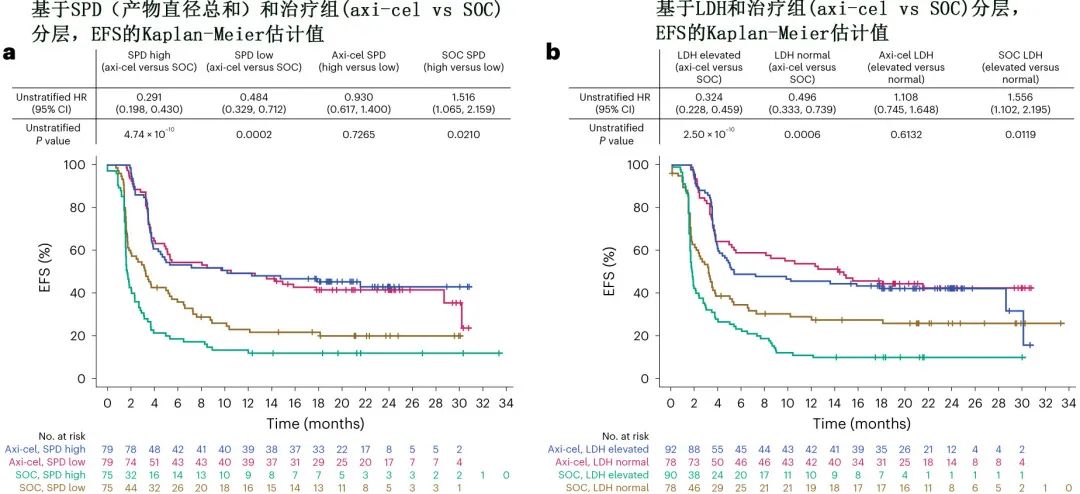
总结
该研究的一个主要发现在于,axi-cel 和 SOC中与结局相关的生物标志物具有明确差异(下图)。
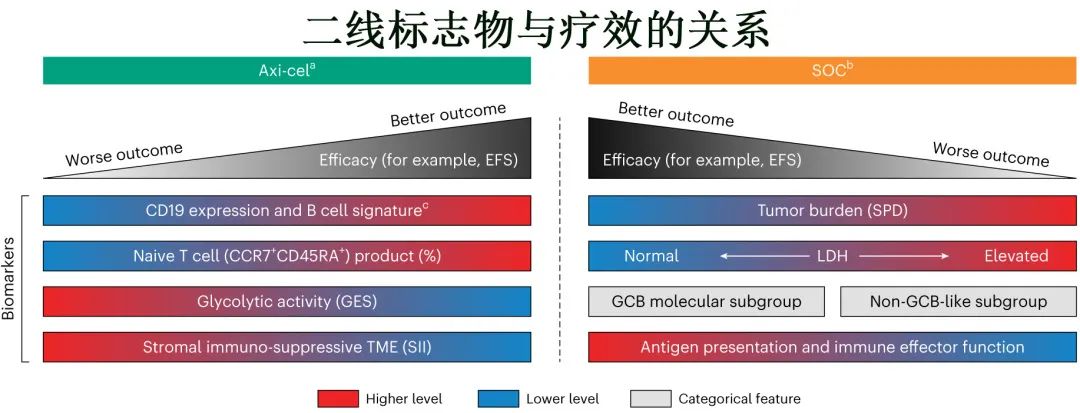
虽然 B 细胞 GES 和 CD19 H 评分与 axi-cel 治疗后的结果呈正相关,但其他 TME 免疫特征(包括 APM 和树突状细胞)与 SOC 后的结局呈正相关,而肿瘤负荷、LDH和细胞起源对 SOC 的影响大于axi-cel结局;这进一步证实axi-cel 与SOC的机制差异:前者为CAR 与 CD19 的直接抗原结合,后者为针对肿瘤表位的内源性免疫(依赖于抗原加工和提呈机制)。值得注意的是,对于所有的生物标志物亚组,axi-cel的结局均优于SOC。CD19 在恶性肿瘤细胞中的低表达与由免疫抑制性基质和髓系基因组成的肿瘤基因表达签名相关,突出了恶性肿瘤细胞特征和显著影响 axi-cel 结果的免疫微环境之间的相互关系。该研究强调了 axi-cel 和 SOC 耐药机制的差异,并支持早期使用 axi-cel 进行干预。
参考文献
Locke FL, et al. Impact of tumor microenvironment on efficacy of anti-CD19 CAR T cell therapy or chemotherapy and transplant in large B cell lymphoma.Nat Med . 2024 Jan 17. doi: 10.1038/s41591-023-02754-1.
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言












好文章,谢谢分享。
37
#肿瘤微环境# #大B细胞淋巴瘤# #CAR-T#
59