ASH 2022:君实生物BTLA单抗tifcemalimab治疗复发/难治性淋巴瘤I期研究结果公布
2022-12-13 君实生物 君实生物 发表于上海
在今年的ASH年会上,君实生物更新了其首个潜在“全球新”(first-in-class)分子BTLA单抗tifcemalimab治疗复发/难治性淋巴瘤的I期研究结果,观察到&l
在今年的ASH年会上,君实生物更新了其首个潜在“全球新”(first-in-class)分子BTLA单抗tifcemalimab治疗复发/难治性淋巴瘤的I期研究结果,观察到“BTLA+PD-1”双免疫疗法的联用疗效前景,特别是对于PD-1抑制剂治疗耐药人群,彰显了中国自主创新的实力。
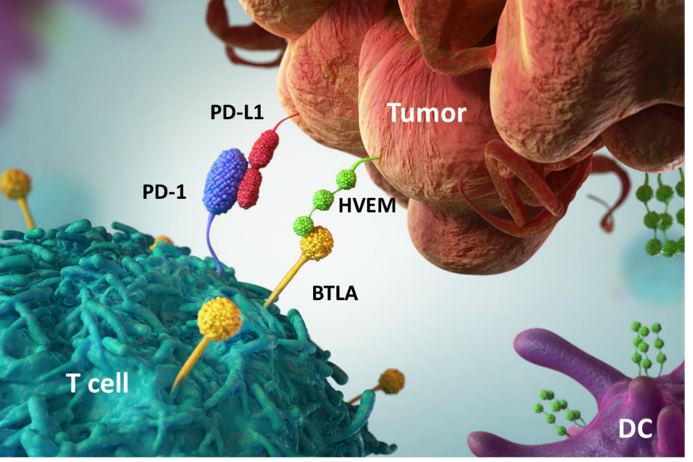
tifcemalimab所针对的BTLA靶点,是2003年发现的表达于活化T、B淋巴细胞的一个重要的免疫检查点分子。肺癌、黑色素瘤、结肠直肠癌和淋巴瘤等肿瘤细胞通过高表达HVEM(BTLA配体),与肿瘤特异的杀伤性淋巴细胞表达的BTLA结合后,可抑制淋巴细胞的免疫功能。
从作用机制上看,BTLA跟PD-1通路有异曲同工之妙。BTLA主要表达于B细胞和T细胞表面,BTLA与肿瘤细胞表面表达HVEM结合后会产生免疫抑制信号,因此阻断BTLA可以解除BTLA/HVEM信号通路对T细胞产生的抑制,逆转免疫细胞的耗竭,进而恢复免疫细胞的活性,抑制肿瘤发展。从机制上看,阻断BTLA/HVEM通路的药效与阻断PD-/PD-L1通路相似。
同时,BTLA靶点抑制剂在解除BTLA/HVEM信号通路的同时,还可能促进HVEM和LIGHT等配体的结合,激活T细胞,发挥不同的免疫调节作用。因此,BTLA还可能具有双重抗肿瘤作用机制。
“BTLA+PD-1”双免疫疗法颇具前景
tifcemalimab(曾用名icatolimab,TAB004/JS004),是君实生物自主研发的全球首个进入临床开发阶段(first-in-human)的抗肿瘤重组人源化抗BTLA(B和T淋巴细胞衰减因子)单克隆抗体,也是君实生物研发管线中备受期待的源创品种之一。
在本届ASH年会上,tifcemalimab以壁报形式更新了其在复发或难治性淋巴瘤患者中进行的I期临床试验初步数据。结果显示,tifcemalimab在所有评估剂量中均具有良好的耐受性,而tifcemalimab联合特瑞普利单抗(抗PD-1单抗)在复发或难治性淋巴瘤患者中的临床活性值得进一步评估,联合剂量扩展部分的试验仍在进行中。
截至2022年10月26日,在联合治疗组的28例可评估患者中,尽管85%患者曾接受抗PD-1抗体治疗后进展,但仍获得39.3%的客观缓解率(ORR)和85.7%的疾病控制率(DCR),且该组中所有缓解患者(CR/PR)中位持续缓解时间(DoR)仍未成熟。
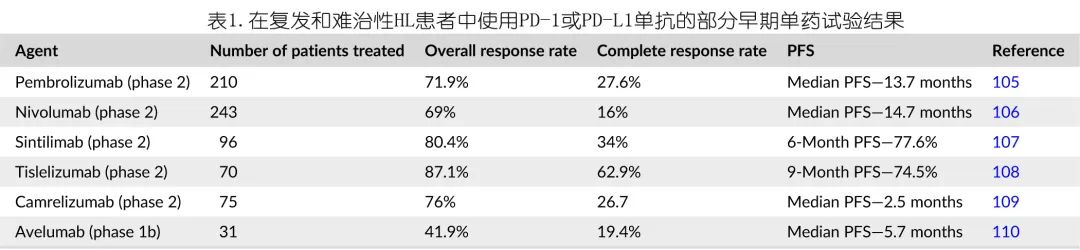
研究者认为,如今PD-1抑制剂已广泛应用在淋巴瘤尤其是复发或难治性经典型霍奇金淋巴瘤(R/R cHL)治疗领域,然而一旦失败便无标准治疗,临床亟需新的治疗手段。通过研究,这类患者在接受tifcemalimab与特瑞普利单抗联合治疗后有望再次获益,并且也观察到这一疗法与其他免疫检查点抑制剂的类似之处,一旦起效可能为患者带来长期生存。
君实生物全球研发总裁邹建军博士表示,"作为一款‘全球新'药物,tifcemalimab在早期临床试验中显示出的安全性和疗效令人期待。特别是此次ASH年会上发表的更新数据,更突显出tifcemalimab与特瑞普利单抗的双免疫疗法治疗对于抗PD-1单抗耐药的复发或难治性淋巴瘤患者颇具前景,值得进一步评估。此外,williamhill asia 在实体瘤患者中也看到了这项联合方案突出的安全性和有效性,期待在后续开展的研究中得到进一步验证。"
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言