Cell Death Dis:Caveolin-1调控酸性鞘磷脂酶/神经酰胺介导的内皮细胞的放疗反应
2020-04-19 QQY MedSci原创
质膜内的组织形式对于其在多个细胞过程中的作用至关重要。 胆固醇作为质膜的主要成分,能够严重影响质膜的组织形式。鞘脂与胆固醇分子之间的相互作用会导致这些脂质的侧向及局部的缔合,最终形成了富含鞘脂及胆固醇
细胞膜穴样内陷(caveolae)是一种非平面的特异性膜微区(囊泡内陷),是脂质筏的一种。
CAV1(整合膜蛋白caveolin-1)为caveolae的主要结构成分,其作为胆固醇的结合蛋白能够稳定脂质筏结构。既往研究发现CAV1在晚期前列腺癌(PCa)中的抗辐射介导的肿瘤-基质相互作用中起着核心作用。在肿瘤基质相互作用中,内皮细胞(EC)是放疗抗性的关键决定因素。目前已有研究证明血管生成性EC中CAV1缺乏会导致受放疗的EC细胞凋亡反应的增加。
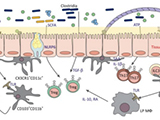
该研究探讨了在EC中CAV1的不同表达水平对酸性鞘磷脂酶(ASMase)/神经酰胺通路的潜在影响;该信号通路是调节放疗及癌细胞放射抗性中EC细胞凋亡反应的关键因素。
CAV1缺乏的EC细胞凋亡敏感性增强与ASMase活性提高、神经酰胺生成、大脂质结构形成以及MAPK/HSP27/AKT信号转导通路改变相关。
在3D共培养中,对CAV1缺乏的EC进行放射性治疗能够增加LNCaP及PC3 PCa细胞的生长延迟。外源性C6及C16神经酰胺治疗可以增加PCa球体的生长延迟并诱导PCa细胞凋亡反应。
对CAV1表达水平升高的PCa细胞中相应的神经酰胺种类进行分析发现,不饱和C24:1神经酰胺水平升高,可能是通过清除诱导EC细胞凋亡反应的C16神经酰胺来实现的。
免疫组织化学实验发现,特异性CAV1肿瘤-基质改变的人晚期前列腺癌标本具有更高的酸性鞘磷脂酶及神经酰胺表达水平。CAV1能够调节神经酰胺依赖性质膜的产生,进而影响EC及相邻PCa细胞的辐射反应。
因此,了解肿瘤细胞与宿主来源的肿瘤微脉管系统之间CAV1依赖性串扰及其对放射敏感性的影响,可能有助于确定靶向CAV1是克服肿瘤放疗抗性的一种合理的治疗策略,从而改善该疾病的临床治疗效果。
原始出处:
Ketteler et al. Caveolin-1 regulates the ASMase/ceramidemediated radiation response of endothelial cells in the context of tumor–stroma interactions. Cell Death and Disease (2020) 11:228
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言









#酸性鞘磷脂酶#
78
#Dis#
49
#CEL#
64
#caveolin-1#
67
#鞘磷脂#
77
#Cell#
61
#神经酰胺#
78
#Death#
67