药捷安康治疗心衰药物PDE9抑制剂TT-00920获批临床试验
2020-11-17 药捷安康 药捷安康
11月16日,中国国家药监局药品审评中心(CDE)公示,南京药捷安康生物科技有限公司的1类新药TT-00920片获得3项临床试验默示许可,拟开发用于心力衰竭。药捷安康公开资料显示,TT-00920是其
11月16日,中国国家药监局药品审评中心(CDE)公示,南京药捷安康生物科技有限公司的1类新药TT-00920片获得3项临床试验默示许可,拟开发用于心力衰竭。药捷安康公开资料显示,TT-00920是其开发的一款创新心衰治疗药物,此前已在美国获批临床。
该药物是药捷安康成立3年以来,第二个自主研发并拥有完全自主知识产权的全球创新药物。公司计划于2020年初在美国启动一期临床试验,评估TT-00920在健康受试者体内的安全性、耐受性和药代动力学特征。
TT-00920是一个高活性、高选择性的磷酸二酯酶9A(PDE9A)抑制剂,用于治疗慢性心衰。PDE9A靶点和心衰存在高度疾病关联性,抑制PDE9A可提高心肌cGMP水平,激活失调的心脏保护机制,保护心肌细胞免受损伤。临床前动物心衰模型中,TT-00920展示出优异的体内疗效,可显著改善心衰动物的左心室功能,逆转心肌细胞病理性重构。

截图来源:CDE官网
药捷安康是一家处于临床阶段的新药研发公司,围绕肿瘤、心血管疾病与代谢疾病领域内的未满足临床需求,以自主研发和合作创新为驱动,打造具有全球突破性的“first-in-class”和“best-in-class”产品。该公司首个临床产品——全新选择性多激酶抑制剂TT-00420已经在中国和美国两地启动全球1期临床试验。
此前,TT-00920已获得美国FDA批准临床,目前正在美国开展临床1期试验,即在健康人群进行人体安全性、药代动力学、以及药效生物标志物的研究。公开资料显示,该研究已于今年3月完成1期临床试验首组健康者给药,预计将于2021年获得数据。
近日,药捷安康还宣布在2020年美国心脏协会年会(AHA)上发表TT-00920的临床前心衰数据。在临床前的慢性心衰模型上,该产品表现出非常良好的药效和对心脏的保护作用,显示TT-00920在心力衰竭患者的治疗中具有较大潜力。
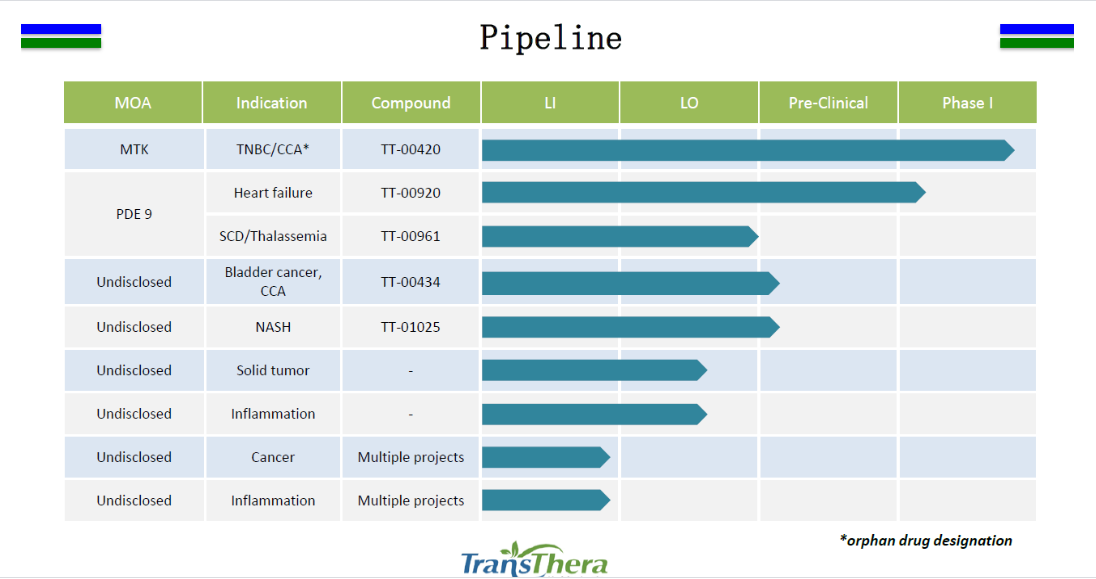
药捷安康研发管线图,来源:药捷安康官网
药捷安康还有6项在研产品未揭盲。从整体数据来看,未来这些产品一旦上市,市场空间非常可观。
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言










#抑制剂#
58
#心衰药物#
70
学习了
150
学习了
140
赞赞赞
106