读书报告 | 靶向CLDN18.2治疗消化道肿瘤
2023-12-20 iCombo iCombo 发表于上海
文章对靶向CLDN18.2的药物在临床研究中的最新进展进行了详细总结。
导读
胃肠道癌症是最常见的恶性肿瘤之一,提高其疗效是改善胃肠道肿瘤患者生存和预后的关键因素。CLDN18.2是一种跨膜蛋白,是紧密连接的主要成分,在维持屏障功能中起重要作用。其在肿瘤组织中广泛表达的特性及其暴露的细胞外环使其成为研究人员开发胃肠道癌症靶向策略和免疫疗法的理想靶点。
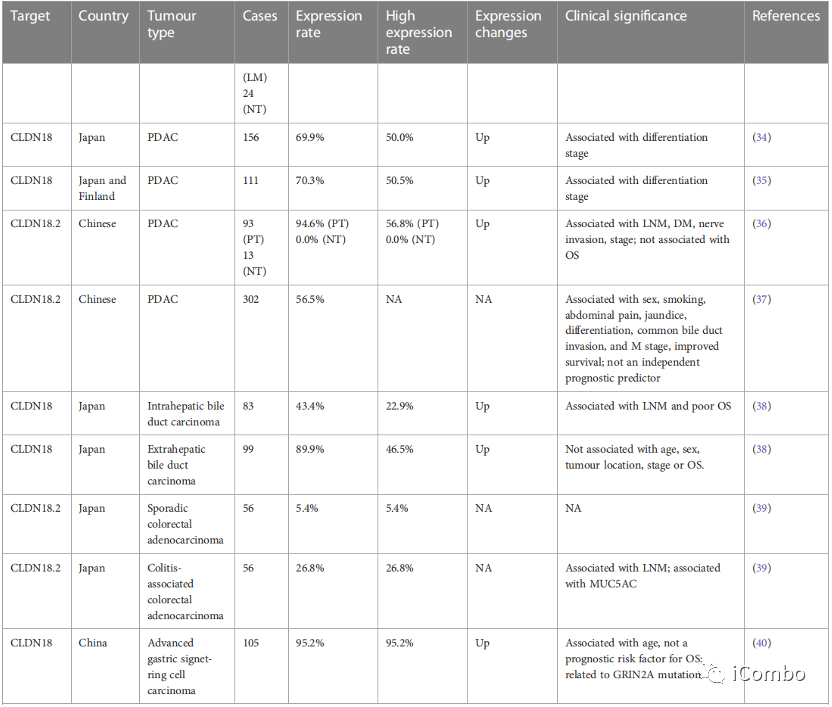
本篇综述阐述了CLDN18.2在胃肠道癌中的表达模式及其临床意义。CLDN18.2蛋白是一种高度选择性的胃谱系标记物,其表达与GC的组织学亚型有关,并且在转移性病灶(淋巴结和肝转移)中的活化程度与原发灶中的活性相当。
本文还讨论了CLDN18.2的促肿瘤和/或抑制肿瘤的功能、其表达的调节机制。CLDN mRNA表达与其启动子CpG岛的甲基化是呈现负相关的,PKC通路、ERK/MAPK通路、HER2/HER3信号通路参与调节CLDN 18.2表达,miRNA也可以通过与CLDN18 mRNA结合调节CLDN18的表达。
最后,文章对靶向CLDN18.2的药物在临床研究中的最新进展进行了详细总结。一些单克隆抗体治疗和CAR-T细胞治疗的临床研究已经披露了临床试验数据。新兴药物类型--ADC和双特异性抗体,近年来已被批准进行临床试验,结果令人期待(Front Oncol.2023 Mar 10;13:1132319. doi: 10.3389 /fonc. 2023.1132319. eCollection 2023)。
CLDN18基本信息
Claudins:至少由27个跨膜蛋白组成的家族,是细胞紧密连接的重要组成部分和功能结构。
Claudin-18的功能:
1. 维持细胞极性和屏障功能
2. 选择通透功能
3. 促进抗酸
Claudin-18基因位点:染色体3q22,分子量约35 kb,含6个外显子和5个内含子。第一个外显子选择性剪接,形成两个不同的剪接突变体(CLDN18.1和CLDN18.2)。
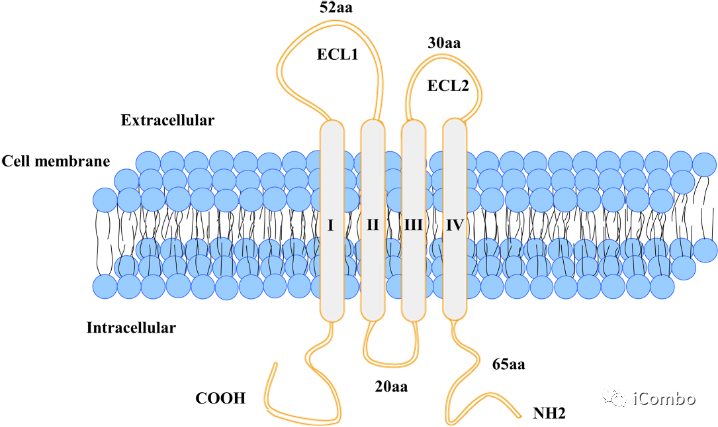
CLDN18蛋白的结构示意图
CLDN18.1在肺肿瘤中的表达模式及临床意义
CLDN18.1在肺泡上皮高表达,参与调节溶质和离子通透性,以及细胞骨架重排。
CLDN18.1基因敲除可增加溶质通透性和肺泡液体清除率,增强上皮钠通道和Na-K-ATP酶活性。
CLDN 18.1在肺癌中的表达明显降低,可能在抑制肿瘤进展中起作用。
当CLDN18.1在失去表达的肺腺癌(LUAD)细胞中恢复时,显著减弱了体内肿瘤的生长以及体外细胞增殖、迁移、侵袭和集落形成,敲除CLDN18.1导致小鼠肺体积增大、祖细胞增殖和肿瘤发生。
CLDN18.2在胃肠道肿瘤中的表达模式及临床意义
CLDN18.2蛋白是一种高度选择性的胃谱系标记物。
除了原位表达外,在胰腺、食管、胆道、卵巢和肺肿瘤中频繁异位激活。
与相应的正常组织相比,在胃癌(GC)和肉瘤(胃间质瘤)组织中发现下调。
在胃恶性转化过程中,CLDN18.2的表达有所下降,但仍保持稳定。
CLDN 18.2在转移性病灶(淋巴结和肝转移)中的活化程度与原发灶中的活性相当。
CLDN18.2的表达与GC的组织学亚型有关。
按Lauren亚型分组的GC中,CLDN18.2在弥漫型GC中的表达显著升高。
按粘蛋白表型分组的GC中,具有肠表型的样本主要表现为CLDN18.2下调,这表明CLDN18的缺失涉及肠表型肿瘤的发病机制,并表明其表达可用作胃表型的标志物。
CLDN18.2表达与临床病理因素的关系:
-
CLDN18.2表达与神经周围浸润呈显著负相关
-
CLDN18.2表达与肿瘤细胞分化的关系有争议
-
在胰腺组织中癌,分析显示淋巴结阳性肿瘤CLDN 18.2的表达明显升高
CLDN18与患者的生存率相关:
-
CLDN18缺失是胃癌患者预后不良的一个独立指标,CLDN18表达的患者OS更长。
-
CLDN18的下调与晚期GC患者的生存率差相关.
-
在胰腺癌(PC)中,CLDN18.2的表达与患者生存期无相关性。
-
在宫颈腺癌中,CLDN18.2为无进展生存(PFS)较差的独立预测因子。
ARHGAP26是一种GTP酶激活蛋白(GAP),其促进RHO GTP酶向GDP状态的转换,并已表明在增强细胞运动. CLDN18-ARHGAP26融合基因是胃癌中最常见的体细胞基因组重排基因之一,特别是在基因组稳定亚型. Ushiku et进行的细胞存活和迁移研究艾尔结果表明,CLDN 18-ARHGAP融合在RhoA基因敲除条件下可补充癌细胞的存活和诱导细胞迁移。RhoA突变存在于弥漫性胃癌(DGC)中,被认为是DGC的驱动基因之一。因此,CLDN 18-ARHGAP融合可能是RhoA突变维持癌细胞存活和促进细胞迁移的一个因素。
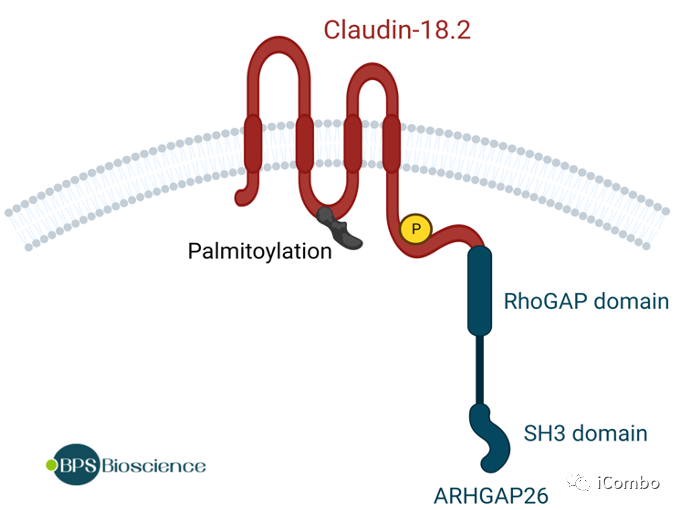
CLDN18-ARHGAP融合是弥漫性胃癌的分子特征之一,也是独立的预后危险因素
研究分析254例胃癌(弥漫型172例,肠型82例)结果发现26例融合阳性病例(26/254,10.24%),其中22例为弥漫型胃癌(22/172,12.79%)。
CLDN18-ARHGAP融合频率在印戒细胞癌中为18.25%,并且CLDN18-ARHGAP 26/6融合与印戒细胞含量、诊断时年龄、男女比例和TNM分期相关。
CLDN18-ARHGAP26/6融合的患者生存率更差,并且这种融合的患者不能从奥沙利铂/氟嘧啶为基础的化疗中获益。
CLDN18-ARHGAP融合蛋白在年轻发病的GC中富集,其存在可能有助于其侵袭性特征:146例40岁以下胃癌患者中,CLDN18-ARHGAP融合率为15.1%。其中18例(12.3%)为CLDN18-ARHGAP26融合体。融合的患者更可能有较大的肿瘤、LNM和晚期,并表现出显著较低的OS。
CLDN18-ARHGAP26融合介导上皮解体,并通过CLDN18的丧失和ARHGAP26功能的获得而有助于GC进展。
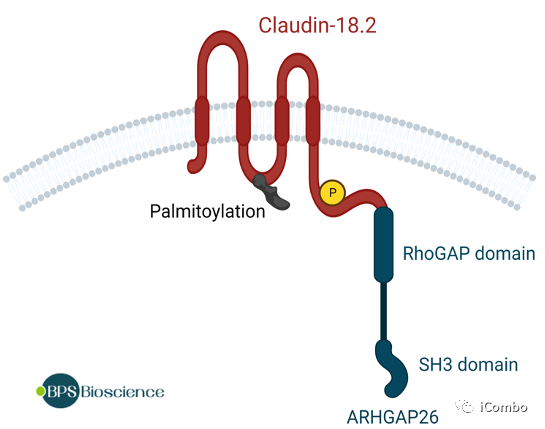
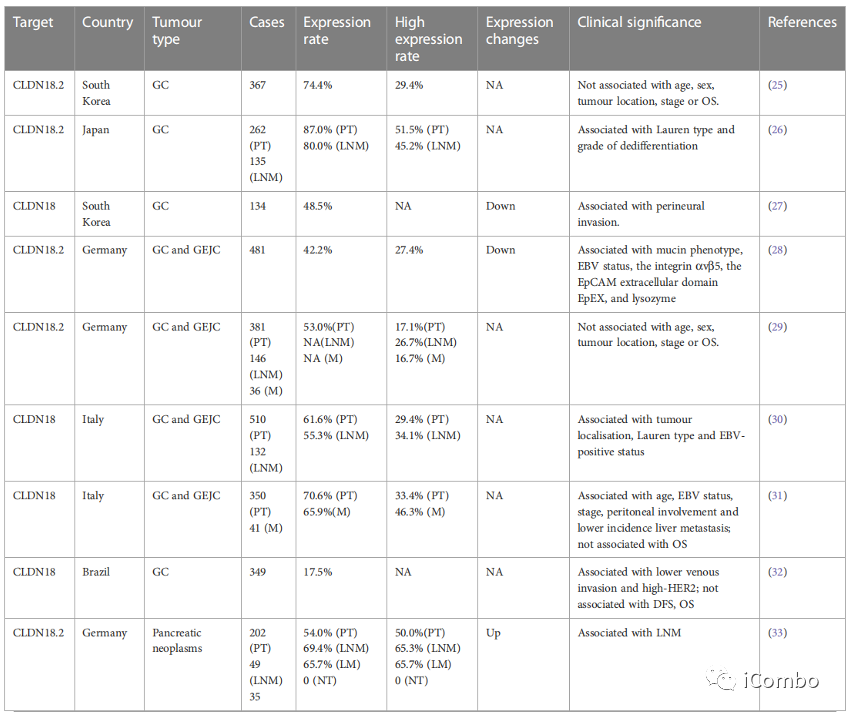
CLDN18.2在消化道肿瘤中的表达模式及临床意义
CLDN18表达的调控--CpG岛的甲基化作用
CLDN mRNA表达与其启动子CpG岛的甲基化呈负相关。
-
体外CLDN18.1启动子的甲基化可以强烈地抑制连接的荧光素酶报告基因的转录,这表明CpG岛的甲基化可能抑制转录因子与CLDN18.1启动子的结合,并减弱CLDN18.1的表达。
-
Claudin-18a1启动子包含两个T/EBP/NKX2.1结合位点,含有同源结构域的转录因子T/EBP/NKX2.1与claudin-18a1启动子结合,促进claudin 18a1表达的反式激活。
-
CpG岛的甲基化可以完全阻止转录因子CREB结合CLDN18.2的启动子区域。
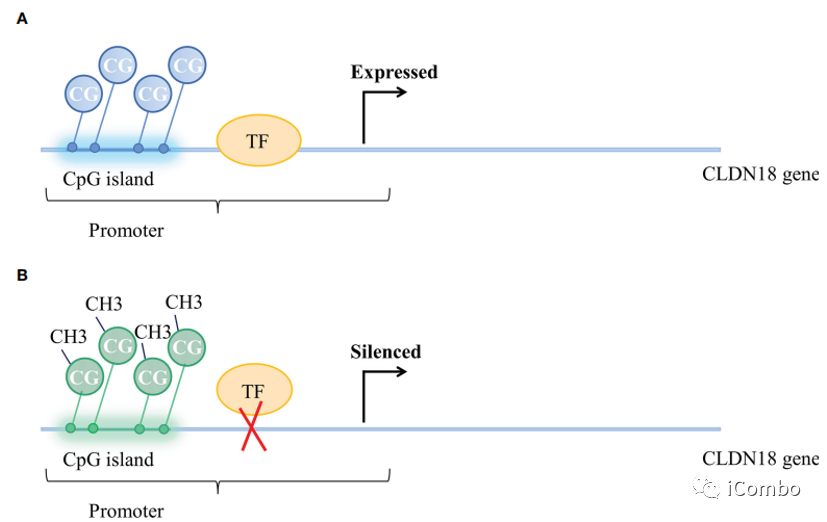
CpG岛的甲基化状态和CLDN18基因的表达。
(A)未甲基化CpG岛,表达CLDN18.2基因。
(B)CpG岛的甲基化阻断了转录因子与CLDN18.2启动子的结合,导致CLDN18.2基因沉默。
CLDN18表达的调控--PKC通路和ERK/MAPK通路
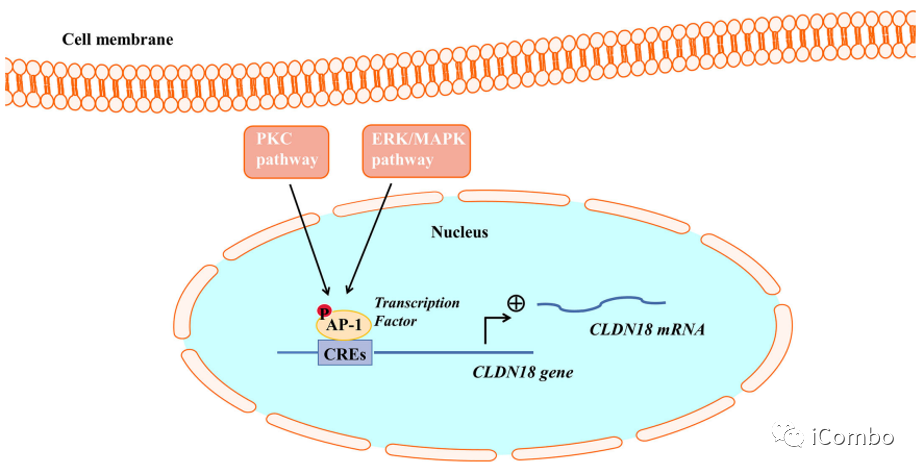
图3 PKC通路和ERK/MAPK通路调控CLDN18.2的表达。AP-1可以与CLDN18.2启动子的顺式调控元件(CREs)结合,提高CLDN18.2的转录活性。PKC和ERK-MAPK通路通过刺激AP-1的磷酸化和激活来增强CLDN18.2 mRNA的转录。
CLDN18表达的调控--HER 2/HER3信号通路

HER2/HER3信号通路通过调控CLDN18的表达来调控屏障功能,但其机制尚不清楚。
有研究表明,NRG-1-HER 2/3信号通路参与IL-1β介导的肺屏障功能障碍。IL-1β通过激活her 2/her 3相关信号通路而抑制claudin 18的蛋白表达和细胞膜定位,从而导致肺屏障功能异常。
CLDN18表达的调控--microRNAs

MiRNAs可以通过与CLDN18 mRNA 3'-UTR的假定结合位点结合,导致mRNA的降解或抑制翻译,显著减弱CLDN-18的表达。
CLDN18在癌症中的二分性作用
CLDN18在癌症中具有二分性的作用(Dichotomous roles):
-
在不同类型的肿瘤中,它可能作为肿瘤的促进者或抑制者。
-
在胃癌和肺癌中起肿瘤抑制作用
-
在其他消化道癌症如管癌、胰腺癌、结直肠癌和胆管癌中起肿瘤促进作用。
CLDN18的肿瘤抑制作用
-
与周围胃正常粘膜或肠上皮化生相比,GC组织中Claudin-18的表达显著降低。
-
敲低Claudin-18可显著促进细胞增殖和侵袭
-
幽门螺杆菌感染在小鼠胃癌发展的早期减弱了CLDN18的表达。
-
CLDN18的缺失促进了小鼠胃中癌细胞的快速发展
-
CLDN18.1被认为在LUAD中具有肿瘤抑制作用
-
CLDN18反向调节下游转录辅活化因子YAP的核定位和活性,促进正常肺中AT2细胞的增殖。
-
CLDN18.1的表达在LUAD中显著减少,并且老年CL DN 18-/-小鼠发展LUAD的倾向增加。
-
CLDN18.1表达与启动子甲基化和LUAD患者死亡率呈负相关。
-
CLDN 18.1在已失去表达的LUAD细胞中的再表达明显减弱了细胞的恶性特性。
-
CLDN18.1可以抑制IGF-1R/AKT和YAP/TAZ/AKT轴。抑制肺上皮细胞的PDK1/Akt信号通路。
CLDN18的促肿瘤作用
CLDN 18的促癌作用主要表现为肿瘤异位激活。
胰腺癌:胰腺癌的早癌的前体病变(PanIN、IPMN和MCN)均表现出频繁的CLDN18免疫反应,提示CLDN18是PDAC早期癌变过程的标志物。
食管癌:健康食管的紧密连接中CLDN 18缺失,而Barrett食管特殊柱状上皮的紧密连接中富含CLDN 18,这一变化可使鳞状上皮细胞更能耐受管腔酸的攻击和破坏,从而促进肿瘤的发生。
胆管癌:敲除claudin-18的表达或特异性抗体可显著减弱其增殖、侵袭和体内胆管腺癌细胞的肿瘤发生。EGFR通路和活性RAS可以通过激活ERK1/2诱导claudin-18的表达。增强的claudin-18表达随后激活ERK1/2。它们形成一个正反馈回路,促进胆管恶性肿瘤。
以上研究结果初步提示其在CLDN18异位激活的肿瘤中具有促癌作用。然而,由于其作用机制的证据探索尚浅,有待于更全面、更深入的研究。
以CLDN18.2为靶点的药物研究进展
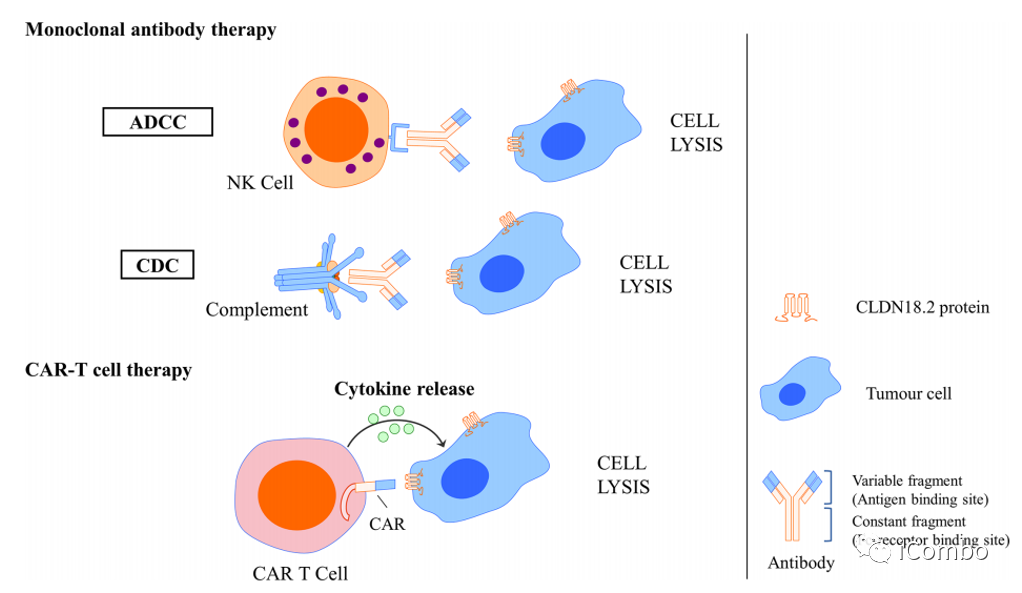
以Claudin18.2为靶点的药物
-
单克隆抗体
-
CAR-T细胞
-
双特异性抗体
-
ADC
结果已公开 的CLDN18.2临床试验:
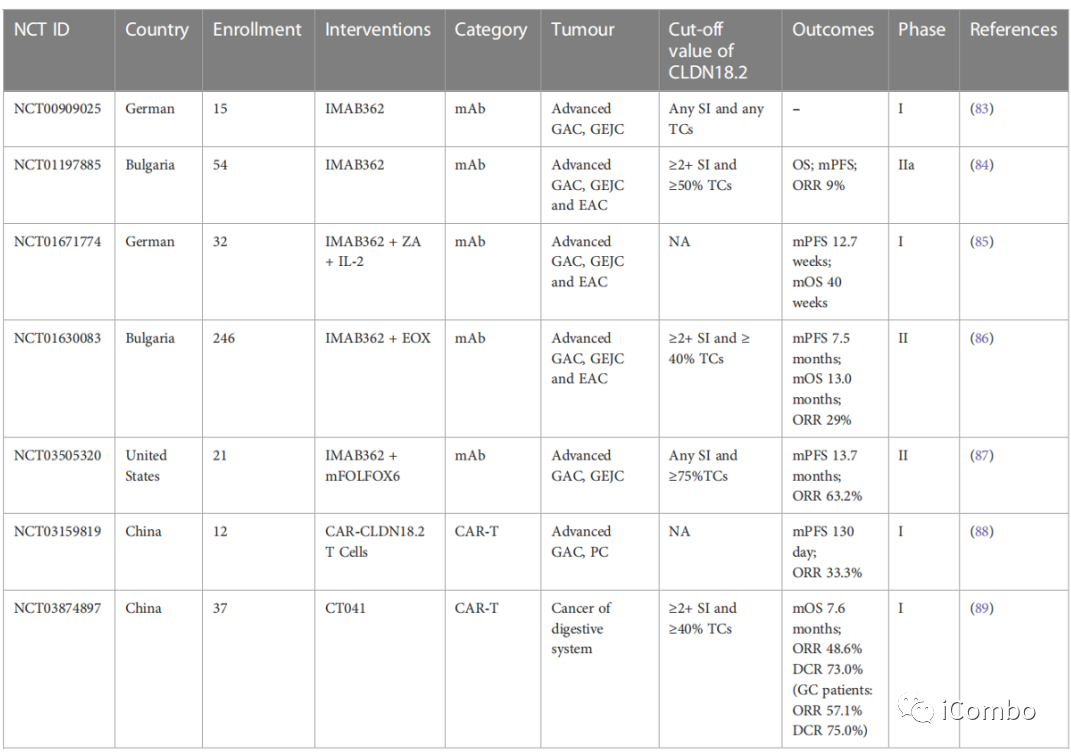
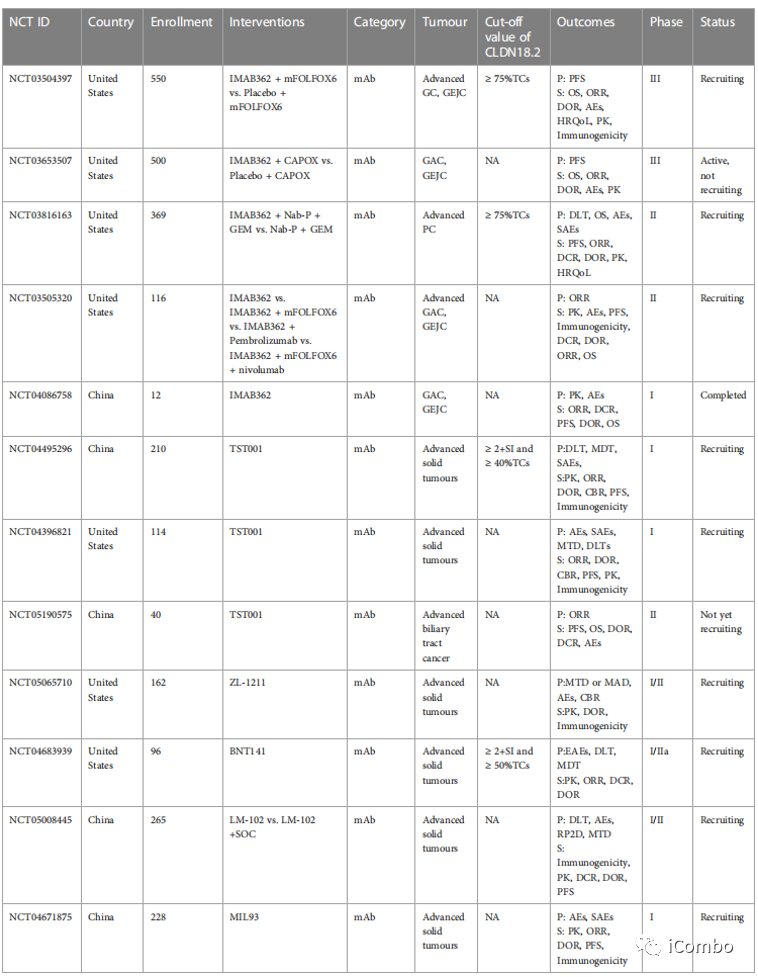
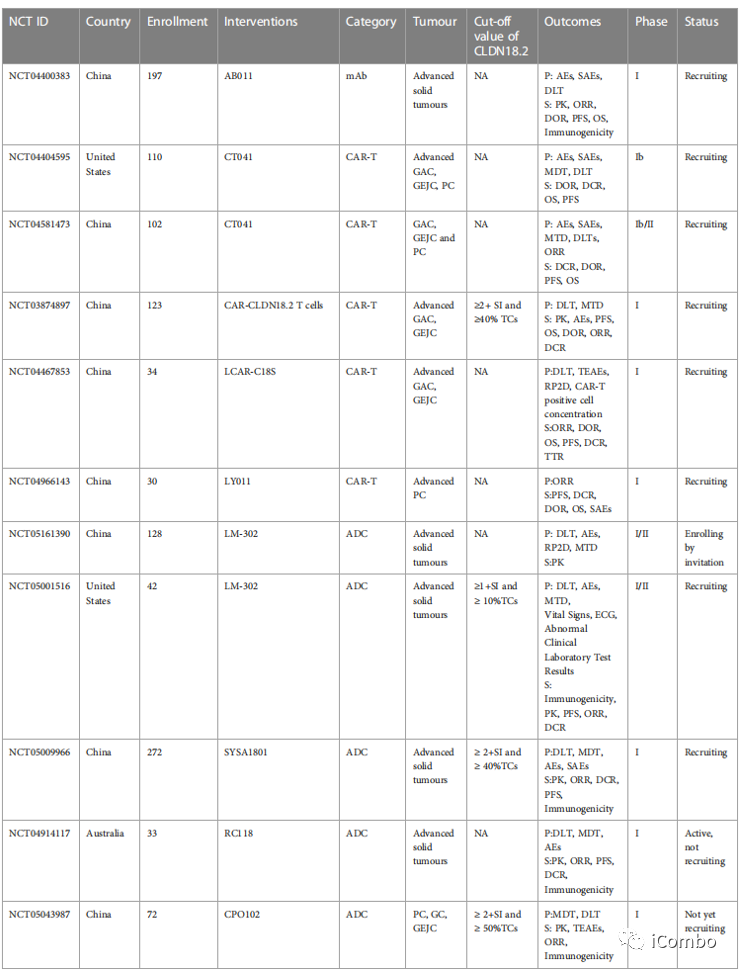
以CLDN18.2为靶点的药物研究进展:单克隆抗体疗法
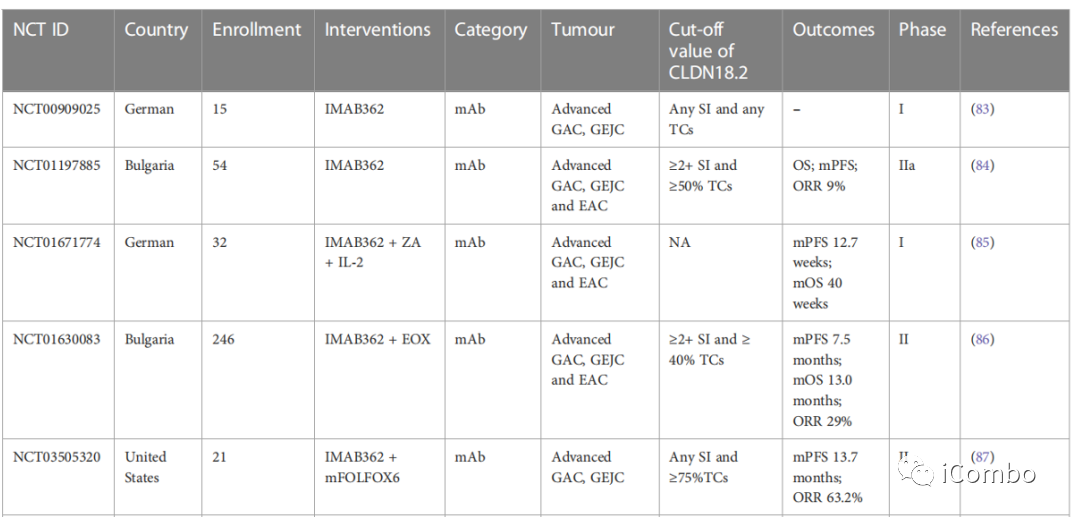
IMAB 362具有良好的耐受性和安全性。
IMAB 362单药以及联合化疗在上述肿瘤患者中是安全的,并且具有抗肿瘤活性。
与单纯化疗相比,联合治疗组患者在更长时间内保持了良好的生活质量和较低的症状负担。
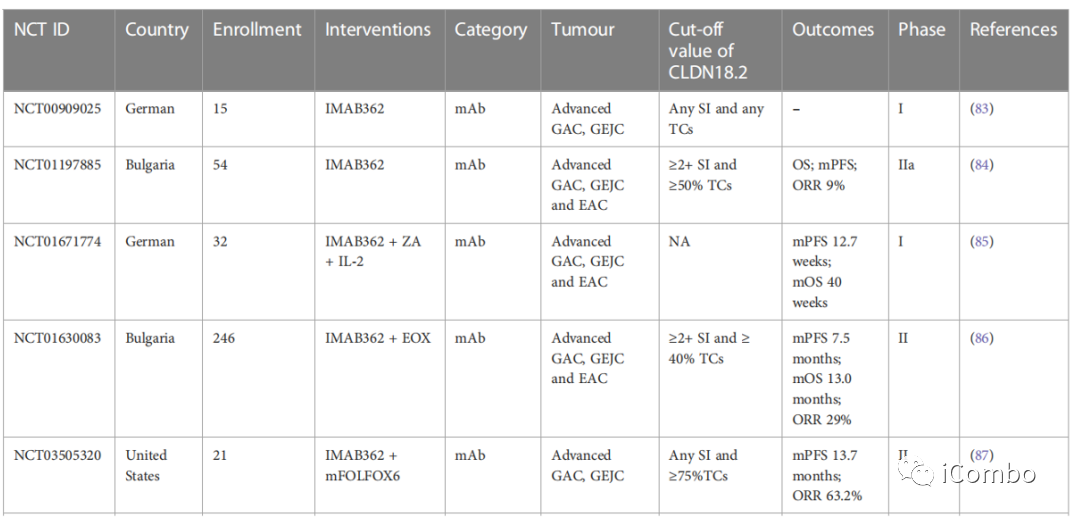
单用IMAB362的总有效率(ORR)和临床获益率(CBR)分别为9%和23%。
IMAB362联合EOX化疗的研究中,ORR为29%,mPFS和mOS分别为7.5m和13.0m。
IMAB362+mFOLFOX6化疗的研究中,ORR为63.2%,mPFS为13.7m。
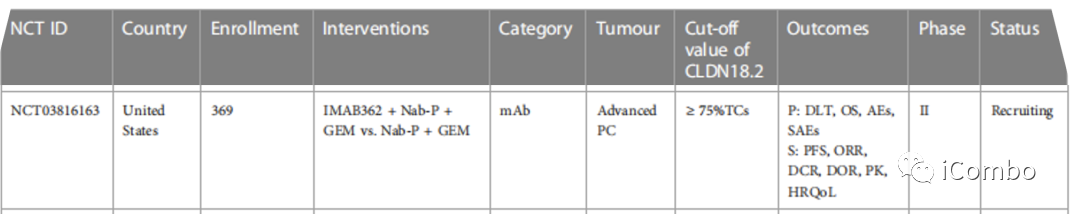
NCT03816163:IMAB362联合Nab紫杉醇和吉西他滨(Nab-P+GEM)一线治疗Claudin 18.2(CLDN18.2)阳性转移性胰腺癌的疗效和安全性评估研究:
一项2期、开放标签、随机研究,2019年起纳入369例claudin 18.2阳性转移性胰腺癌患者,
以CLDN18.2为靶点的药物研究进展:CAR-T细胞治疗
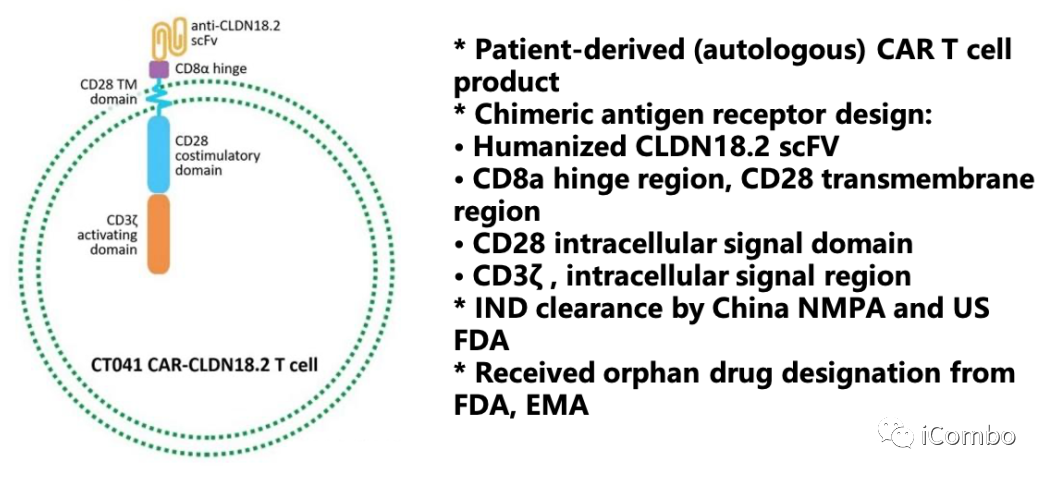
CT041(科济药业)
-
人源化CLDN18.2特异性单链可变片段(scFvs),特异性识别CLDN18.2
-
使用scFv作为靶向成分,产生包含CD28共刺激结构域的CLDN 18.2特异性CAR T细胞

NCT03874897:一项开放、多中心、剂量递增/递减和剂量扩展I期临床研究,研究CT041在消化系统肿瘤患者中的安全性、疗效、药代动力学和免疫原性。
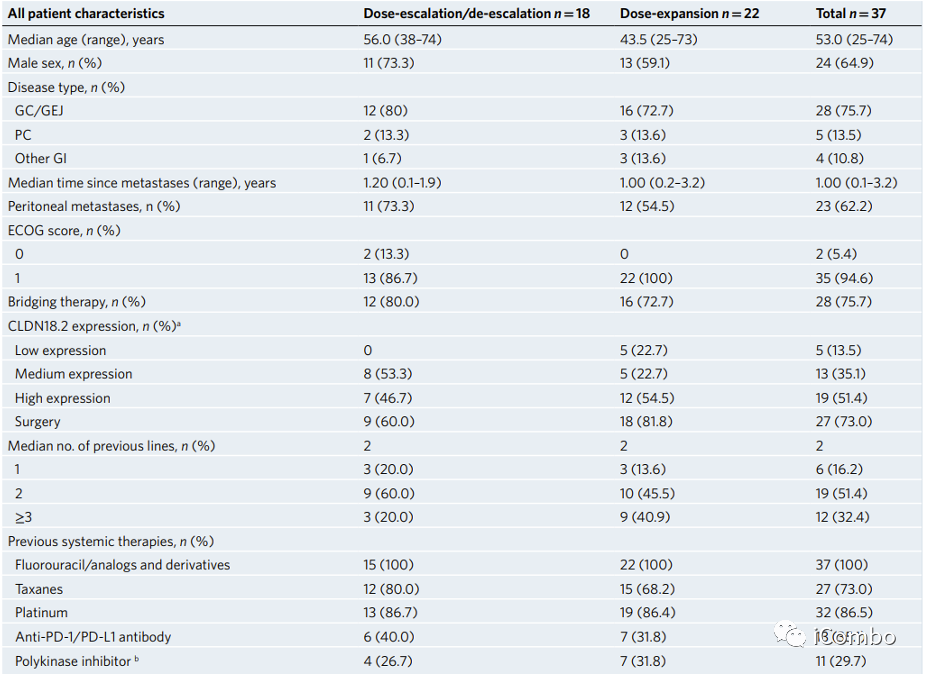
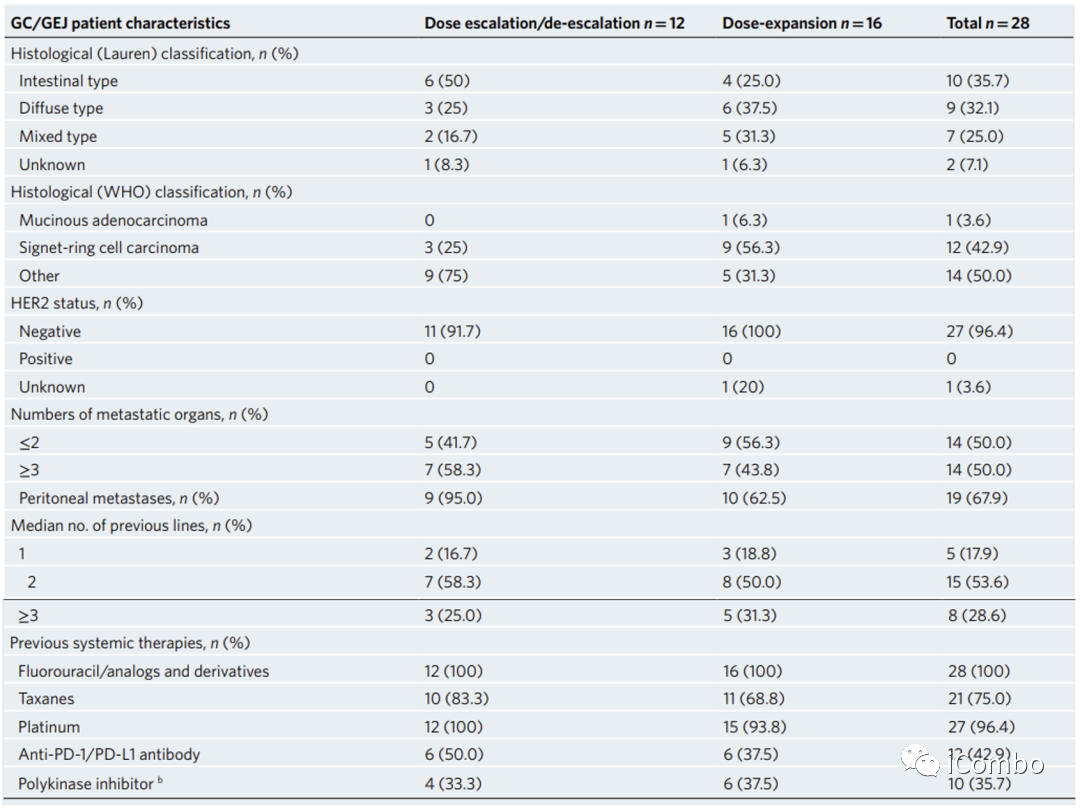

疗效:全部
ORR 48.6%,DCR 73.0%,mPFS 3.7m,6-month OS率 80.1%。
亚组:GC/GEJ,
ORR 57.1%,DCR 75%, mPFS 4.2m,6-month OS率 81.2%。
≥2线 ORR 61.1%,DCR 83.3%,mPFS为5.6m,6个月时的持续缓解率为57.1%。
以CLDN18.2为靶点的药物研究进展:
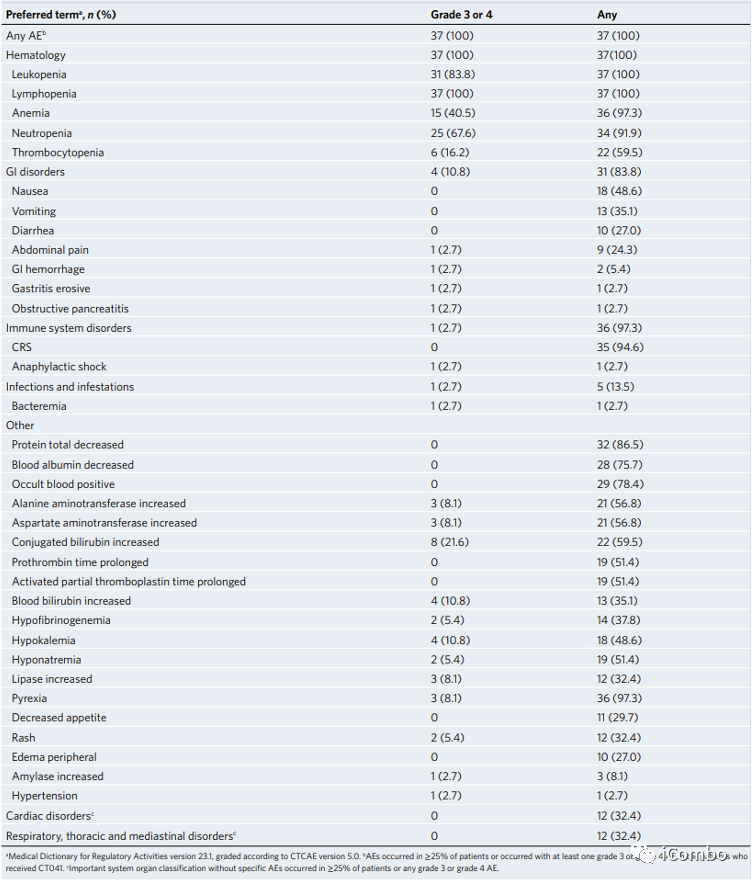
安全性
-
CT041首次输注后28天内未观察到DLT。
-
最常报告的≥3级不良事件为预处理相关血液学毒性(37/37,100%)、白细胞减少症(31/37,83.8%)、中性粒细胞减少症(25/37,67.6%)、贫血(15/37,40.5%)和血小板减少症(6/37,16.2%)。多发生于输注后28天内,中位恢复时间为4-9天。
-
本研究中未观察到≥3级细胞因子释放综合征(CRS)。1级或2级CRS中位发生时间为输注后2天,中位持续时间为6天。
-
未观察到免疫效应细胞相关神经毒性综合征(ICANS)。未报告治疗相关死亡。
以CLDN18.2为靶点的药物研究进展:ADC和双特异性抗体
目前已经进入临床试验的双特异性抗体包括Claudin18.2/CD3、Claudin18.2/4-1BB、Claudin18.2/PD-L1和Claudin18.2/CD47 。这些双特异性抗体相比单克隆抗体具有更强的特异性和更低的脱靶毒性,对胃癌和胰腺癌的治疗具有潜力。
安进/百济神州的AMG 910为靶向CLDN18.2和CD3的双特异性T细胞接合剂(BiTE)分子,是首个进入临床的 Claudin18.2/CD3 双抗
国内信达公司的IBI389(NCT05164458)以及齐鲁制药的QLS31905(NCT05278832)也有类似药物正在Ⅰ期临床试验阶段。
康诺亚生物的 CMG901,是全球首个Claudin18.2 ADC,CMG901是由靶向 Claudin18.2的人源化单抗CM311和微管聚合蛋白抑制剂MMAE通过可裂解连接臂偶联而成的ADC。
荣昌、石药、恒瑞、礼新医药等均有靶向Claudin18.2 的 ADC布局,正在开展Ⅰ/Ⅱ期临床研究。
多个ADC和双特异性抗体的临床试验仍在进行中,尚未公布结果。
小结
1. CLDN18.2限制性地分布于正常胃组织,并在GC组织中下调;但在其他肿瘤组织中高度激活,包括胰腺、食管、胆道、卵巢和肺肿瘤。
2. CLDN18.2在胃癌形成过程中有高表达,在转移灶中仍有表达。因此,CLDN18.2被认为是肿瘤治疗,特别是胃肠道肿瘤的理想靶点。
3. CLDN18.2在不同类型的肿瘤中可以作为癌基因或抑癌基因,其表达受CpG岛、PKC、ERK/MAPK、HER2/HER3信号通路和microRNA的甲基化状态的调节。
单克隆抗体和CAR-T疗法在CLDN 18.2阳性胃癌和胰腺癌人群中表现出了良好的安全性,并在临床疗效方面取得了令人鼓舞的初步结果。
正在进行的针对CLDN18.2在各种肿瘤中的长期研究或新兴药物的临床试验结果令人期待,这可能为数百万CLDN18.2阳性肿瘤患者(包括GC、PC、肝细胞癌和胆管癌)提供新的潜在方法和获益。
未来探索的方向:可能从治疗中获益的CLDN18.2高表达人群的界定、标志物疗效的预测、不良反应的防控措施、多靶点共表达人群的治疗方案选择、免疫治疗的联合应用等。
后续的CAR-T细胞、ADC、bsAb药物的临床试验,无疑为CLDN18.2高表达、靶向药物或已行多线治疗疗效不佳的患者提供了更多的选择。
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言













#CAR-T# #胃肠道癌症# #CLDN18.2#
60