Cell Research:“高危”三阴性乳腺癌有望增添代谢治疗靶点,“复旦肿瘤”科学家绘制出很大三阴性乳腺癌代谢物图谱
2022-02-04 复旦大学 中国生物技术网
肿瘤代谢视角下的相关研究成果有效丰富了三阴性乳腺癌研究的内涵,巩固了‘临床问题-科学研究-临床实践’的研究闭环。
三阴性乳腺癌是“粉红杀手”乳腺癌的一种亚型,约占所有乳腺癌人群的15%。因恶性程度高、复发转移风险大、缺少精准治疗靶点,三阴性乳腺癌又被称为“最凶”乳腺癌。
今日,复旦大学附属肿瘤医院乳腺外科邵志敏教授、江一舟教授领衔团队成功绘制出当前世界上最大规模的三阴性乳腺癌代谢物图谱,优化了既往分型标准,为三阴性乳腺癌的精准个体化治疗提供新方向;作为三阴性乳腺癌“复旦分型”研究的延续,研究团队还针对目前疗效最差的两个三阴性乳腺癌亚型,提出对代谢通路中的关键代谢物鞘氨醇-1-磷酸和N-乙酰-天冬-谷氨酸的合成进行抑制,有望成为此类乳腺癌的精准靶向治疗的潜在策略。国际权威期刊Cell Research于日前刊登了这项重要成果,影响因子达到25.62。

三阴性乳腺癌“复旦分型”突破“无药可医”困境
据介绍,“雌激素受体”、“孕激素受体”、“HER2”是三种目前乳腺癌治疗最具临床意义的细胞分子,常常作为乳腺癌精准治疗的靶点,而三阴性乳腺癌因为这三种细胞分子表达均为阴性而得名。这种“三阴”特性也使得三阴性乳腺癌的治疗手段和疗效均劣于其他乳腺癌亚型。
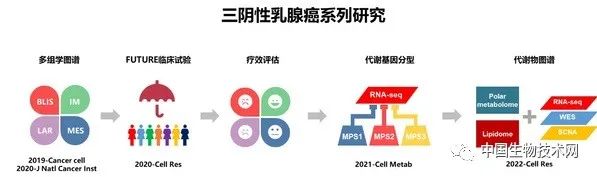
为寻求三阴性乳腺癌精准诊疗策略,复旦大学附属肿瘤医院邵志敏教授、江一舟教授领衔团队开展系列研究,持续攻关,于2019年在国际上率先绘制出全球最大三阴性乳腺癌多组学图谱,并据此提出三阴性乳腺癌“复旦分型”, 将三阴性乳腺癌分为了4个不同的亚型:免疫调节型、腔面雄激素受体型、基底样免疫抑制型、间质型;并针对每个亚型鉴定了一些潜在的治疗靶点。
在随即开始的名为“FUTURE(未来)”的“伞形”临床研究中,研究团队对前期研究发现进行验证,通过对不同“复旦分型”精准施治,突破了既往难治性三阴性乳腺癌患者“无药可医”的困境,将“无药可治”的多线治疗失败的复发转移性三阴性乳腺癌治疗有效率从10%提高到29%。但同时,研究团队也发现,部分前期鉴定的靶点疗效未达预期,比如腔面雄激素受体型和基底样免疫抑制型疗效较差,不良反应较多。因此,研究团队不断对这部分疗效差的亚型深化研究,尝试寻找新的治疗靶点,为三阴性乳腺癌患者带来更好的疗效。
绘制最大代谢物图谱锁定三阴性乳腺癌“高危”亚型
为确保快速增殖,癌细胞通常较正常细胞需要消耗更多的营养和能量,因此肿瘤细胞代谢呈现与正常细胞明显不同的特征,这一特征也常常成为肿瘤学家们研究的重要方向。
邵志敏教授、江一舟教授团队尝试从肿瘤代谢的角度来对三阴性乳腺癌进一步研究,特别是那些疗效较差的亚型,以发现更多特异靶点,优化三阴性乳腺癌的精准治疗策略。
研究团队首先通过大量数据的综合分析,发现三阴性乳腺癌的代谢基因特征在不同样本中存在显著差异。多种生物信息学算法计算的结果提示,根据代谢基因的差异可以将三阴性乳腺癌分成三个代谢亚型,分别为脂质合成型、糖酵解型以及混合型。每种代谢亚型可采用不同的治疗手段,并可能在未来推向临床。相应研究成果发表于国际著名期刊《Cell Metabolism》。
前期关于代谢基因的研究,提示了三阴性乳腺癌具有显著的代谢紊乱,有进一步深入研究的必要。因此,邵志敏教授、江一舟教授团队继续深入挖掘三阴性乳腺癌代谢物的特征。通过对330例三阴性乳腺癌样本和部分配对癌旁组织进行极性代谢组和脂质代谢组的检测,最终绘制出当前世界最大规模的三阴性乳腺癌代谢物图谱,系统性解析了三阴性乳腺癌的代谢组特征:磷脂和鞘脂等多种脂质显著上调,糖基化相关代谢物堆积。代谢特征与肿瘤基因组的改变密切相关。根据代谢物特征可将三阴性乳腺癌进一步分成三个类型:鞘脂富集型,氧化代谢物和糖基化代谢物富集型和低代谢紊乱型。代谢物分型与前期代谢基因分型有一定吻合度,优化了“复旦分型”。
研究发现,根据代谢物特征可以将“复旦分型”中基底样免疫抑制亚型进一步分为两种类型。这两种细分后的亚型预后明显不同,可以更精准“锁定”基底样免疫抑制亚型三阴性乳腺癌中真正“高危”的患者群体,有助于寻找三阴性乳腺癌新的潜在代谢治疗靶点;另一种腔面雄激素受体亚型与鞘脂富集的代谢物亚型重合度较高,具有显著的神经酰胺类脂质堆积的特征,可能从中挖掘治疗靶点。
代谢通路关键物质有望成精准治疗靶点
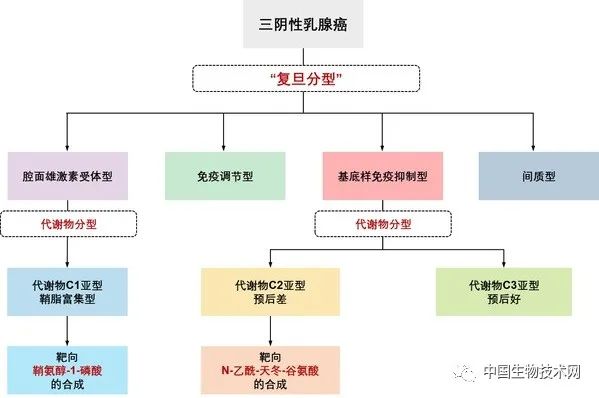
“腔面雄激素受体型和基底样免疫抑制亚型三阴性乳腺癌是‘FUTURE(未来)’研究中疗效较差或副反应比较大的类型,williamhill asia 希望通过肿瘤代谢视角开展研究,优化三阴性乳腺癌诊疗策略,”江一舟教授表示,“三阴性乳腺癌代谢物图谱的绘制,为捕捉这类亚型乳腺癌的有效靶点奠定了基础。”
在对“高危”基底样免疫抑制亚型三阴性乳腺癌的研究中,研究团队发现,N-乙酰-天冬-谷氨酸在谷氨酸代谢网络中发挥重要作用。通过抑制该物质合成,可有效抑制肿瘤的生长。
此外,在对另一种疗效较差的腔面雄激素受体型三阴性乳腺癌的代谢研究中,也取得了显著进展。利用研究团队建立的类器官平台和复旦大学附属肿瘤医院动物实验平台,研究人员通过一系列生物模型证实,靶向鞘氨醇-1-磷酸的合成或可成为针对腔面雄激素受体型三阴性乳腺癌的靶点。
“目前复旦肿瘤团队基于三阴性乳腺癌‘复旦分型’的研究已经衍生出诸多分支。肿瘤代谢视角下的相关研究成果有效丰富了三阴性乳腺癌研究的内涵,巩固了‘临床问题-科学研究-临床实践’的研究闭环,”邵志敏教授说,“研究团队不断探索为乳腺癌患者提供更精确的治疗策略,让延长更多三阴性乳腺癌患者的生存期不再只是梦想。”
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言










#阴性乳腺癌#
59
#治疗靶点#
74
#CEL#
58
#Cell#
70
#代谢物#
64
#三阴性#
0
#复旦#
62
#Research#
63
学习
79