新规来了!药物临床试验期间方案变更技术指导原则(试行)
2022-06-28 国家药监局药审中心 网络
适用于与注册相关的中药、化药、生物制品(含疫苗)相关的临床试验方案变更。
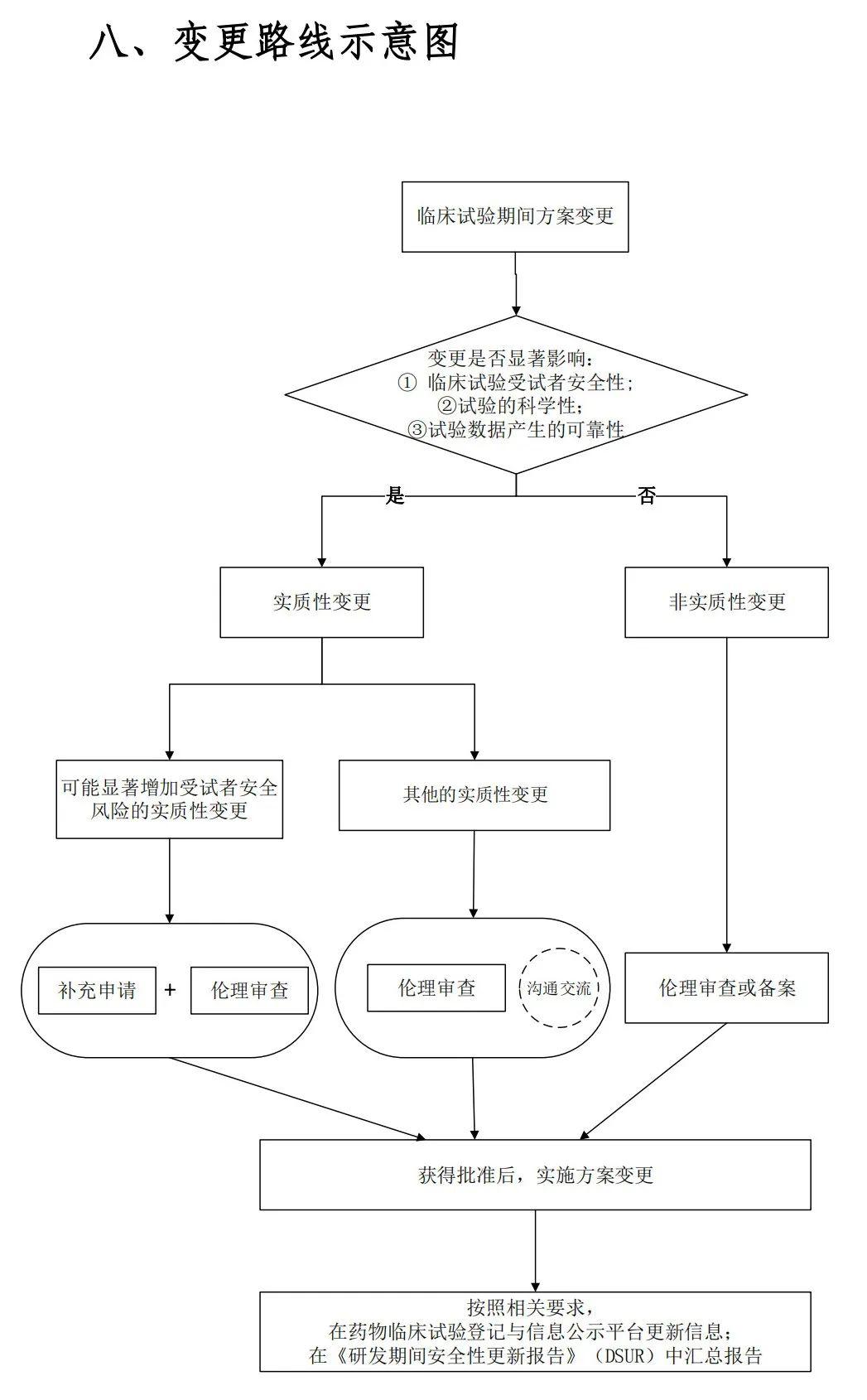
日前,国家药品监督管理局药品审评中心发布了《药物临床试验期间方案变更技术指导原则(试行)》。本指导原则适用于与注册相关的中药、化药、生物制品(含疫苗)相关的临床试验方案变更;不适用于临床试验期间改变剂型、给药途径、新增适应症以及增加与其他药物联合用药等情形。旨在指导药物临床试验申办者规范开展临床试验期间方案变更相关工作,自发布之日起施行。
具体通知如下:
为指导药物临床试验申办者规范开展临床试验期间方案变更相关工作,在国家药品监督管理局的部署下,药审中心组织制定了《药物临床试验期间方案变更技术指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审核同意,现予发布,自发布之日起施行。
特此通告。
国家药监局药审中心
2022年6月23日
附件:药物临床试验期间方案变更技术指导原则(试行)











本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言












#药物临床试验#
85
#技术指导原则#
70
#新规#
68