JOURNAL OF HEPATOLOGY:基于液体活检的蛋白质生物标志物用于胆管癌的风险预测、早期诊断和预后
2023-06-21 Jenny Ou MedSci原创 发表于上海
血清EV含有蛋白质生物标志物,用于CCA的预测、早期诊断和预测,可以使用总血清检测,代表个性化医学的肿瘤细胞衍生液体活检工具。

胆管癌(CCA)包括一组异质的恶性肿瘤,这些肿瘤可以在胆汁系统的任何位置出现。根据解剖学起源,它们被归类为肝内(iCCA)、围阚(pCCA)或远端(dCCA)。尽管CCA仍然被认为是一种罕见的癌症,但在过去几十年里,其全球发病率和相关死亡率一直在惊人地增长。此外,这些肿瘤的无声增长严重损害了它们的早期检测,限制了患者获得潜在治疗方案(即肿瘤切除)的机会。
CCA诊断需要成像方法和进一步的细胞学/组织学确认。癌症生物标志物碳水化合物抗原19-9(CA19-9)是目前诊所用于帮助CCA诊断的唯一液体活检工具,但其诊断能力很低,特别是在CCA早期阶段。当前非侵入性诊断方法的次优准确性反映了细胞学/组织学确认的必要性。然而,由于患者的脆弱性和晚期疾病阶段,出血和腹膜播种的风险,和/或收集的组织数量少,可能不足以进行细胞学/组织学确认,特别是在pCCA和dCCA病例中,有时不鼓励进行肿瘤活检或刷牙。
大多数CCA被认为是零星的,缺乏明确的病因,尽管一些成熟的条件会显著增加CCA发展的几率,包括胆道囊肿、胆结石、肝硬化、某些病毒或胆道疾病(例如原发性硬化性胆管炎[PSC])的存在。特别是,PSC是一种病因不明的慢性胆汁淤积和免疫介导的肝病,其特征是肝细胞死亡、纤维化和肝功能衰竭。PSC给CCA的发展带来了巨大的风险(高达20%的终身风险),导致过早死亡。
使用非侵入性方法对PSC患者进行CCA的早期诊断具有挑战性,因为良性和恶性胆道狭窄之间存在重叠的放射学特征。所有这些证据都强调了CCA需要准确的非侵入性生物标志物,以此建立监测计划,在高风险人群中早期发现这些生物标志物,并更快地诊断零星的CCA,最终降低与癌症相关的死亡率。
细胞外囊泡(EVs)是纳米脂质双层球体,是人类疾病生物标志物的有希望的来源。这些从细胞释放出来,存在于生物流体中,含有不同类型的生物分子(如蛋白质、核酸、脂质和代谢物),并参与细胞之间的通信,是生物标志物发现的有用工具。
2023年3月1日发表在JOURNAL OF HEPATOLOGY上的文章,通过质谱法表征了来自分离性PSC、伴随PSC-CCA、在随访期间出现CCA的PSC、非PSC病因的CCA和肝细胞癌和健康个体的EV。ELISA定义并验证了PSC-CCA、非PSC CCA或CCA的诊断生物标志物,无论其病因如何(Pan-CCA)。在单细胞水平的CCA肿瘤中评估了它们的表达。调查了CCA的预后EV生物标志物。

本文摘要图
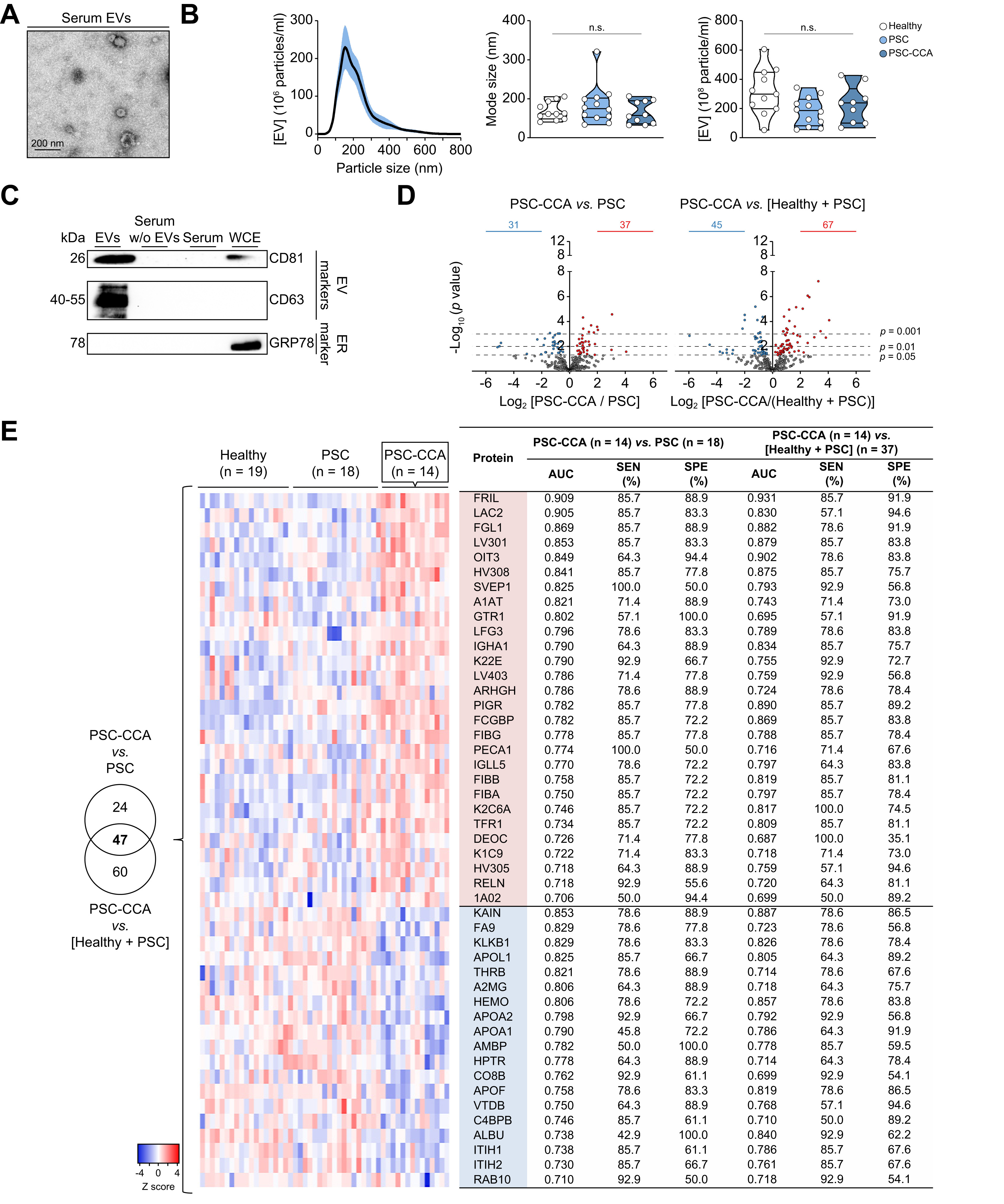
分离的血清EV组分富含外切体和微囊,并含有具有PSC-CCA诊断能力的蛋白质
EV的高通量蛋白质组学确定了PSC-CCA、非PSC CCA或Pan-CCA的诊断生物标志物,以及肝内CCA和肝细胞癌的鉴别诊断,这些生物标志物由ELISA使用总血清进行交叉验证。基于机器学习的算法披露了CRP/FIBRINOGEN/FRIL用于诊断PSC-CCA(局部疾病[LD])与孤立的PSC(AUC = 0.947;赔率比[OR] =36.9),并与碳水化合物抗原19-9相结合,仅超过碳水化合物抗原19-9。
CRP/PIGR/VWF允许诊断LD非PSC CCA与健康个体(AUC = 0.992;OR = 387.5)。值得注意的是,CRP/FRIL准确诊断为LD Pan-CCA(AUC = 0.941;OR = 89.4)。在出现恶性肿瘤的临床证据之前,CRP/FIBRINOGEN/FRIL/PIGR水平显示了PSC中CCA发展的预测能力。多器官转录组学分析显示,血清EV生物标志物主要在肝胆组织中表达,CCA肿瘤的单细胞RNA测序和免疫荧光分析显示,它们主要存在于恶性胆管细胞中。多变量分析揭示了EV预后生物标志物,COMP/GNAI2/CFAI和ACTN1/MYCT1/PF4V分别与患者的生存率呈负值和正值。
综上所述,本文证明,血清EVs含有蛋白质生物标志物,用于预测PSC中的CCA发展,以及PSC患者、没有PSC患者和CCA患者的早期肿瘤检测,无论其病因如何,这些都可以使用总血清进行检测。这具有重要的临床相关性,因为PSC无症状患者的早期CCA检测与肝移植后OS的改善和无复发生存率有关,还因为与更高级CCA的患者相比,接受手术或肝移植的“非常早期”iCCA患者表现出更好的预后。
本文还强化了由不同病因引起的CCA患者的想法(例如PSC与非PSC)可能具有共同和不同的血清EV蛋白,因此,需要使用适当、定义明确的生物标志物来识别特定患者亚组中的CCA,从而在CCA的个性化诊断方面向前迈进了一步。这一点,再加上大多数候选生物标志物优先在CCA肿瘤内的恶性胆管细胞中表达,这加强了作为创新的肿瘤细胞衍生液体活检策略的方法。为了确认这些新的预测、诊断和预后生物标志物的转化能力,应该使用更大的患者队列进行下一个前瞻性验证阶段。这将为CCA的早期非侵入性诊断开辟一条新的途径,从而实现及时的治疗干预,并改善患者的福利和结果。
原文出处
Lapitz, A.; Azkargorta, M.; Milkiewicz, P.; Olaizola, P.; Zhuravleva, E.; Grimsrud, M. M.; Schramm, C.; Arbelaiz, A.; O'Rourke, C. J.; La Casta, A.; Milkiewicz, M.; Pastor, T.; Vesterhus, M.; Jimenez-Agüero, R.; Dill, M. T.; Lamarca, A.; Valle, J. W.; Macias, R. I. R.; Izquierdo-Sanchez, L.; Pérez Castaño, Y.; Caballero-Camino, F. J.; Riaño, I.; Krawczyk, M.; Ibarra, C.; Bustamante, J.; Nova-Camacho, L. M.; Falcon-Perez, J. M.; Elortza, F.; Perugorria, M. J.; Andersen, J. B.; Bujanda, L.; Karlsen, T. H.; Folseraas, T.; Rodrigues, P. M.; Banales, J. M., Liquid biopsy-based protein biomarkers for risk prediction, early diagnosis, and prognostication of cholangiocarcinoma. Journal of Hepatology 2023, 79 (1), 93-108.
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言