ALK阳性NSCLC治疗药物Aalectinib被FDA授予突破性药物资格
2016-10-05 Mechront 译 MedSci原创
罗氏旗下Genentech于10月4日称:成人晚期ALK阳性非小细胞肺癌(NSCLC)一线治疗药物——肺癌新药Alecensa(alectinib)——获FDA授予突破性药物资格。 FDA此决定主要基于J-ALEX研究的结果;该研究为开放标签、3期试验,纳入了207例未经治疗的ALK阳性、晚期或复发性NSCLC患者,被随机分为alectinib (Alecensa, Genentech)或c
罗氏旗下Genentech于10月4日称:成人晚期ALK阳性非小细胞肺癌(NSCLC)一线治疗药物——肺癌新药Alecensa(alectinib)——获FDA授予突破性药物资格。
FDA此决定主要基于J-ALEX研究的结果;该研究为开放标签、3期试验,纳入了207例未经治疗的ALK阳性、晚期或复发性NSCLC患者,被随机分为alectinib (Alecensa, Genentech)或crizotinib (Xalkori, Pfizer)组进行治疗。
alectinib组患者与crizotinib组患者相比,疾病进展或死亡风险下降66%(HR = 0.34, 95% CI, 0.17-0.7)。
alectinib组患者的中位PFS未达;crizotinib组患者的中位PFS为10.2个月(95% CI, 8.2-12。
crizotinib组的3到4级不良事件的发生比alectinib组更频繁(51% vs. 27%)。
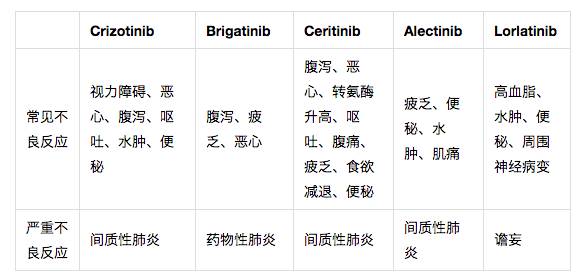
alectinib组最常见的不良反应包括恶心(74%)、腹泻(73%)、呕吐(59%)、视觉障碍(55%)、味觉障碍(52%),便秘(46%)、丙氨酸转氨酶升高(32%)和天冬氨酸转氨酶升高(31%)。
原始出处:
FDA grants breakthrough therapy designation to Alecensa for first-line treatment of ALK–positive NSCLC.Helaio.October 4, 2016
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言










#药物资格#
66
#阳性NSCLC#
48
#ALK阳性#
44
#Alectinib#
53
#Aalectinib#
52
#突破性药物资格#
61
#ALK阳性NSCLC#
59
#治疗药物#
47
#Aalectinib#
50
#突破性药物#
55