RNAi疗法lumasiran获得欧盟批准治疗1型原发性高草酸尿症
2020-11-20 MedSci原创 MedSci原创
Alnylam Pharmaceuticals宣布,欧盟委员会批准了其RNAi治疗药物Oxlumo(lumasiran)用于治疗1型原发性高草酸尿症(PH1)。
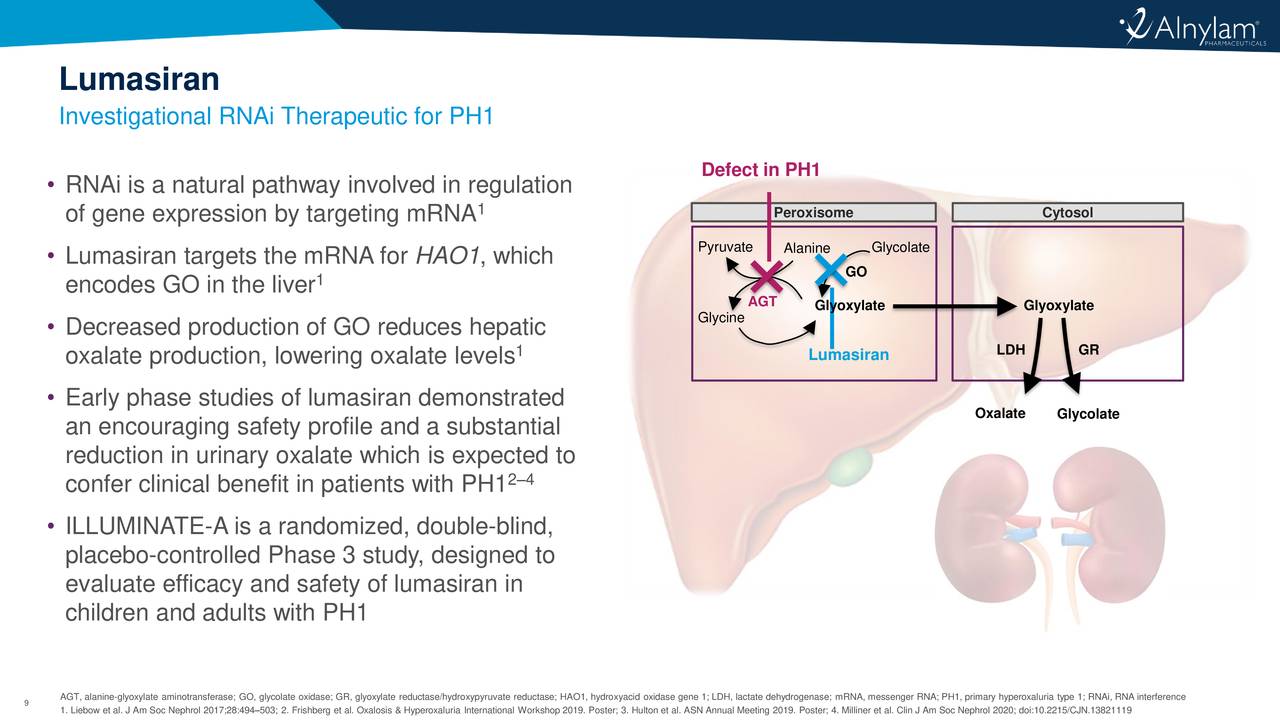
Alnylam Pharmaceuticals宣布,欧盟委员会批准了其RNAi治疗药物Oxlumo(lumasiran)用于治疗1型原发性高草酸尿症(PH1)。Lumasiran通过降解HAO1 mRNA和消耗乙醇酸氧化酶来发挥作用,乙醇酸氧化酶则进一步抑制肝脏过度生产的草酸盐,草酸盐可促进PH1疾病进展。
图片来源:seekingalpha.com
首席执行官John Maraganore表示:“ Alnylam的Lumasiran从发现到获得监管机构批准仅仅花了六年时间。” 上个月,欧洲药品管理局人用药品委员会基于两项III期试验的数据发表了正面意见,此后获得了监管部门的批准。
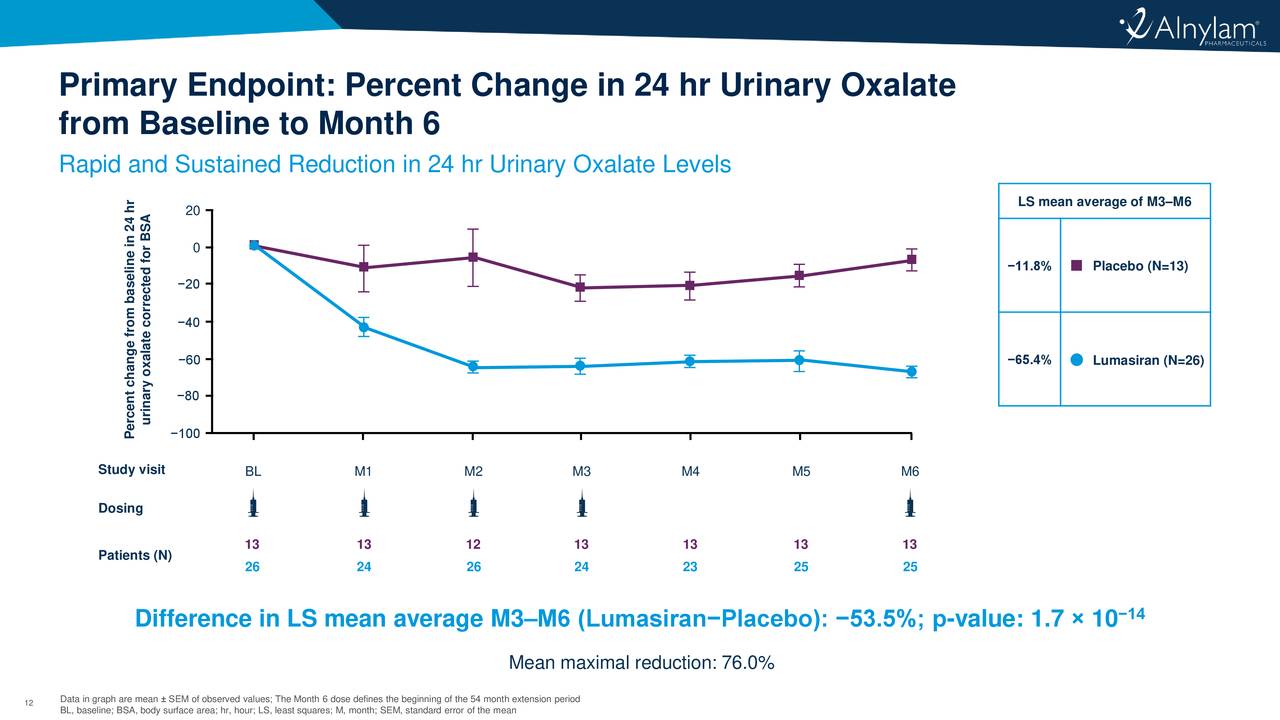
在ILLUMINATE-A中,包括成人和六岁及以上的儿童,Oxlumo达到了主要终点,尿草酸盐相对于安慰剂平均减少了53.5%,并且草酸盐相对于基线平均减少了65.4%。与安慰剂组相比,大多数接受Oxlumo治疗患者的草酸尿水平也达到了正常或接近正常水平。同时,在六岁以下婴幼儿中评估的ILLUMINATE-B研究也显示Oxlumo的疗效结果和安全性与ILLUMINATE-A中观察到的相当。
图片来源:seekingalpha.com
该疗法是由医护人员每月一次皮下注射,持续三个月,然后每季度一次。Oxlumo也在美国被授予优先审查,FDA预计将于12月3日做出决定。
原始出处:
https://www.firstwordpharma.com/node/1775889?tsid=28®ion_id=2
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言









#原发性#
43
#RNAi#
57
替代移植吗
105
#RNAi疗法Lumasiran#
57
#欧盟批准#
63
#RNAi疗法#lumasiran获得#欧盟#批准治疗1型#原发性高草酸尿症#,RNAi疗法的新药很快就会大量问世了
186