既往研究显示,针对CTLA-4和PD-1免疫检查点阻断联合疗法(CICB)与患者的高客观反应率相关,但很大一部分患者会经历免疫相关不良事件(irAE)。有趣的是,患者的临床反应率和irAE似乎相关,目前关于治疗毒性的相关分子机制尚不清楚。
因此,需要深入了解CICB治疗的相关生物标志物以及患者对CICB的反应和药物毒性相关机制。
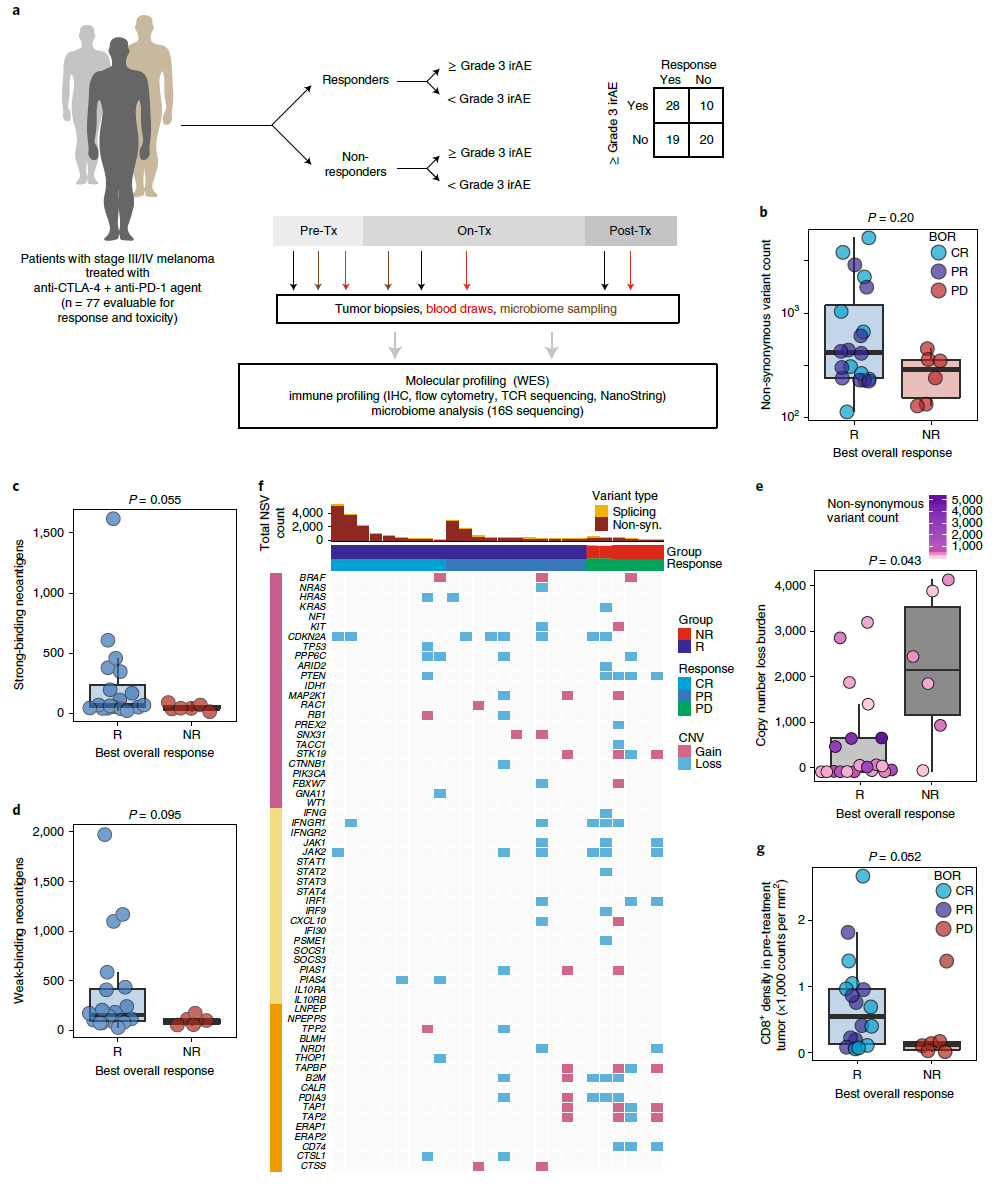
为了解决上述问题,研究人员对77名接受CICB治疗的晚期黑色素瘤患者的血液、肿瘤组织和肠道微生物组进行了分析,并在临床前模型中进行了平行研究。
患者治疗反应的分子和免疫预测因子分析
结果显示,任何≥3级的免疫相关不良事件的发生率均很高(49%)。对CICB治疗反应的肿瘤相关免疫和基因组生物标志物与ICB单药治疗中所鉴定的生物标志物类似,且研究人员发现,CICB的毒性与更多样化的外周T细胞库相关。肠道微生物组分析显示,具有药物毒性反应的患者的肠道拟杆菌的丰度显著更高,在结肠炎患者样本和临床前模型中粘膜IL-1β的水平上调。
肠道微生物与CICB反应的关联性
总而言之,该研究结果为靶向CICB毒性提供了潜在的新治疗策略。
原始出处:
Andrews, M.C., Duong, C.P.M., Gopalakrishnan, V. et al. Gut microbiota signatures are associated with toxicity to combined CTLA-4 and PD-1 blockade. Nat Med (08 July 2021).
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言











#Nat#
49
#微生物#
56
#阻断#
50
#微生物组#
68
#肠道微生物组#
51
#CTLA-4#
73
#Med#
61
😎
82