JAMA Oncol | 新辅助阿替利珠单抗联合化疗放疗治疗不可切除性 III 期 NSCLC 的疗效和安全性
2024-07-28 daikun MedSci原创 发表于上海
该研究旨在评估在不可切除的III期NSCLC患者中,在CRT前后给予阿替利珠单抗治疗的安全性及有效性,新辅助阿替利珠单抗在不可切除性III期NSCLC患者中具有良好的安全性,并显示出令人鼓舞的疗效。
对于不可切除的 III 期 NSCLC 患者,传统的化疗放疗方案 (CRT) 治疗效果有限,5 年生存率约为 15%,PACIFIC 试验证实了辅助性度伐利尤单抗在 CRT 后的疗效,将 5 年生存率提高了约 10%,然而,该研究仅纳入了CRT 后病情稳定且无进展的患者,新的研究表明,在 CRT 前给予免疫检查点抑制剂 (ICI) 可能会提高更多患者的疗效,该研究旨在评估在不可切除的 III 期 NSCLC 患者中,在 CRT 前后给予阿替利珠单抗治疗的安全性及有效性。

方法
该研究是一项单队列、II 期、非随机对照试验,纳入了病理确诊的不可切除性 III 期非小细胞肺癌 (NSCLC) 患者,ECOG 体能状态良好 (0-1 分), 具有可测量疾病,患者接受新辅助治疗: 4 个周期的阿替利珠单抗 (1200 mg,静脉注射,每 21 天一次); 化疗放疗: 阿替利珠单抗完成后,进行放疗 (60 Gy,照射野) 联合每周卡铂 (曲线下面积 2) 和紫杉醇 (50 mg/m²),随后进行巩固化疗 (卡铂曲线下面积 6 和紫杉醇 200 mg/m²,每 21 天一次,共 2 个周期) ;辅助治疗: 放疗完成后,继续使用阿替利珠单抗 (1200 mg,每 21 天一次) 完成 1 年的治疗。主要终点为12 周疾病控制率 (DCR), 次要终点为无进展生存期 (PFS) 、总生存期 (OS)、 客观缓解率 (ORR)和 安全性。
研究结果
75.8% 的患者完成了新辅助治疗,71.0% 的患者完成了化疗放疗,41.9% 的患者完成了所有研究治疗。新辅助治疗 12 周后的 DCR 为 74.2%,客观缓解率 (ORR) 为 66.2%,中位无进展生存期 (PFS) 为 30.0 个月,中位总生存期 (OS) 未达到,24 个月生存率为 73.7%。
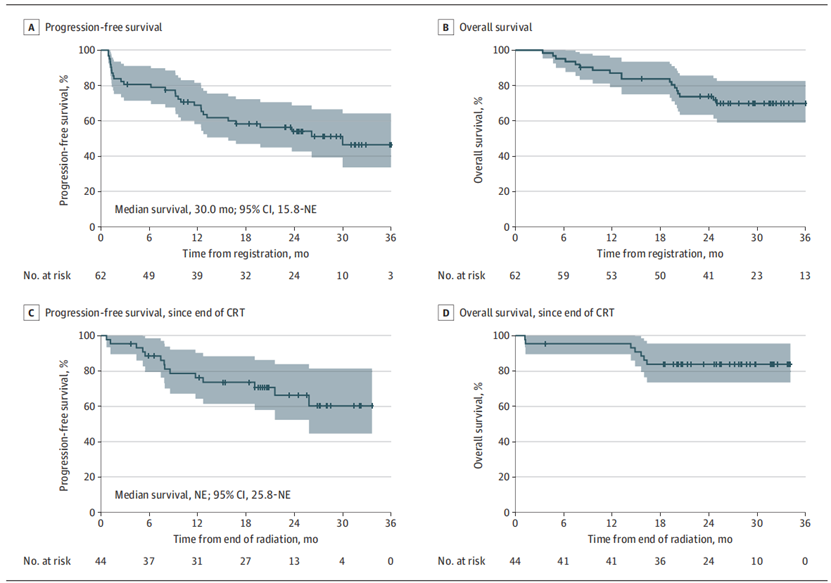
安全性分析
27.4% 的患者出现 3 级或更高的免疫相关不良事件,包括 1 例 5 级肺炎和 1 例 4 级吉兰-巴雷综合征,48.4% 的患者出现 3 级或更高的治疗相关不良事件,12 名患者因不良事件停止治疗。
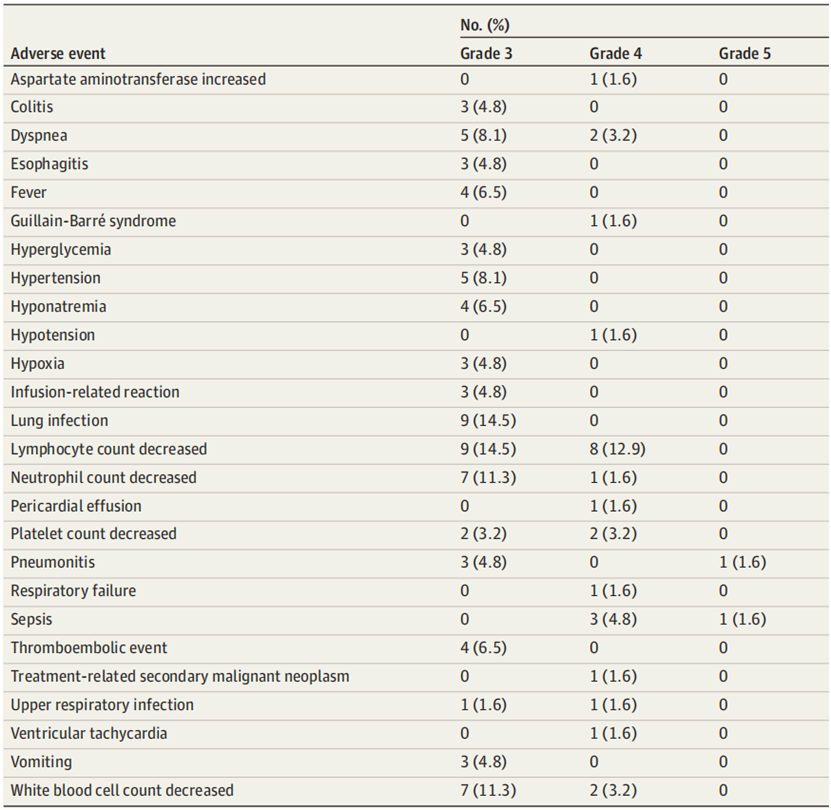
结论
这项 II 期非随机对照试验表明,新辅助阿替利珠单抗在不可切除性 III 期 NSCLC 患者中具有良好的安全性,并显示出令人鼓舞的疗效,未来需要开展随机对照试验,进一步验证新辅助阿替利珠单抗的疗效和安全性。
原始出处
Ross HJ, Kozono D, Wang XF, et al. Atezolizumab Before and After Chemoradiation for Unresectable Stage III Non–Small Cell Lung Cancer: A Phase II Nonrandomized Controlled Trial. JAMA Oncol. Published online July 25, 2024. doi:10.1001/jamaoncol.2024.1897.
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言














#NSCLC# #阿替利珠单抗# #化疗放疗#
14