引领多发性硬化治疗新纪元——承诺中华,不负所托
2020-08-07 陶然 健康界
当人类1‰概率的事情发生在1/14亿的生命个体时,那往往并不是一件幸运的事,罕见病患者就是这样一种“特殊”存在,瓷娃娃(成骨不全症)、蜘蛛人(马凡综合征)、渐冻人
当人类1‰概率的事情发生在1/14亿的生命个体时,那往往并不是一件幸运的事,罕见病患者就是这样一种“特殊”存在,瓷娃娃(成骨不全症)、蜘蛛人(马凡综合征)、渐冻人(进行性肌营养不良症)、月亮孩子(白化病)、大理石宝宝(骨质石化症)、企鹅家族(小脑萎缩症)......成为了他们“形象”的代名词。
多发性硬化(multiple sclerosis,MS)作为罕见病的一种,好发于青壮年,据2018年中华医学会神经病学分会发布的《中国多发性硬化患者生存报告》估计,我国约有3万名MS患者,约2/3的患者确诊该病需耗费1~5年,而12%患者确诊时间耗费可超过6年,并且大部分患者未接受标准治疗。从这些数据可以看出,MS等罕见病救治过程是一条艰难之路,难以诊断、难以治疗和难以获得药物是罕见病患者的困境。
诺华制药,取意于“承诺中华”,秉持着“承诺通过不断创新的产品和服务,致力于提高中国人民的健康水平和生活质量”的宗旨,一直以来,诺华制药从未停止对各种罕见病的探索。据了解,诺华科学家已经对40多种罕见病的治疗方法进行了调查研究,不断探索罕见病用药的新途径、新靶点,特别是在MS新药研发方面。
聚焦MS用药,多重保障患者未来
8月1日,为了提高罕见病领域对S1P受体调节剂的认知水平,打通领域壁垒分享资源,诺华制药特别联合健康界传媒进行了一场以“MS用药的现状与未来”为主题的线上研讨会,这场会议由健康界传媒执行CEO王娜主持,并且多位重量级嘉宾出席,中国罕见病联盟执行理事长、中国医院协会副会长李林康教授特别为本次会议发来了致辞。
李林康教授表示非常高兴能有这样一个机会,单纯就MS用药这一个问题进行深入交流,并且极大肯定了国家政府、中国罕见病联盟、药企等在罕见病及其药物方面的重视与支持力度。
近年来,无论是在加快罕见病药物审评审批、罕见病药物创新、药物供应支持方面,还是在罕见病诊疗、药物报销方面,我国陆续出台了相关政策,大连医科大学公共卫生学院袁妮教授在“国内外罕见病和药物报销政策”的主题演讲中详细阐述了我国罕见病医疗保障制度的发展过程。
首都医科大学附属北京天坛医院的张星虎教授通过临床真实生动的案例,系统分析了S1P受体调节剂——芬戈莫德的治疗方案,引发了大家对MS用药的进一步探究,MS患者的用药种类有限,但新药研发之路仍在不断开拓向前,诺华制药在这方面做出了很好的示范。
张星虎教授介绍芬戈莫德的临床研究
全力向前,实现NEDA-4四重控制
2019年7月19日,诺华制药(中国)宣布,国家药品监督管理局批准捷灵亚?(芬戈莫德)用于治疗10岁或10岁以上患者的复发型多发性硬化(RMS),这是目前唯一一个有儿童适应症的多发性硬化疾病修正治疗(DMT)药物,同时也是目前临床现有的三种DMT中唯一可实现NEDA-4四重控制的药物。
芬戈莫德发挥双重作用机制
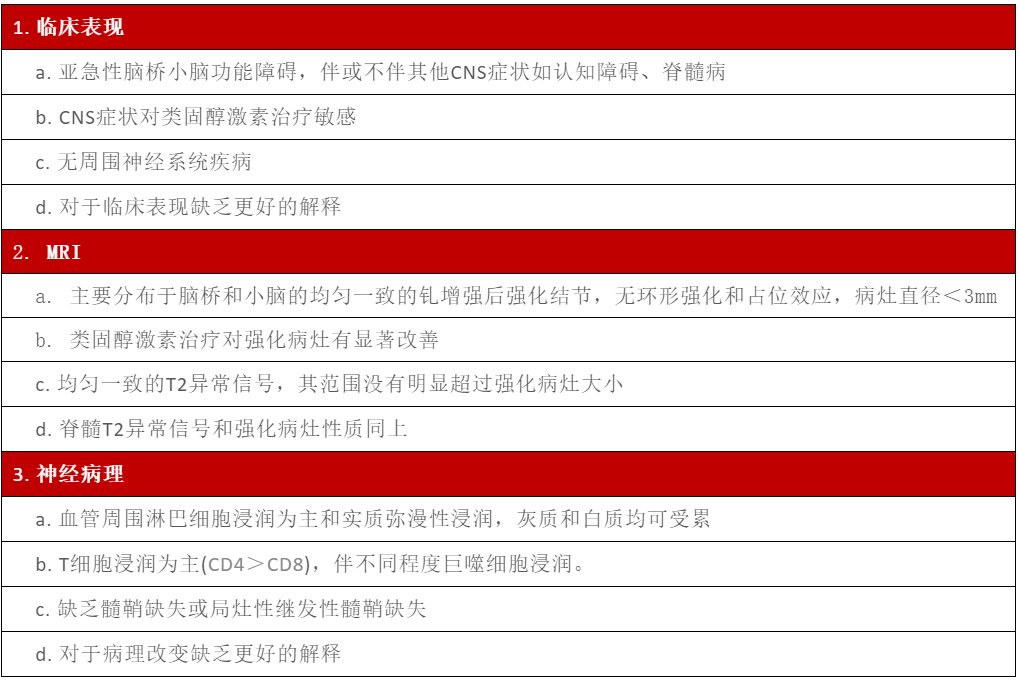
据悉,芬戈莫德自全球上市以来,已在80多个国家获批,近30万例患者获益。纵观目前已上市和处于临床II期、III期的药物,针对MS的药物开发策略主要分为三种:新型免疫调节剂、靶向S1P受体调节剂和神经修复剂,其中靶向S1P受体调节剂是较新的MS靶点药物。北京协和医院的梅丹教授就MS新药研发与新靶点机制的内容也带来了精彩讲说,梅丹教授从我国MS流行病学数据出发,通过介绍MS的病理机制深入分析到MS临床发展与结局。
梅丹教授肯定芬戈莫德的临床疗效
但如芬戈莫德这些新药的诞生之路往往充满挑战,芬戈莫德自2010年FDA获批成全球第一个口服DMT药物,在全球近30万患者验证了其疗效及安全性,长达14年临床研究证实了芬戈莫德的长期安全性良好,不良事件发生率低。为此,复旦大学附属华山医院的钟明康教授就MS药物研发面临的挑战与机遇进行了详细阐述。如钟明康教授所说,药物从首次发现到应用于临床需经历层层的考核验证,药物的临床研究评价指标非常关键。
钟明康教授介绍芬戈莫德发展历程
医药联合,循证数据支持新发展
会议最后,首都医科大学附属北京天坛医院赵志刚教授就MS用药保障和患者获益等问题主持并进行讨论,同时参与讨论的还有复旦大学附属华山医院陈向军教授、首都医科大学宣武医院董会卿教授、中国人民解放军总医院黄德晖教授、北京大学人民医院封宇飞教授、中日友好医院李朋梅教授、四川省人民医院童荣生教授、首都医科大学宣武医院闫素英教授、南华大学附属南华医院周玉生教授、北京医院张华教授多位优秀专家。
多位专家就MS用药保障和患者获益问题进行讨论
众所周知,新药往往需要经过多项临床前研究千锤百炼后从而真正走进临床,北京大学人民医院封宇飞教授特别建议药物上市后应多进行注册研究。芬戈莫德在我国上市之后,现有处方的患者疗效显着,作为国家药品监督管理局药品审评中心承诺的一部分,诺华也已经计划开展针对芬戈莫德的PAC STUDY在多个中心内补充相关的中国人群数据,将给我国临床医生和患者更全面的数据支持,让更多临床医生和患者放心治疗。
聆听了多位专家的讲说后,南华大学附属南华医院周玉生教授强调临床药师团队也应加强参与临床的治疗,站在患者角度,保障用药供应。陈向军教授对此同样做出了解释,“在罕见病用药方面,药物的安全性应该由临床药师提供指导建议,而药物有效性和疾病机制解释方面需要临床医生和亚专科医生发挥更多作用”,陈向军教授同时强调像芬戈莫德这类分子靶向药物可以进行更多创新性研究。
不负所托,双药新生显实力
诺华公司在创新药物研发方面从未停止探索的脚步,继芬戈莫德之后,2019年西尼莫德在FDA首批,在我国被列入1类创新药,2020年5月实现了与全球的同步上市。芬戈莫德在外周与中枢的双重机制下更注重外周的炎症控制,在复发缓解阶段一线早期使用将使患者获益更大。与芬戈莫德不同的是,西尼莫德在机制上更侧重于中枢内神经变性的修复,在有进展早期信号的患者人群上更有疗效优势。
芬戈莫德和西尼莫德的优势患者人群对比
董会卿教授特别感谢了国家对罕见病的重视,表达了对芬戈莫德临床疗效的肯定,同时对芬戈莫德进入医保后的价格饱含期待。芬戈莫德作为第一批48种临床境外急需新药目录之后,2019年7月正式获批,2020年1月正式上市,目前属于自费药物(建议零售价为10 500元/盒,一盒28片,一日一片)。考虑MS患者的经济负担,诺华制药再次表示,虽然芬戈莫德还未进入医保,但是诺华非常有诚意进行医保谈判,从而真正造福我国MS患者。
未来可期,创新发展共促药物可及
会中,黄德晖教授结合临床实际诊疗经验强调院内MDT诊疗模式应联合药学专家从而进一步促进罕见病诊疗,同时建议我国MS的诊疗应以中心模式开展。张华教授强调了MS早诊早治的重要性,同时指出MS的检测、诊断、收费等应尽量标准化,从而真正实现药物的可及性。童荣生教授再次强调了药事服务在罕见病诊疗中的作用和价值,同时期待对芬戈莫德的安全性开展更多研究。“药物监护在患者用药期间亟需重视,并且需要关注反弹症状以及如何进行防范。”闫素英教授对药物监护做了特别强调,并且指出芬戈莫德等新药发展阶段更应如此。
如大家所知,MS是长期进展免疫疾病,对MS患者停止任何免疫调节治疗都可能出现疾病活动性的恢复,这与疾病本身的波动性相关,临床很难明确界定疾病活动性恢复或反弹,而停用DMT药物都有疾病活动性恢复或反弹的风险。令人欣慰的是,芬戈莫德自2010年上市以来已经应用于80多个国家近30万MS患者,FDA报道中仅发现了35例反弹,临床为万分之一数量级的发生率。李朋梅教授在会议最后中对芬戈莫德的发展前景予以深厚期待,“如果药物本身的疗效性和安全性都有很好的循证数据支持,并且在准入医保后切实考虑患者经济负担,我相信这个药物是有希望的”。
“罕见病用药是世界性难题,需要政府、医院、药企、社会多方位努力,促进创新药物研发、创新管理模式以及创新诊疗模式”,赵志刚教授对多位专家的精彩讨论做出了最后的分析。会议最后,健康界执行CEO王娜进行了总结,“在罕见病用药医保制度不断优化落实的过程中,相信如诺华制药这样具有强大社会责任感的企业,在MS新药研发方面将为williamhill asia 不断带来好消息”。
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言









#新纪元#
54
#多发性#
54