老年男性残胃癌1例报道及多学科分析
2013-07-19 解放军307医院消化肿瘤科 葛飞娇 中国医学论坛报
病例简介 病史及既往史 男性,77岁,因“进食哽噎感1个月”于2010年9月就诊。 既往史: 36年前因良性胃穿孔行远端胃切除毕罗氏I式吻合。 入院检查及诊断 辅助检查 实验室检查异常结果:血红蛋白96 g/L(120~160 g/L),肿瘤标志物糖类抗原(CA19-9)138.9 U/ml。 内
病例简介
病史及既往史
男性,77岁,因“进食哽噎感1个月”于2010年9月就诊。 既往史: 36年前因良性胃穿孔行远端胃切除毕罗氏I式吻合。
入院检查及诊断
辅助检查
实验室检查异常结果:血红蛋白96 g/L(120~160 g/L),肿瘤标志物糖类抗原(CA19-9)138.9 U/ml。
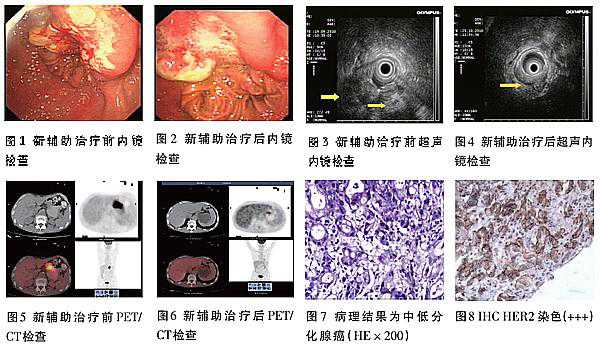
内镜检查:胃-肠吻合口可见隆起型肿物(图1);超声内镜(EUS)检查可见肿物呈低回声改变,局部胃壁五层结构消失,肿物侵透外膜并与周围组织分界不清,胃周围未见肿大淋巴结(图3)。
腹部CT检查:残胃腔内可见肿物生长,增强扫描见强化影。正电子发射体层摄影(PET)/CT检查显示残胃内肿物代谢活性增高,标准化摄取比(SUV)11.5,全身其他各处未见异常放射性分布(图5)。
内镜活检病理结果:胃中低分化腺癌,劳伦斯(Laurence)分型混合型(图7);免疫组织化学染色(IHC)检测,人表皮生长因子受体2(HER2)+++(图8)。
查体:上腹轻压痛,其余未见异常。
诊断
残胃癌cT4aN0M0 [ⅢB期,美国癌症联合会(AJCC)第7版]。
术前新辅助治疗
术前行XELOX方案(奥沙利铂+卡培他滨)联合曲妥珠单抗方案治疗3个周期,疗程中出现药物毒性标准(CTC)4级中性粒细胞减少及血小板减少,给予药物减量并延期化疗。
治疗后,内镜及超声内镜复查显示胃内隆起型肿物范围较前明显缩小,肿物呈低回声改变,但仍侵犯胃壁全层并突破外膜,与周围组织分界不清(图2,4)。
PET/CT复查提示残胃内肿物范围较化疗前明显缩小,代谢活性显著降低,SUV值3.5,全身其他各处未见异常放射性分布(图6)。CA19-9显著下降至38.1 U/ml。
手术及术后辅助治疗
手术治疗 行残胃癌根治术。
术后病理检查 残胃吻合口溃疡型中分化腺癌,大小4.0×3.0 cm,侵透胃壁全层并侵犯部分结肠壁,可见脉管癌栓,淋巴结未见转移(0/37),肠管断端及食管断端未见癌细胞。
IHC染色,CD34 (+),CD44 (+),受体酪氨酸激酶(c-Met)(+), 唾液酸糖蛋白(D2-40)(+),表皮生长因子受体(EGFR)(-),HER2(++),细胞因子P170(-),P27(-),P53(-)。荧光原位杂交(FISH)法检测HER2(+)。病理分期T4aN0M0(ⅢB期,AJCC第7版)。
术后辅助治疗 因患者高龄、术后恢复欠佳,选择单药替吉奥(S1)辅助化疗3个周期,因无法耐受不良反应而停止治疗。
随访 术后定期随访至今,未见复发。
MDT讨论荟萃
新辅助治疗在局部进展期胃癌中的应用
MAGIC研究是最具代表性的、大型Ⅲ期围手术期化疗的临床试验,其结果显示,对于局部进展期胃癌,术前应用新辅助化疗可降低肿瘤分期,提高手术根治率,并提高患者总生存率。
该患者曾行毕罗氏I式吻合术,局部解剖结构改变,邻近重要大血管及胆总管结构紊乱,超声内镜显示肿瘤组织与周围组织结构分界不清,因此直接手术风险较大且根治性手术(R0)切除率低,推荐进行术前新辅助治疗。新辅助治疗又分为新辅助化疗和新辅助放化疗,根据患者的一般状况、局部分期和既往手术史进行临床决策。
根据该患者年龄及既往手术史,同步放化疗副反应较大,且残胃癌异常局部解剖结构可能进一步加重同步放化疗后手术相关并发症。因此多学科(MDT)讨论认为,该患者应选择术前新辅助化疗。
胃癌新辅助治疗方案的选择
根据MAGIC临床研究,ECF(表柔比星+顺铂+氟尿嘧啶)方案目前被认为是循证医学证据最为充分的术前新辅助化疗方案。但是,由于大量临床试验已经证实铂类、紫杉醇类、氟尿嘧啶类药物应用于晚期胃癌一线治疗取得不亚于ECF方案的疗效,因此新辅助治疗方案也可考虑使用此类药物的联合方案。
新辅助化疗的目的在于将不能手术或手术困难的局部进展期胃癌转变为可手术切除,应把握好术前化疗的机会,承担一定的治疗毒性风险,选择疗效相对较好的化疗方案以创造较高的治疗有效率。
作为唯一批准应用于晚期胃癌治疗的靶向药物,联合曲妥珠单抗化疗可显著提高HER2阳性患者的治疗有效率,并在国际多中心Ⅲ期临床研究TOGA试验中得到证实,为更好地提高治疗有效率,在新辅助化疗基础上加用曲妥珠单抗是合理的。
最终,经MDT讨论,为该例HER2阳性患者选择了XELOX联合曲妥珠单抗的方案。
如何选择胃癌术后辅助治疗方案
胃癌术后辅助治疗通常取决于术后病理的TNM分期。但对于曾接受新辅助化疗的患者,由于可能使部分肿瘤达到降期,术后病理分期并不能很好地体现患者原本的肿瘤分期并指导预后,因而,术前分期作为术后辅助化疗的依据更为合理。对于新辅助治疗有效的患者,术后往往沿用原方案进行辅助治疗,但是靶向药物应用于术后辅助治疗目前尚无相关临床试验报道,因此并不推荐应用于术后辅助治疗。
目前,已有CLASSIC研究和ACTS-GC研究结果证实,胃癌术后接受XELOX方案或S1单药辅助治疗,可显著延长无病生存和总生存。对于该例患者,由于术前术后分期均为ⅢB期,理论上应接受XELOX方案术后辅助化疗,但患者术后体质差、并发症多,无法耐受原方案治疗,经MDT讨论给予单药S1辅助治疗。
本例患者特点为高龄、残胃癌T4b期、毕罗氏Ⅰ式吻合术后、HER2阳性,其中大部分因素对于胃癌治疗来说都是难点,特别是直接手术风险较大,且R0切除机会较小。但在经历了多学科讨论后,为患者选择了新辅助化疗和靶向治疗。虽然新辅助化疗并没有使该患者达到降期,但肿瘤范围的显著缩小也为手术的完整切除创造了机会。此外患者术后辅助治疗时间较短且使用药物仅为单药,说明患者无病生存期的显著获益(超过23个月)主要与新辅助化疗有关。
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言









#老年男性#
46
#多学科#
51
#残胃癌#
49