NKTR-214联合Opdivo治疗黑色素瘤的两项III期研究,结果失败(PIVOT IO-001)
2022-04-02 网络 网络
基于2019年美国临床肿瘤学会(ASCO)年会上公布的正在进行的I/II期临床研究PIVOT-02的转移性(IV期)黑色素瘤患者研究数据。结果显示,截止2019年3月29日,中位随访12.7个月,接受
基于2019年美国临床肿瘤学会(ASCO)年会上公布的正在进行的I/II期临床研究PIVOT-02的转移性(IV期)黑色素瘤患者研究数据。结果显示,截止2019年3月29日,中位随访12.7个月,接受NKTR-214联合Opdivo免疫组合治疗的38例疗效可评估患者中,总缓解率(ORR)为53%(20/38)、完全缓解率(CR)为34%(13/38)、疾病控制率(DCR:CR+PR+SD,完全缓解+部分缓解+疾病稳定)为74%。在这一亚组中,有53%的患者表现出对治疗的反应,包括肿瘤环境被认为是最不利的参与者——没有PD-L1和T细胞水平较低。
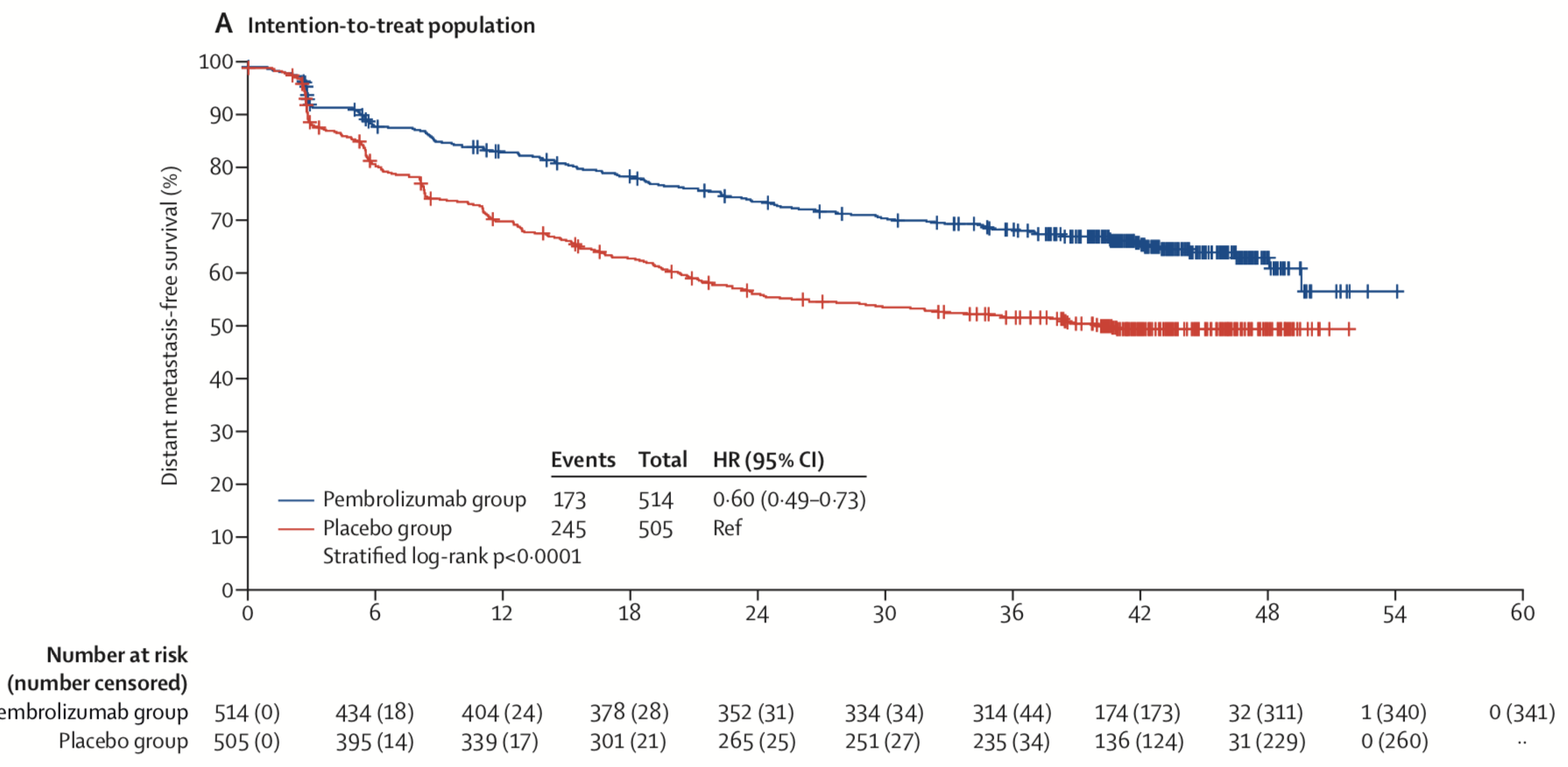
3月14日,百美施贵宝和 Nektar Therapeutics 联合宣布了bempegaldesleukin (NKTR-214)联合纳武利尤单抗相较于纳武利尤单抗单药在先前未经治疗的不可切除或转移性黑色素瘤的临床III期研究(PIVOT IO-001)首次数据分析结果。结论指出,经盲态独立中央审查 (BICR) 评估,该研究未达到无进展生存期和客观缓解率的主要终点,总生存期作为第一次中期分析中的第三个主要终点也不符合统计学意义。受此消息影响,Nektar股价当天下跌超过60%,收于4.16美元。
Bempegaldesleukin (BEMPEG/NKTR-214) 是一种免疫刺激性 IL-2 细胞因子前药,经过工程化改造,由平均与六个聚乙二醇 (PEG) 链偶联的 IL-2 组成,旨在通过结合 IL-2Rβγ 受体而不结合抑制免疫的调节性T细胞IL-2Rαβγ受体,提供快速和持续的信号传导,选择性刺激和扩增特定的抗癌T细胞和自然杀伤 (NK) 细胞。同时,NKTR-214也被设计为通过其PEG 链的缓慢释放来增加 IL-2 的半衰期(~20 小时),从而实现持续(超过3周)激活IL-2途径,以减少给药频率。

此外,基于独立数据监测委员会 (DMC)对PIVOT IO-001研究的审查结果,两家公司还决定停止招募并揭盲正在进行的辅助性黑色素瘤临床III期PIVOT-12研究,该研究旨在评估在高复发风险患者中完全切除黑色素瘤后,NKTR-214联合纳武利尤单抗相较于单独使用纳武利尤单抗的辅助免疫治疗功效。
NKTR-214最初由Nektar Therapeutics开发,百时美施贵在2018年以18.5亿美元首付款(含股权投资)签署合作开发协议,Nektar股价随后也一度飙升至108美元。尽管NKTR-214和纳武利尤单抗联用曾在早期研究中显示对皮肤癌、肾癌和膀胱癌的治疗响应,但这些研究并没有设置对照组,也使得NKTR-214在纳武利尤单抗基础上能够增加多少临床益处变得扑朔迷离,在这个基础上贸然推进至III期临床自然也就增添了不确定性。不过,两家公司决定继续推进在肾细胞癌和膀胱癌中的相关临床探索,包括III期临床。
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言









#III期研究#
69
#色素#
70
#III#
62
#NKT#
72
#NKTR-214#
67
#Opdivo#
61
#黑色素#
47
#黑色素#
61
#III期#
79
失败是成功之母
74