Lancet Oncol:在晚期肾细胞癌患者中,纳武利尤单抗单药或联合纳武利尤单抗和伊匹木单抗作为免疫治疗增敏的效果评估(TITAN-RCC 研究)
2024-02-27 daikun MedSci原创 发表于上海
该研究旨在评估在中高危转移性肾细胞癌患者中,纳武利尤单抗单药治疗以及纳武利尤单抗联合伊匹木单抗作为纳武利尤单抗单药治疗无应答后的免疫治疗增强剂的疗效和安全性,增强治疗可提高客观反应率。
纳武利尤单抗和伊匹木单抗的联合使用已被批准作为中高危转移性肾细胞癌的一线治疗方案,此外,纳武利尤单抗单药治疗被批准作为所有风险组转移性肾细胞癌的二线治疗方案,然而,在一线治疗中,与纳武利尤单抗单药治疗相比,纳武利尤单抗和伊匹木单抗联合使用疗效更好,但毒性也更大,因此,该研究旨在评估在中高危转移性肾细胞癌患者中,纳武利尤单抗单药治疗以及纳武利尤单抗联合伊匹木单抗作为纳武利尤单抗单药治疗无应答后的免疫治疗增强剂的疗效和安全性。

方法
这是一项多中心、单臂、II期临床试验,共纳入207例患者,患者分为两组,未治疗的一线组和接受过一种系统性治疗(抗血管生成或坦罗莫司)的二线组,一线组109例,二线组98例,所有患者首先接受纳武利尤单抗诱导治疗,240mg静脉注射,每2周一次,持续16周,根据疗效评估结果,无应答者接受纳武利尤单抗联合伊匹木单抗增强治疗,剂量为纳武利尤单抗 3mg/kg和伊匹木单抗 1mg/kg,每3周一次,共2-4次,主要终点为确认的客观反应率。
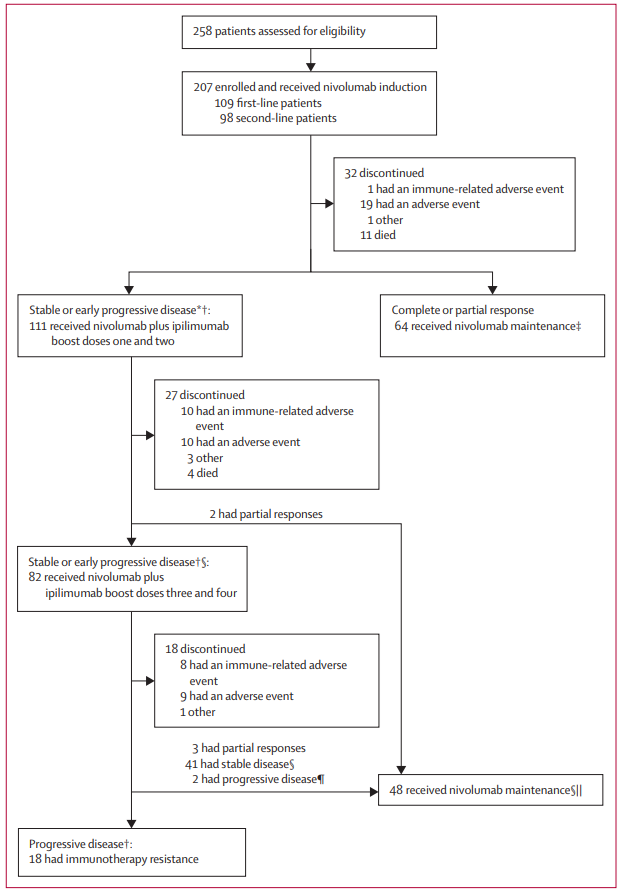
研究结果
一线组共有39例(36%)患者获得确认的客观反应,二线组有31例(32%)患者获得确认的客观反应,一线组中纳武利尤单抗诱导治疗后无应答者中,有16%对增强治疗有客观反应;二线组中纳武利尤单抗诱导治疗后无应答者中,有17%对增强治疗有客观反应,一线组中位无进展生存期6个月,二线组3.7个月,一线组中位总生存期36.1个月,二线组33.7个月。
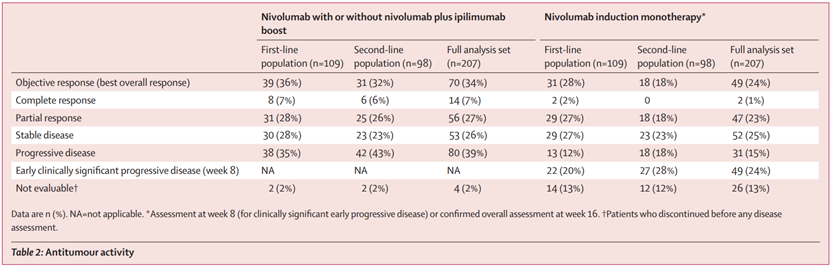

安全性
该研究方案最常见的严重不良反应为脂肪酶升高(7%)、腹泻(6%)和结肠炎(6%),共3例治疗相关死亡,一线组2例,二线组1例,其中,一线组1例可能为缺血性中风,1例为呼吸衰竭;二线组1例为肺炎,最常见的任何等级治疗相关不良事件包括乏力(37%)、瘙痒(30%)、腹泻(25%)、皮疹(20%)、食欲减退(13%)、脂肪酶升高(11%)和恶心(11%),治疗相关不良事件导致治疗延迟的占35%,该研究的安全性特征与纳武利尤单抗和伊匹木单抗联合使用的情况一致,提示联合使用具有较好的安全性。

结论
纳武利尤单抗诱导治疗联合增强治疗可提高客观反应率,但整体疗效和毒性似乎劣于批准的纳武利尤单抗联合伊匹木单抗一线方案,增强治疗似乎可提高客观反应率,整体生存期似乎优于纳武利尤单抗单药治疗,对于纳武利尤单抗治疗后进展的患者,纳武利尤单抗联合伊匹木单抗可作为挽救策略,该研究为进一步评估伊匹木单抗与纳武利尤单抗联合治疗转移性肾细胞癌提供了数据支持。
原始出处
Grimm M-O, et al. 2023. Tailored immunotherapy approach with nivolumab with or without nivolumab plus ipilimumab as immunotherapeutic boost in patients with metastatic renal cell carcinoma (TITAN-RCC): a multicentre, single-arm, phase 2 trial. The Lancet Oncology 24:1252-1265.
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言















#肾细胞癌# #纳武利尤单抗# #伊匹木单抗#
57