JCO:北京大学齐长松团队发现CAR-T细胞治疗胰腺癌,疾病控制率达70.8%
2024-06-22 iNature iNature 发表于威斯康星
以评估CT041在既往治疗过的胰腺癌(PC)患者中的作用(CT041是一种嵌合抗原受体(CAR)修饰的T细胞疗法,特异性靶向实体瘤中的CLDN18.2)。
最致命、最难发现、扩散最快,让胰腺癌成了令人生畏的“癌中之王”。近年来,胰腺癌的发病率在国内外均呈明显的上升趋势。中国国家癌症中心2021年统计数据显示,胰腺癌位居我国男性恶性肿瘤发病率的第 7 位,女性恶性肿瘤发病率的第11位,位列恶性肿瘤相关死亡率的第 6 位。
随着早诊意识和手段的增强以及医学技术的进步,胰腺癌5年生存率有所改观。2000年左右统计数据显示,胰腺癌患者的5年生存期不到5%,2020年,这一数据已接近9%,胰腺癌传统的治疗方式依然有限。
2024年5月24日,北京大学齐长松团队在Journal of Clinical Oncology(IF=45)在线发表题为“Safety and Efficacy of CT041 in Patients With Refractory Metastatic Pancreatic Cancer:A Pooled Analysis of Two Early-Phase Trials”的研究论文,该研究报告了两项探索性临床试验的汇总分析结果,以评估CT041在既往治疗过的胰腺癌(PC)患者中的作用(CT041是一种嵌合抗原受体(CAR)修饰的T细胞疗法,特异性靶向实体瘤中的CLDN18.2)。

该研究联合队列包括24例晚期PC患者。其中5例(20.8%)患者曾接受过1线治疗,19例(79.2%)患者接受过≥2线治疗。最常见的治疗中出现的3级或以上不良事件是预处理相关的血液学毒性。细胞因子释放综合征(CRS)和胃肠道紊乱是报道最多的1级或2级不良事件。
总有效率为16.7%,疾病控制率为70.8%。输注后的中位无进展生存期(mPFS)为3.3个月(95% CI, 1.8至6.2),中位总生存期(mOS)为10.0个月(95% CI, 5.5至17.6)。中位缓解持续时间(mDoR)为9.5个月(95% CI, 2.6至未达到),12个月时DoR率为50% (95% CI, 5.8至84.5)。取得部分缓解/病情稳定的患者的mPFS (6.0 vs 1.0个月,P < 0.001)和mOS (17.6 vs 4.0个月,P < 0.001)较进展性疾病组延长。17例(70.8%)患者的CA19-9水平降低了至少30%。在既往治疗进展后的转移性PC患者中,CT041显示出可耐受的安全性和令人鼓舞的抗癌疗效信号。
胰腺癌(PC)由于其高侵袭性、易转移和复发,仍然是世界范围内预后差的最致命的肿瘤之一,这一事实突出了对替代治疗方式的需求吉西他滨为基础的治疗方法,包括吉西他滨加nab-紫杉醇(GnP)和氟尿嘧啶、亚叶酸钙、伊立替康和奥沙利铂(FOLFIRINOX),多年来一直是转移性PC的标准一线治疗方法。对于二线治疗,在吉西他滨或GnP治疗失败后,建议使用nal-IRI加氟尿嘧啶(FU)/亚叶酸钙(LV)和FOLFIRINOX。传统治疗方法在PC中的失败证明了对替代疗法的探索。
嵌合抗原受体修饰的T细胞作为一种新的免疫治疗策略,在治疗血液系统恶性肿瘤方面取得了突破性进展。然而,在实体肿瘤中应用CAR-T细胞疗法仍然存在挑战。Claudin18异构体2 (Claudin18.2或CLDN18.2)是Claudin家族的成员,病理状态下在包括PC在内的癌组织中以紧密连接结构在细胞膜上表达。CLDN18.2在原发性PC标本中阳性率为59.2%,高表达(染色强度≥12)的比例为54.6%。基于CAR-T疗法的治疗潜力和CLDN18.2在PC中的表达,CLDN18.2靶向CAR-T细胞(CTo41)进入临床试验。
当前汇总分析中描述的CT041在PC患者中的安全性与初步分析中报道的延长随访没有明显变化。注入后的CAR-T细胞被广泛激活,与靶肿瘤细胞上的抗原结合,导致大量炎症细胞因子的释放。在正常组织中,CLDN18.2只存在于胃粘膜细胞的紧密连接中,然而,只有1例患者发生3级胃粘膜糜烂,报道的粘膜损伤事件大多数为1级或2级,这是可控的。该报告显示,CTo41在CLDN18.2阳性PC患者中耐受性良好。
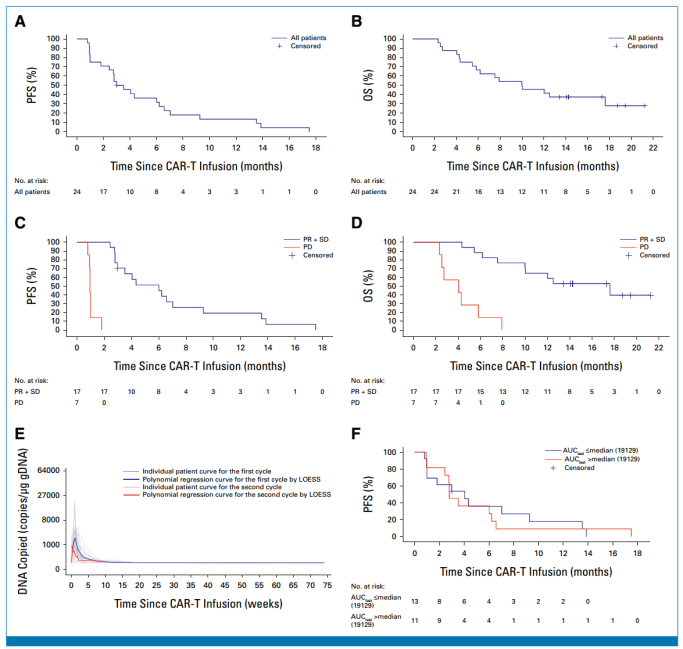
CAR-T细胞扩增与剂量、输注周期和反应的相关性
图|源Journal of Clinical Oncology
目前的汇总分析结果似乎在批准的二线治疗方案的结果背景下是有希望的。在先前接受过CLDN18.2阳性PC治疗的患者中,CT041显示出具有临床意义的抗肿瘤活性(mPFS 3.3个月,mOS 10.0个月)。缓解是持久的,mDoR为9.5个月,12个月的DoR率为50%。尽管该队列中的大多数患者接受了≥2线治疗,但CT041治疗显示出良好的OS数据。值得注意的是,在接受CT041作为二线治疗的患者中,ORR和mPFS达到40.0%和7.0个月,这对于CT041在这种情况下早期使用的更多研究是令人鼓舞的。
在针对间皮素特异性的CAR-T I期试验中,6名转移性PC患者入组。根据RECIST 1.1标准,两名患者的最佳总体反应是SD。有趣的是,通过氟脱氧葡萄糖(FDG)正电子发射断层扫描(PET)-计算机断层扫描(CT)监测肿瘤的代谢活性体积(MAV)显示,在CAR-T细胞输注1个月后,3例患者的总MAV保持稳定,1例患者的总MAV下降了69.2%,所有肝脏病变的FDG摄取完全减少。在该报告中,也发现了部分患者的病变体积增大,但CT扫描肿瘤密度降低,CA19-9降低的现象。
结 语
本研究数据显示,CLDN18.2 CAR-T细胞治疗在大量预处理的CLDN18.2阳性胰腺癌患者中具有探索性的有希望的抗癌活性。该方案改善了OS、PFS、CA19-9反应和DCR,并具有预期的安全性和一般可控的不良事件。这项研究的结果为研究与疗效相关的潜在生物标志物提供了理论依据,并保证未来有其他潜在的增强治疗。
参考文献:
https://ascopubs.org/doi/10.1200/JCO.23.02314
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言

















#胰腺癌# #CAR-T细胞治疗#
103