FDA扩大了Lynparza(奥拉帕尼)的适应症范围
2022-03-12 Allan MedSci原创
与安慰剂相比,Lynparza组患者的死亡风险降低了 32%。
乳腺癌是由乳房组织发展成的癌症。乳腺癌的征象包括乳房肿块、乳房形状改变、皮肤凹陷、乳头分泌物或是皮肤出现红色鳞屑状斑块。而出现远端转移的病患,可能会有骨痛、淋巴结肿大、呼吸困难或黄疸的情形。大约5至10%的病例是因父母亲的遗传而发生,这些遗传因子包含了BRCA1、BRCA2与其他因子。
近日,FDA 扩大了对阿斯利康(AstraZeneca)和默克公司(Merck & Co.)的 Lynparza(奥拉帕尼)的批准范围,允许对已经接受过化疗的 BRCA 突变、HER2 阴性、高风险乳腺癌的患者进行辅助治疗。据两家公司称,这一决定使口服 PARP 抑制剂 Lynparza(奥拉帕尼)成为第一个获批的针对早期乳腺癌 BRCA 突变的药物。
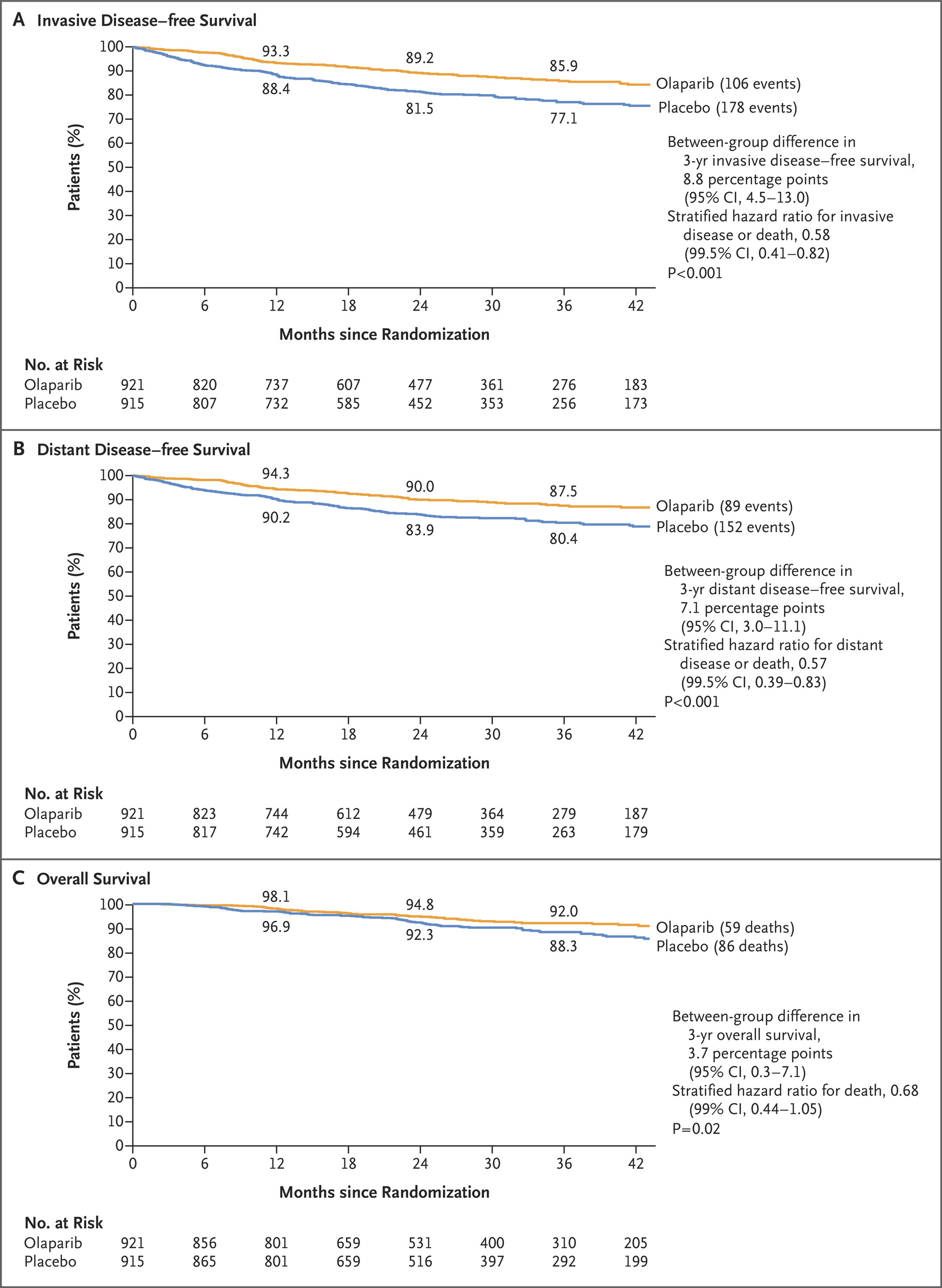
该批准得到了 III 期 OlympiA 试验结果的支持,该试验也发表在 NEJM 上。在这项研究中,与安慰剂相比,Lynparza(奥拉帕尼)使浸润性乳腺癌复发、二次癌症或死亡的风险降低了 42%,实现了无浸润性无病生存的主要终点。
关于总生存期 (OS) 的关键次要目标,结果显示,虽然 Lynparza 的 3 年估计 OS 高于安慰剂,但在中期分析中差异不显著。然而,近日两家公司报告了更新的 OlympiA 结果,其中 Lynparza 确实显示出显著且具有临床意义的 OS 改善,与安慰剂相比,Lynparza组患者的死亡风险降低了 32%。
Lynparza 已经在美国、欧盟、日本和其他几个国家获得批准,用于先前接受过化疗的 gBRCAm、HER2 阴性、转移性乳腺癌患者。阿斯利康公布的 Lynparza 在 2021 年第四季度的销售额为 10 亿美元,比去年同期增长 25%。
原始出处:
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言











#奥拉帕利#
90
#FDA#
95
好东西,谢谢分享
51
#适应症#
67