Algernon已提交Pre-IND申请,以进行Ifenprodil治疗新冠肺炎的临床试验
2020-03-14 Allan MedSci原创
临床阶段药物开发公司Algernon Pharmaceuticals宣布,已向美国FDA提交Pre-IND申请。
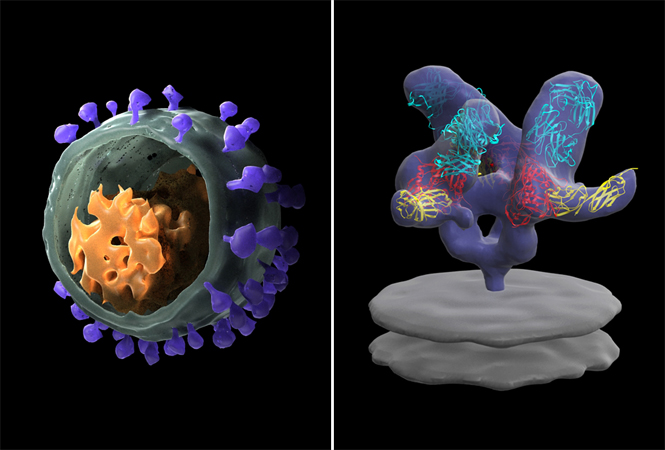
临床阶段药物开发公司Algernon Pharmaceuticals宣布,已向美国FDA提交Pre-IND申请。这将启动与美国FDA的正式沟通,以推进NP-120(Ifenprodil)治疗COVID-19感染相关的急性肺损伤(ALI)和急性呼吸窘迫综合征。
在申请中,Algernon已就使用新的注射和缓释制剂提供了指导。这项申请文件还包括对扩展访问路径(也称为“同情使用”路径)的说明。
最近的一项独立研究发现,在NP-120(Ifenprodil)治疗亚洲H5N1病毒感染的小鼠的研究中,NP-120(Ifenprodil)显著降低了ALI并将存活率提高了40%。亚洲H5N1病毒是迄今为止已知最致命的流感病毒,死亡率超过50%。另一项先前研究还显示,该药物可延长受感染小鼠在缺氧(低氧)条件下的生存期。
原始出处:
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言















#GER#
60
#IND#
51
#lgE#
89
#PRO#
53
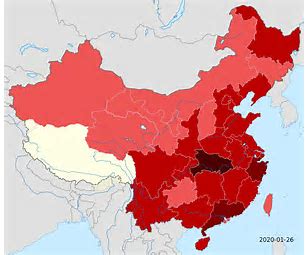
新冠肺炎,疫情何时才能消失
74