Adv Sci:中山大学张春宇/姚书忠/王伟发现脂肪酸氧化通过乙酰辅酶A介导的细胞干性宫颈癌淋巴结转移
2024-04-16 iNature iNature 发表于陕西省
该研究发现淋巴转移性CCa细胞对葡萄糖和糖酵解的依赖性降低,但脂肪酸氧化(FAO)增加。抑制肉碱棕榈酰转移酶1A(CPT1A)显著损害棕榈酸酯诱导的细胞干性。
越来越多的证据表明,癌细胞的代谢重编程支持肿瘤转移期间的能量和代谢需求。然而,尚不清楚宫颈癌(CCa)淋巴结转移(LNM)背后的代谢变化机制。
2024年3月23日,中山大学张春宇、姚书忠及王伟共同通讯在Advanced Science 在线发表题为“Fatty Acid Oxidation Supports Lymph Node Metastasis of Cervical Cancer via Acetyl-CoA-Mediated Stemness”的研究论文,该研究发现淋巴转移性CCa细胞对葡萄糖和糖酵解的依赖性降低,但脂肪酸氧化(FAO)增加。抑制肉碱棕榈酰转移酶1A(CPT1A)显著损害棕榈酸酯诱导的细胞干性。
从机制上讲,FAO衍生的乙酰辅酶A增强了干性基因启动子中H3K27乙酰化(H3K27Ac)的修饰水平,在富含脂质的淋巴结环境中增强了细胞干性和淋巴结转移。CPT1A功能的遗传和药理学丧失明显抑制了CCa细胞在肿瘤引流淋巴结中的转移定植。总之,上述发现提出了一种通过靶向FAO治疗CCa和淋巴结转移患者的有效方法。

宫颈癌(CCa)是全球最常见的女性癌症之一,2020年新增病例60.4万例,死亡34.2万例。由于骨盆的特殊解剖结构,宫颈癌细胞主要通过淋巴管扩散到盆腔和主动脉旁淋巴结。患有CCa和淋巴结转移(LNM)的患者复发率较高,5年总生存率较低。2018年国际妇科和产科联合会(FIGO)也建议无论原发肿瘤的大小和范围如何,CCa和LNM患者应诊断为IIIc期,表明LNM状态在CCa患者的预后中具有关键作用。因此,有必要阐明LNM的潜在分子机制,并探索潜在的CCa治疗靶点。
代谢重编程是恶性肿瘤的标志,使肿瘤细胞能够解决不同转移阶段的代谢问题。与代谢可塑性相关的一个关键概念是转移部位的营养可用性,能够解释为什么肿瘤细胞更喜欢转移到特定器官而不是其他器官。继发部位的葡萄糖、谷氨酰胺、丙酮酸和脂肪酸等特定营养素在转移细胞播种和定植时支持其增殖。最近,脂肪酸氧化(FAO)和脂质代谢因其对各种类型癌症(包括宫颈癌)进展的关键作用而受到广泛关注。据报道,溶质载体有机阴离子转运蛋白家族成员1B3(SLCO1B3)可增强晚期浆液性卵巢癌(HGSOC)的FAO,促进其转移。该团队之前的研究发现,脂肪酸结合蛋白5(FABP5)在LNM的宫颈癌中显著上调,并且FABP5过表达通过激活NF-κB信号通路显著促进淋巴结转移。然而,尚不清楚宫颈癌发生淋巴结转移的作用机制。
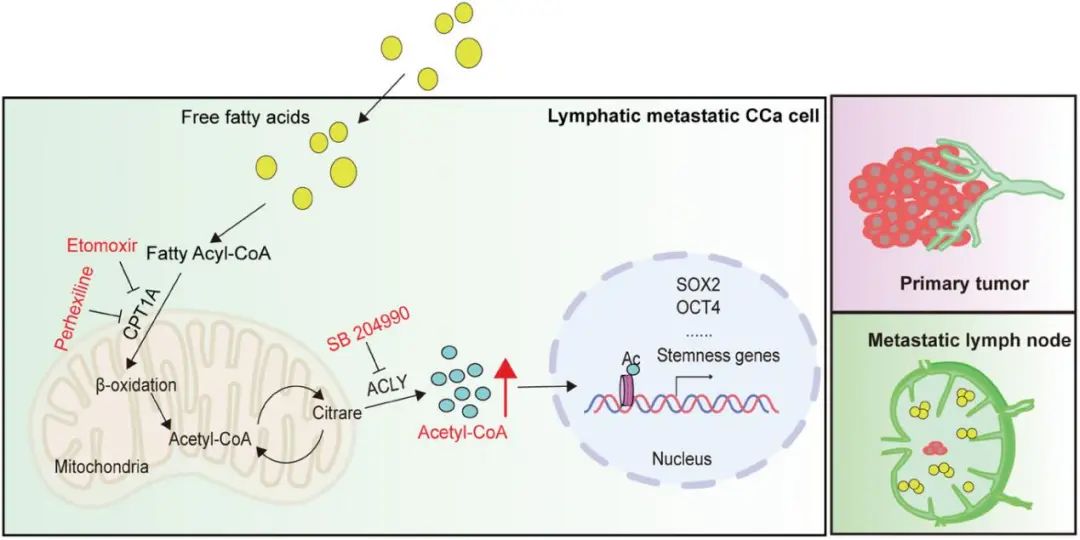
FAO衍生的乙酰辅酶A增强干性基因启动子H3K27乙酰化修饰水平,增加了富含脂质的淋巴结环境中细胞干性和淋巴结转移(摘自Advanced Science )
该研究发现了由FAO介导的CCa转移的潜在机制。作者发现FAO增强是转移性CCa细胞的新代谢标志,且CPT1A基因丢失和药理学抑制都损害了LNM。具体而言,FAO调控H3K27ac干性轴的激活,该轴对CCa细胞定植和淋巴结生长至关重要。总之,上述内容表明,CPT1A和FAO是代谢可塑性的核心调控因子,支持CCa细胞干性和LNM,也是预防宫颈癌发生淋巴结转移的潜在靶点。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202308422
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言















该研究发现了由FAO介导的CCa转移的潜在机制。作者发现FAO增强是转移性CCa细胞的新代谢标志,且CPT1A基因丢失和药理学抑制都损害了LNM。
33
#宫颈癌# #乙酰辅酶A#
31