NEJM:礼来Aβ抗体二期临床结果公布:达到主要终点,错失次要终点
2021-03-14 haibei MedSci原创
2021年3月13日,礼来的Aβ抗体Donanemab的二期临床结果在新英格兰杂志被公布(临床编号:NCT03367403)。
2021年3月13日,礼来的Aβ抗体Donanemab的二期临床结果在新英格兰杂志被公布(临床编号:NCT03367403)。阿尔茨海默病的一个重要标志是淀粉样蛋白-β(Aβ)肽的积累。Donanemab靶向Aβ的特定形式,即N端第3位焦谷氨酸化的Aβ(N3pG-Aβ),N3pG-Aβ更容易聚集,是备受关注的AD治疗靶点。该临床试验是研究Donanemab治疗早期阿尔茨海默病的效果。

礼来对早期症状性阿尔茨海默病患者进行了Donanemab的二期试验,这些患者在正电子发射断层扫描(PET)上有tau和淀粉样蛋白沉积。患者以1:1的比例随机分配,接受Donanemab(前三次剂量为700mg,此后为1400mg)或安慰剂治疗,每4周静脉注射一次,持续72周。
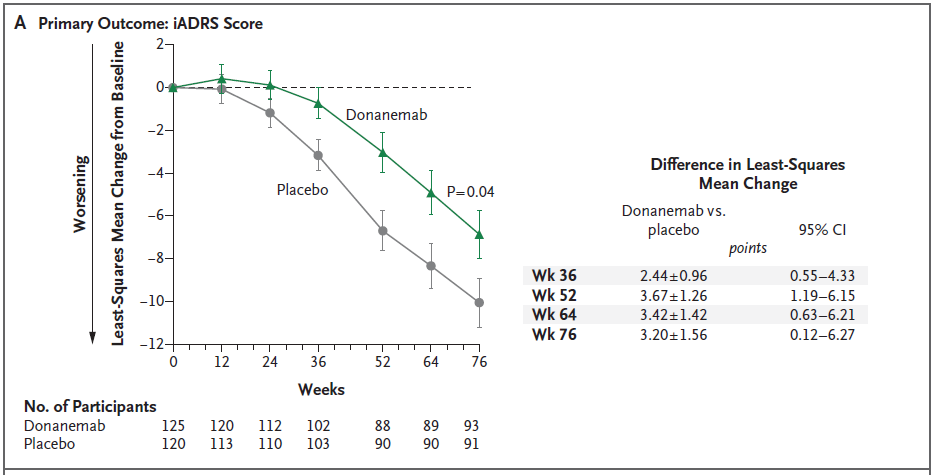
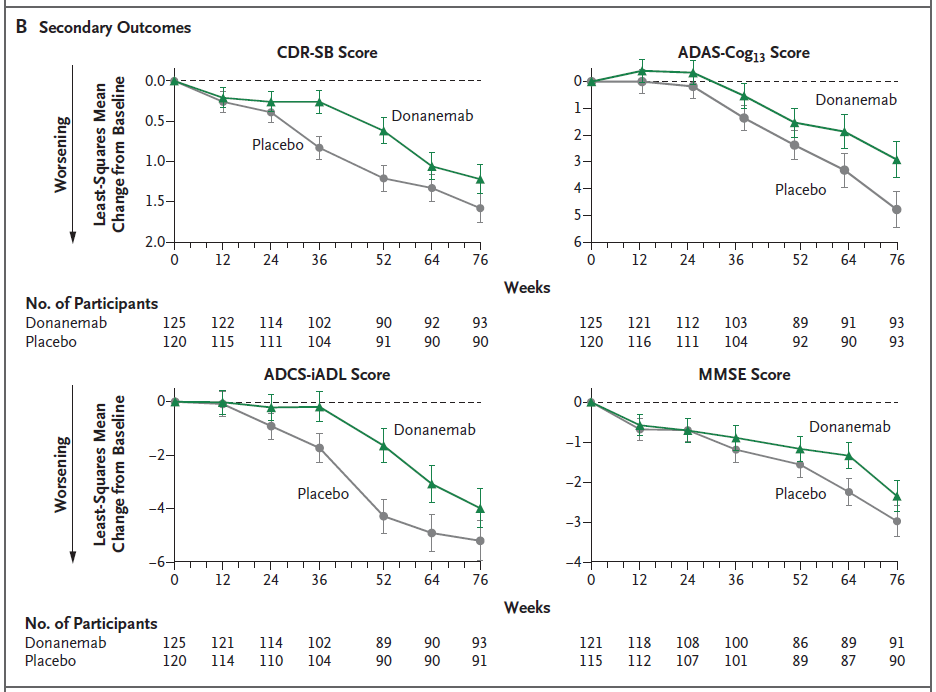
主要结果是76周时阿尔茨海默病综合评定量表(iADRS;范围,0~144,分数越低表示认知和功能损害越大)上的分数与基线的变化。次要结果包括临床痴呆评分量表-评分加和(CDR-SB)、阿尔茨海默病评估量表13项认知子量表(ADAS-Cog13)、阿尔茨海默病合作研究-日常生活活动量表(ADCS-iADL)和迷你精神状态检查(MMSE)的评分变化,以及PET上淀粉样蛋白和tau负担的变化。
在该研究中,共有257名患者入组;131人被分配接受Donanemab治疗,126人接受安慰剂。两组的基线iADRS评分均为106分。76周时iADRS评分与基线的变化为:Donanemab为-6.86,安慰剂为-10.06(差异,3.20;95%置信区间,0.12~6.27;P=0.04),具有显著差异。
然而,大多数次要结果的统计没有实质性差异。此外,Donanemab治疗可能与淀粉样蛋白相关的脑水肿或积液有关(大多无症状)。
因此,在早期阿尔茨海默病患者中,Donanemab治疗组在76周时的认知和日常生活活动能力的综合评分优于安慰剂组,但次要结果参差不齐。研究Donanemab在阿尔茨海默病中的疗效和安全性还需要更长时间和更大规模的试验。
原始出处:
Mark A. Mintun et al. Donanemab in Early Alzheimer’s Disease. NEJM (2021).
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言











#二期临床#
57
#临床结果#
76
#结果公布#
65
#主要终点#
57
#Aβ#
87
顶刊就是顶刊,谢谢williamhill asia 带来这么高水平的研究报道,williamhill asia 科里同事经常看williamhill asia ,分享williamhill asia 上的信息
86