3月25日,CDE官网显示住友制药SEP-363856片临床申请已获国家药监局受理。
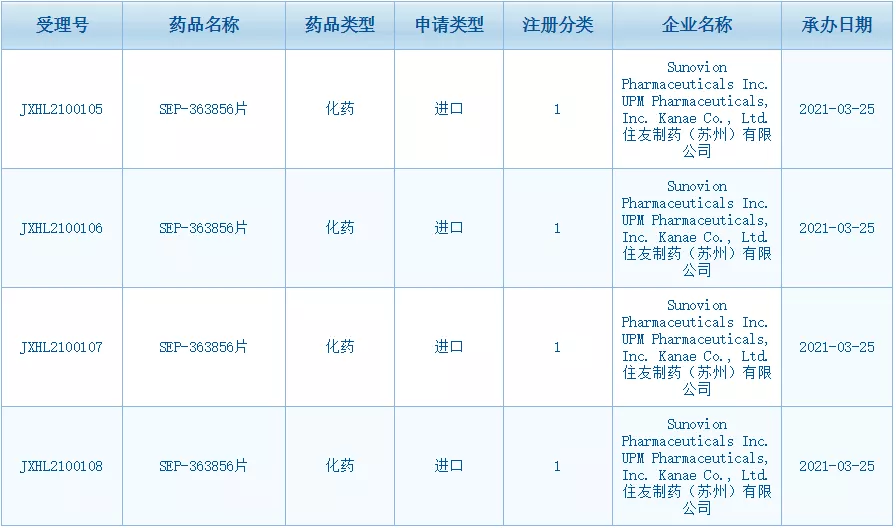
SEP-363856是一种新型的痕量胺相关受体1 (TAAR1)和5-羟色胺1A (5-HT1A)受体激动剂。与目前临床使用的非典型抗精神分裂症药物不同,SEP-363856不与多巴胺2 (D2)或5-HT2A (5-HT2A)受体结合,因此不会导致D2相关锥体外系反应和内分泌相关副作用。

2020年4月,SEP-363856治疗精神分裂症的一项代号为SEP361-201的关键临床研究结果发表在了《新英格兰医学杂志》上。该项研究评估了SEP-363856治疗精神分裂症急性加重成人患者的疗效。试验中,患者按1:1的比例随机分配,每日接受一次SEP-363856(50或75 mg)或安慰剂治疗,持续4周。主要终点为PANSS总评分较基线的变化;次要终点有8个,包括临床总体印象-严重度量表(CGI-S)和简短阴性症状量表(BNSS)评分较基线的变化。
研究结果显示,第4周时SEP-363856组患者PANSS总评分较基线下降17.2,安慰剂组这一数值为9.7(p=0.001)。CGI-S评分结果显示,SEP-363856组患者疾病的总体严重程度较安慰剂组有所改善(p<0.001)并且所有主要的PANSS分量表(阳性、阴性和一般精神病理学症状)评估结果也较安慰剂组有所改善(p<0.02)。

安全性方面,SEP-363856组有7名患者(5.8%)发生严重不良事件,安慰剂组有2名(1.6%)。在整个研究过程中,SEP-363856的耐受性良好,SEP-363856组和安慰剂组的总停药率相似。两组的锥体外系症状发生率以及血脂、糖化血红蛋白和催乳素水平的变化相似。
SEP-363856目前正在进行一项全球性的III期临床(DIAMOND)项目,以评估其针对其它类型精神分裂症的疗效。2019年5月,美国FDA授予了 SEP-363856治疗精神分裂症的突破性疗法资格。
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言











期待上市,广大群众获益
72
#申报#
58
国内什么时候上市呀
80
期待早日上市。
77
#新靶点#
55
#精神分裂#
47
我学到了很多东西谢谢老师
98
好文章!
94