随着免疫治疗不断发展,越来越多研究证明,免疫治疗可以给早期患者带来获益,肺癌围术期免疫治疗的时代已经开启。回顾2023年,众多重磅NSCLC围术期免疫治疗研究数据发表,围术期免疫治疗逐渐呈现出全新的格局,但与此同时,仍有许多临床问题需要进一步探讨和研究,如:哪种治疗模式更优、NSCLC围术期是否有其他可探讨方向、免疫治疗对手术是否有影响等,本期给大家分享围术期免疫治疗模式相关研究进展和临床经验。
1 围术期治疗模式如何选择“夹心面包”模式或成潮流
肺癌围术期治疗经历前期探索阶段后,随着临床经验的不断积累,在治疗模式上已逐渐由单纯的术前新辅助或术后辅助进化为两者结合的围术期治疗模式:新辅助+辅助;从临床梳理的临床研究设计也可以发现,越来越多后期启动的三期研究,是以“夹心面包”的形式开展;从临床发表的数据可以发现,新辅助+辅助的围术期治疗模式确实给患者带来了远期获益,但这并不能说明“夹心面包”模式的围术期治疗方案适合所有患者,究竟哪种围术期治疗模式更优仍然是一个值得深入探讨和研究的科学问题,只能说“夹心面包“模式在临床中的应用越来越广泛。
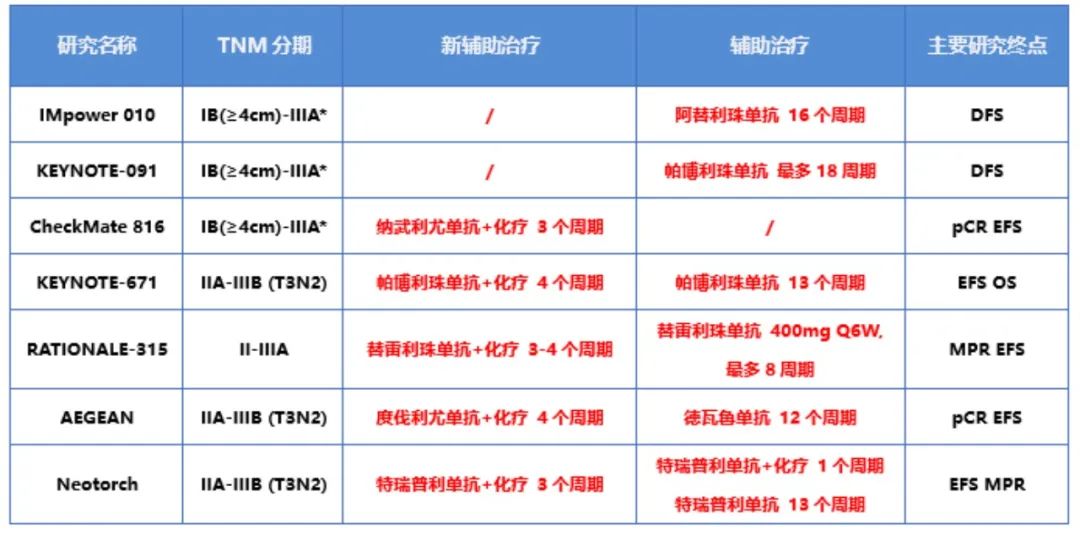
NSCLC相关围术期临床研究设计汇总表
辅助免疫治疗
众所周知,Impower010研究是全球首个针对NSCLC开展的术后免疫辅助研究,研究结果证实[1-2],阿替利珠单抗辅助治疗可以显著提高患者的DFS率,其中2年和3年的DFS均明显高于对照组(74.8% vs. 61.0%, 60.0%vs.48.2%),5年OS率高达84.8%。基于相关研究数据,2023年《CSCO非小细胞肺癌诊疗威廉亚洲博彩公司 》将阿替利珠单抗列入了免疫辅助治疗的I级推荐:用于PD-L1 TC≥1%、经手术切除、以铂类为基础化疗之后的II-IIIA期和IIB(T3N2M0)期NSCLC患者辅助治疗。
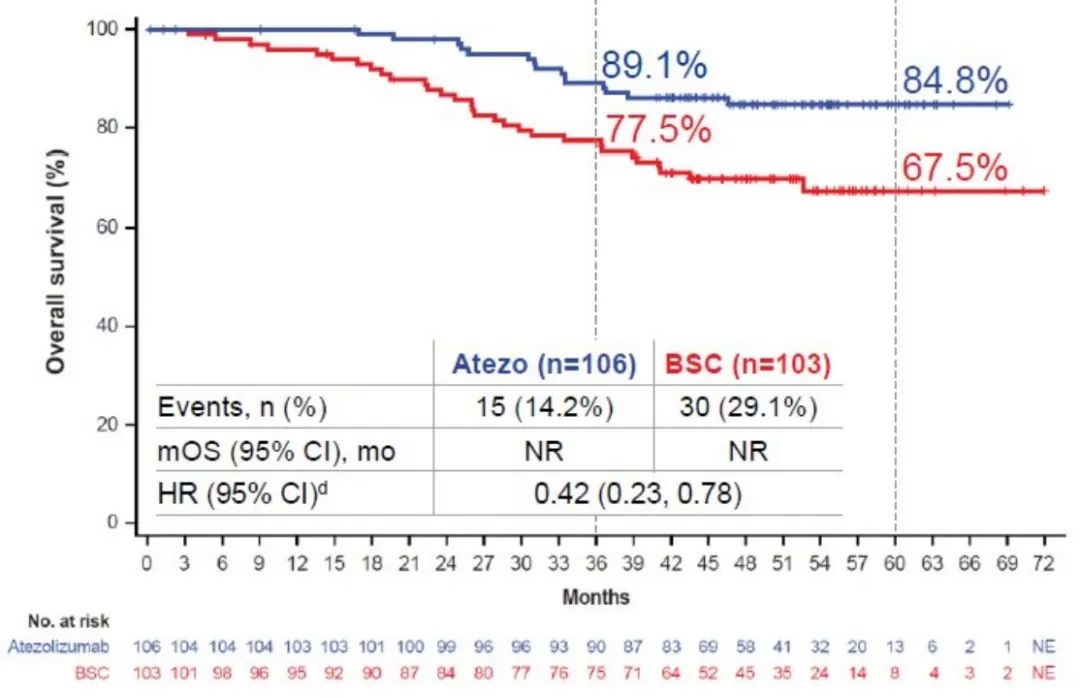
阿替利珠单抗PD-L1 TC≥50%(II-IIIA期)亚组的OS数据(图源2022年WLCL会议)
2023年ESMO-IO公布了KEYNOTE-091最终DFS分析数据3:在IIT人群中:无论PD-L1的表达如何,帕博利珠单抗显著提高了IB(T≥4cm)-IIIA期NSCLC患者的DFS(HR 0.81,95% CI 0.68-0.96)(与二次中期分析数据一致)。然而在PD-L1 TPS≥50%人群中,帕博利珠单抗辅助治疗相比安慰剂治疗,没有显著改善患者DFS(HR 0.83,95% CI 0.59-1.16;p=0.13),这一结果,打破了williamhill asia 对PD-L1高表达免疫疗效更优的认知,那么究竟PD-L1表达是否能预测围手术期免疫治疗患者获益?值得探讨。
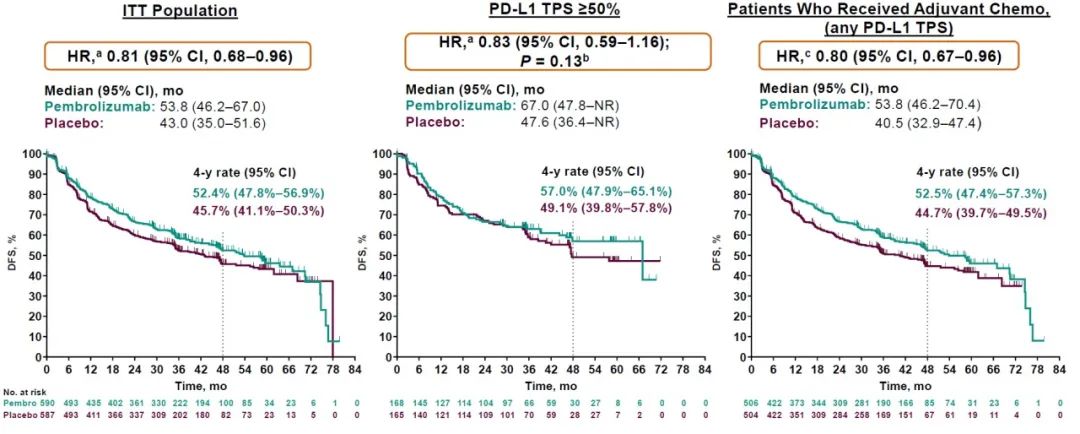
KEYNOTE-091最终DFS分析数据(图源2023年ESMO-IO会议)
新辅助免疫联合化疗
众所周知,CheckMate816是一项针对IB(肿瘤最大径≥4 cm)至IIIA期可切除NSCLC患者开展的III期临床研究[4-6],研究主要终点为pCR和EFS。2021 年AACR公布该研究达到pCR主要终点:纳武利尤单抗联合化疗组pCR率达24.0%,而单纯化疗组仅为2.2%(OR=13.94,99% CI:3.49~55.75,P<0.0001)。
2023 年AACR大会公布了CheckMate816研究中国亚组探索性分析的结果,研究纳入97名中国患者,3年EFS率达到59%(化疗组35%),疾病进展、复发或死亡风险下降达53%。
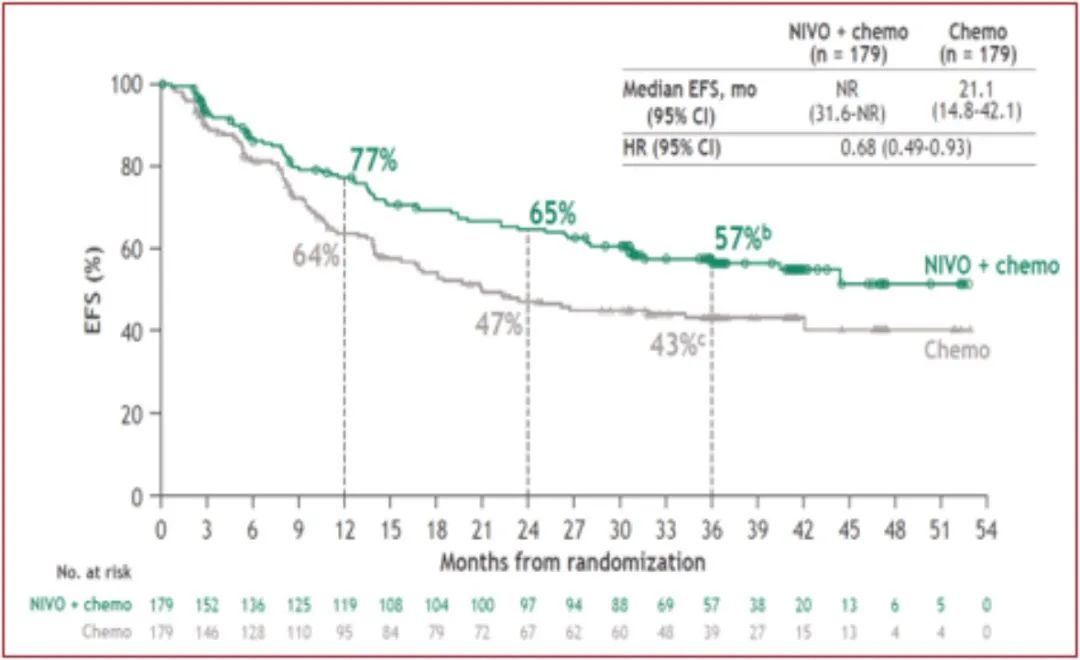
CheckMate 816研究3年随访OS结果(图源2023年ELCC会议)
基于Checkmate-816研究数据,2022年3月,FDA 批准纳武利尤单抗(nivolumab)联合铂类化疗可作为成年可切除(肿瘤 ≥4 cm 或淋巴结阳性)非小细胞肺癌(NSCLC)的新辅助治疗。2023年1月17日,纳武利尤单抗获得NMPA批准新增NSCLC新辅助治疗适应症。
夹心面包模式-新辅助免疫治疗+术后辅助免疫治疗
夹心面包模式以AEGEAN. Neotorch、KEYNOTE-671、RATIONALE-315研究为代表,AEGEAN[7]研究是第一个公布阳性数据的3期临床研究,2022年6月该研究报阳,2023年AACR公布了相关研究结果:度伐利尤单抗+化疗显著提高了患者的pCR率和EFS,试验组对比化疗组pCR率为17.2% vs.4.3%;随后WCLC 更新了新辅助治疗后手术结局相关数据,试验组及对照组的手术切除率分别为80.6%和80.7%;2023年ESMO 公布了ctDNA检测的结果:新辅助治疗可以有效降低ctDNA VAF。基于以上数据,NMPA批准O药新辅助治疗相关适应症。
与此同时,KEYNOTE-671[8-9]于2023年3月1日报阳,2023年ASCO公布了了主要研究终点:帕博利珠单抗联合化疗围术期治疗显著改善患者EFS,死亡风险降低了42%,帕博利珠单抗±化疗新辅助/辅助试验组未达到中位EFS(95%CI, 34.1个月-NR)。2023 ESMO公布了OS阳性结果,中位随访36.6个月,帕博利珠单抗组3年OS率为71.3%,对照组为64.0%。FDA于10月批准了帕博利珠单抗用于II-IIIB期NSCLC患者新辅助、辅助治疗适应症。
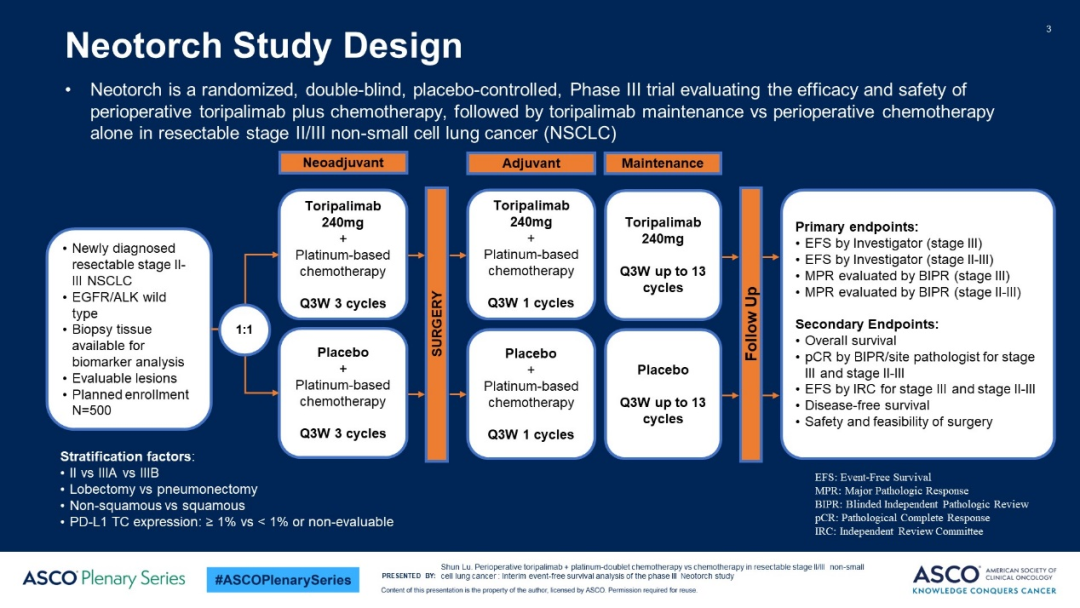
Neotorch研究[10]于2023年ASCO公布了了主要研究终点EFS数据,已获批适应症;RATIONALE-315研究[11]于2023 ESMO上首次公布数据,中位随访16.8个月,替雷利珠单抗+化疗组MPR率达56.2%(P<0.0001),pCR率40.7%(P<0.0001)。
既往针对早期可切除NSCLC患者的围术期治疗方案仅限于化疗,疗效改善有限,2023年可谓NSCLC围术期的大年,随着相关研究数据陆续重磅报道,夹心面包模式越来越多被临床应用。
2 个性化选择治疗方案或许是围术期治疗模式选择的终极答案
截至目前,围术期究竟哪种治疗方案更优并没有确切的答案,如何更好地平衡花费、疗效和安全性仍需更多地临床研究和实践积累找到答案。
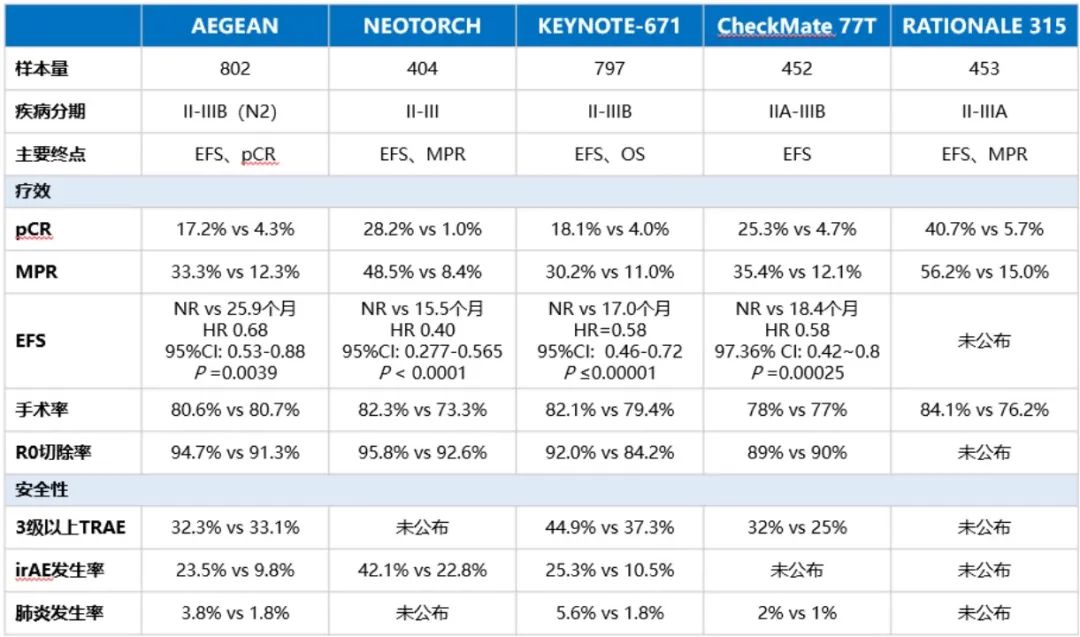
表2:围术期免疫治疗近期研究汇总[7-12]
免疫新辅助治疗,可以刺激机体释放更多抗原,激活机体免疫细胞功能,实现缩瘤降期,提高手术 PCR率,但同时有可能出现纤维化,增加手术难度;免疫辅助治疗,患者可以尽快进行手术,增加患者远期获益,但并不能满足有缩瘤降期患者需求;新辅助+辅助的治疗模式,结合两者优势,缩瘤降期,增加手术机会的同时,增加了患者远期获益,最重要的是,给部分不可手术患者提供了转化治疗的机会和手术可能。
结合当前临床实践经验,更多IIA期NSCLC患者或倾向选择手术+术后辅助免疫治疗的方案;而IIB-III期NSCLC患者,根据实际情况,可考虑新辅助免疫,或“夹心面包”模式,根据患者自身情况,个性化选择治疗方案才是当前最优选择。
综上所述,围手术期免疫治疗在可切除NSCLC中的应用虽然已经取得了显著的进展,但当前还有诸多的临床问题需要进一步探索,如:如何选择围术期治疗模式,如何筛选获益人群,哪些生物标志物可以指导临床获益等等,都需要未来的不断的研究和临床实践积累得出答案,期待未来更多的临床试验结果的公布,给患者带来更精准、更有效的治疗选择,给患者带来更多获益。
参考文献
1.Enriqueta Felip, et al. Atezolizumab (atezo) vs best supportive care (BSC) in stage II-IIIA NSCLC with high PD-L1 expression: Sub-analysis from the pivotal phase III IMpower010 study. Annals of Oncology (2022) 33 (suppl_2): S71-S78.
2.Felip E, Altorki N, Vallieres E, et al. IMpower010: overall survival interim analysis of a phase III study of atezolizumab vs best supportive care in resected NSCLC. Presented at the 2022 World Conference on Lung Cancer; August 6-9, 2022; Vienna, Austria; PL03.09.
3.2023 ESMO IO 120MO
4.Forde P, Spicer J, Lu S, et al. Nivolumab + platinum-doublet chemotherapy vs chemotherapy as neoadjuvant treatment for resectable (IB–IIIA) non-small cell lung cancer in the phase 3 CheckMate 816 trial. AACR 2021.
5.Neoadjuvant nivolumab(N)+platinum-doublet chemotherapy(C)for resectable NSCLC: 3-y update from CheckMate 816. 2023 ELCC. 84MO.
6.Wang CL et al., Poster presentation at the AACR Annual Meeting; April 14–19, 2023; Orlando, FL.
7.Forde P, Spicer J, Lu S, et al. Nivolumab + platinum-doublet chemotherapy vs chemotherapy as neoadjuvant treatment for resectable (IB–IIIA) non-small cell lung cancer in the phase 3 CheckMate 816 trial. AACR 2021.
8.Heather Wakelee, Moishe Liberman, Terufumi Kato, et al. Perioperative Pembrolizumab for Early-Stage Non–Small-Cell Lung Cancer. N Engl J Med. 2023. doi:10.1056/NEJMoa2302983.
9.Spicer JD, et al. Overall survival in the KEYNOTE-671 study of perioperative pembrolizumab for early-stage non-small-cell lung cancer(NSCLC).2023 ESMO, LBA56.
10.SHUN. L. Perioperative Toripalimab + Platinum-Doublet Chemotherapy vs Chemotherapy in Resectable Stage ll/lll Non-small Cell Lung Cancer:Interim Event-Free Survival Analysis of the Phase Ill Neotorch Study [M]. ASCO Monthly Plenary Series (April). 2023.
11.D. Yuel,et al. Pathological Response to Neoadjuvant Tislelizumab(TIS) Plus Chemotherapy(CT) in Resectable Stage II-IIIANSCLC Patients(pts) in the Phase3(Ph3) RATIONALE-315 Trial. 2023 ESMO. LBA58.
12.Cascone T, et al. CheckMate 77T: Phase III study comparing neoadjuvant nivolumab (NIVO) plus chemotherapy (chemo) vs neoadjuvant placebo plus chemo followed by surgery and adjuvant NIVO or placebo for previously untreated, resectable stage II–IIIb NSCLC. 2023 ESMO, LBA1.
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言














#非小细胞肺癌# #免疫治疗#
114