阿斯利康和第一三共制药的Enhertu在美国获批用于早期治疗乳腺癌
2022-05-09 Allan MedSci原创
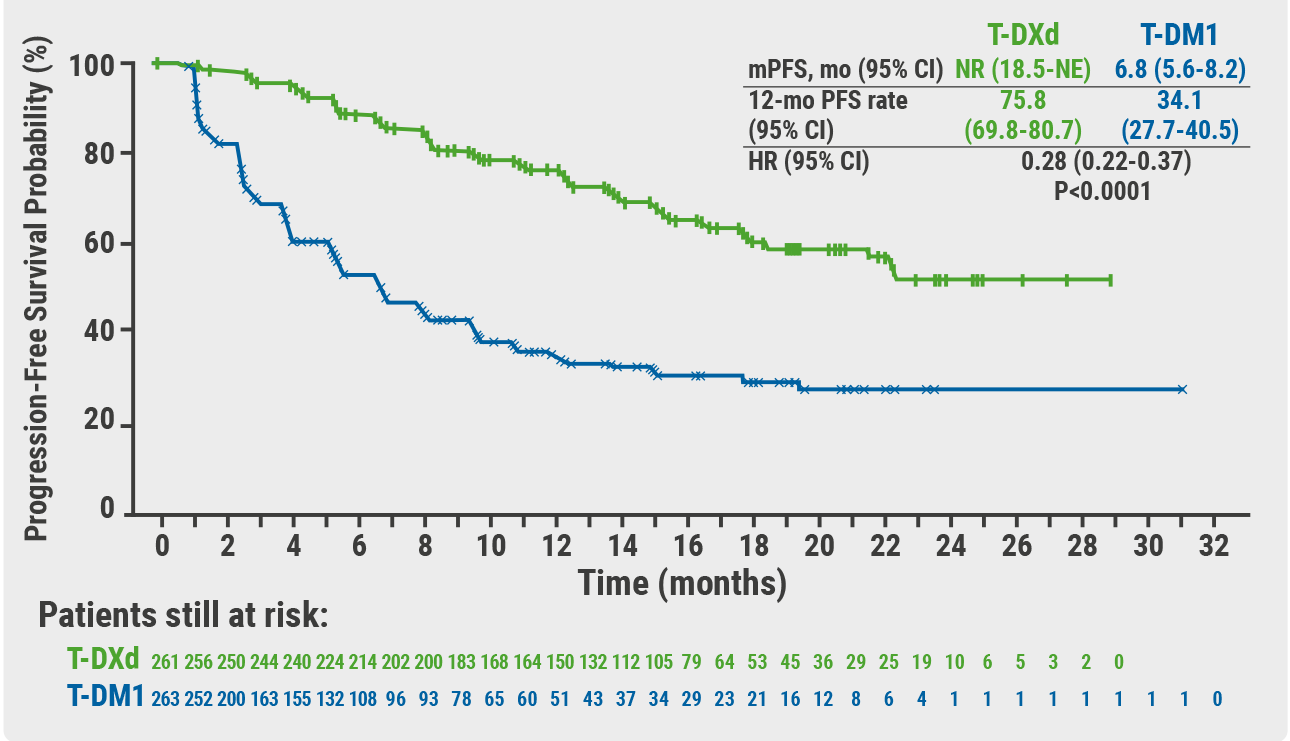
与罗氏的 Kadcyla(曲妥珠单抗 emtansine)相比,Enhertu 在 HER2 阳性不可切除和/或转移性患者中将疾病进展或死亡风险降低了 72% 。
HER2 阳性乳腺癌是一种被称为人表皮生长因子受体 2(HER2)的蛋白质检测呈阳性的乳腺癌。这种蛋白质对癌细胞的生长有促进作用。HER2 阳性乳腺癌通常比其他类型的乳腺癌更具侵袭性。
阿斯利康(AstraZeneca)和第一三共(Daiichi Sankyo)近日宣布,FDA 已批准 Enhertu(曲妥珠单抗-deruxtecan)用于治疗患有不可切除或转移性 HER2 阳性乳腺癌患者。两家公司指出,该决定将抗体-药物偶联物 Enhertu 的适应症扩大到早期治疗线。
具体而言,Enhertu 已被批准用于治疗患有不可切除或转移性 HER2 阳性乳腺癌成人患者,这些患者在转移性环境中或在新辅助或辅助环境中接受过基于抗 HER2 的方案,并且在治疗期间或在完成治疗后六个月内出现疾病复发。阿斯利康肿瘤业务部门执行副总裁 Dave Fredrickson 说:“williamhill asia 很高兴通过这项批准,美国的患者现在可以在治疗早期使用 Enhertu”。
最初的加速批准得到了单臂 II 期 DESTINY-Breast01 试验数据的支持,其中 Enhertu 组患者的总体缓解率为 60.3%,包括 4.3% 的完全缓解率和 56% 的部分缓解率。III 期 DESTINY-Breast03 研究的结果显示,与罗氏的 Kadcyla(曲妥珠单抗 emtansine)相比,Enhertu 在 HER2 阳性不可切除和/或转移性患者中将疾病进展或死亡风险降低了 72% 。
两家公司指出,新的批准是根据 FDA 的实时肿瘤学审查(RTOR)计划授予的,而该申请也通过 Orbis 项目进行评估,澳大利亚、巴西、加拿大、以色列和瑞士的监管机构通过 Orbis 项目进行合作审查。
原始出处:
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言

















#Enhertu#
70
#早期治疗#
76
#美国获批#
67
乳腺癌治疗新方法
74
#阿斯利康#和#第一三共#制药#乳腺癌#,三个关键词
163