Cell子刊:中山大学王军舰/刘培庆/袁燕秋开发治疗骨肉瘤的潜在新策略
2024-05-04 iNature iNature 发表于上海
该研究表明核受体RORγ可能作为OS的潜在治疗靶点,OS表现出过度活化的氧化磷酸化(OXPHOS)程序,该程序为促进肿瘤进展的碳源提供燃料。
骨肉瘤是最常见的恶性骨肿瘤,预后较差。
2024年4月30日,中山大学王军舰、刘培庆及袁燕秋共同通讯在Cell Reports Medicine在线发表题为“Tumor mitochondrial oxidative phosphorylation stimulated by the nuclear receptor RORγ represents an effective therapeutic opportunity in osteosarcoma”的研究论文,该研究表明核受体RORγ可能作为OS的潜在治疗靶点,OS表现出过度活化的氧化磷酸化(OXPHOS)程序,该程序为促进肿瘤进展的碳源提供燃料。
该研究发现,RORγ在OS肿瘤中过表达,并与过度激活的OXPHOS有关。RORγ诱导PGC-1β的表达,并与PGC-1β物理相互作用,通过上调呼吸链组分基因的表达激活OXPHOS程序。抑制RORγ强烈抑制OXPHOS的激活,下调线粒体功能,增加ROS的产生,导致OS细胞凋亡和铁死亡。RORγ逆激动剂强烈抑制OS肿瘤的生长和进展,并使OS肿瘤对化疗敏感。综上所述,该研究结果表明,RORγ是OS中OXPHOS程序的关键调节因子,并为这种致命疾病提供了有效的治疗策略。

骨肉瘤(Osteosarcoma, OS)是儿童和青少年最常见的原发性骨恶性肿瘤目前的标准治疗,包括手术和化疗,已将局部OS患者的5年生存率提高到约60%。然而,由于缺乏有效的转移性和耐药性OS治疗,复发和/或转移性OS患者的死亡率仍然很高,在过去的40年里,5年生存率保持在约20%。因此,迫切需要确定潜在的治疗靶点并制定更有效的晚期骨肉瘤治疗策略。
据报道,人类乳腺癌在成骨分化过程中会经历代谢重编程,导致OXPHOS增强,从而加速上皮-间质转化的进程经典霍奇金淋巴瘤(cHL)表现出全局激活的OXPHOS信号。依赖OXPHOS的ATP合成对cHL细胞的生存和生长至关重要。癌细胞表现出代谢异质性,可分为高OXPHOS亚群和低OXPHOS亚群。有趣的是,来自PDAC的干细胞强烈依赖于高OXPHOS,这赋予了对化疗的高耐药性使用线粒体ETC抑制剂治疗可有效抑制高OXPHOS肿瘤的生长和转移,并使其对化疗增敏。因此,靶向OXPHOS可能是治疗OXPHOS上调的癌症亚型的有效策略。
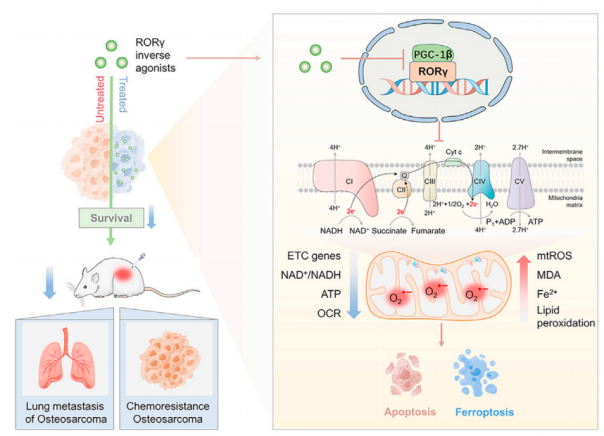
机理模式图(图源自Cell Reports Medicine )
核受体(NRs)是一个大的转录因子家族,参与调节关键的生理功能,如细胞分化、胚胎发育和器官生理类视黄酮相关孤儿受体γ (RORγ,由RORC编码)是NR超家族成员,与RAR相关孤儿受体a (RORα)和RAR相关孤儿受体B (RORβ) 23一起参与多种生理过程,包括细胞增殖、凋亡、代谢和免疫调节。RORγ有两个同工异构体RORγt和RORγ。RORγt是一种T细胞特异性亚型,受胸腺中T细胞特异性启动子的调控。由于RORγt在炎症相关T辅助型17 (Th17)细胞发育和自身免疫性疾病中的重要作用,已经确定靶向RORγt是一种很有前景的自身免疫性疾病治疗策略。
然而,RORγ在其他人类疾病中的功能在很大程度上仍然未知。RORγ抑制强烈抑制肿瘤生长,并在前列腺癌、乳腺癌和胰腺癌的治疗耐药中起关键作用。但是,RORγ在OS中的作用在很大程度上仍然未知,需要进一步研究。该研究揭示了NR RORγ是OS中OXPHOS程序的关键驱动程序。在多种体外和体内模型中,RORγ逆激动剂强烈抑制OXPHOS激活,失调线粒体功能,诱导细胞凋亡和铁死亡,并阻断OS肿瘤的生长和进展。这些发现表明,RORγ是晚期OS的有效治疗靶点。
原文链接:
https://doi.org/10.1016/j.xcrm.2024.101519
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言

















#骨肉瘤#
23