FDA批准lumasiran治疗原发性高草酸尿症1型,Alnylam的RNAi帝国再下一城!
2022-10-11 会会药咖 会会药咖
近日,FDA批准了Alnylam的RNAi药物lumasiran的新适应症,通过降低血浆中的草酸盐水平来治疗原发性高草酸尿症1型(又称Ph1)这种罕见的遗传性疾病。主要基于一系列临床试验结果,见:NE
近日,FDA批准了Alnylam的RNAi药物lumasiran的新适应症,通过降低血浆中的草酸盐水平来治疗原发性高草酸尿症1型(又称Ph1)这种罕见的遗传性疾病。主要基于一系列临床试验结果,见:NEJM:Lumasiran,一种治疗原发性1型高草尿症的干扰RNA、Genet Med:lumasiran治疗原发性1型高草酸尿症的3期试验:一种新的婴幼儿RNAi疗法
本次适应症获批彻底宣告了Alnylam在罕见病PH1领域的全面胜利。竞争对手Dicerna虽然在Ph1阶段先行获得成果,但在2021股价大跌后已被诺和诺德以33亿美元收购,Alnylam再次成为赢家。
随着首个RNAi药物获批,资本与希望同时归来,技术借此实现了快速迭代。第一代药物Patisiran使用的是通过静脉给药的LNP递药技术,而现在Alnylam已能够皮下给药,通过RNAi与N-乙酰半乳糖胺 (GalNAc)或者类似的配体进行连接,使药物具有更好的治疗指数,提升剂量并减少副作用。
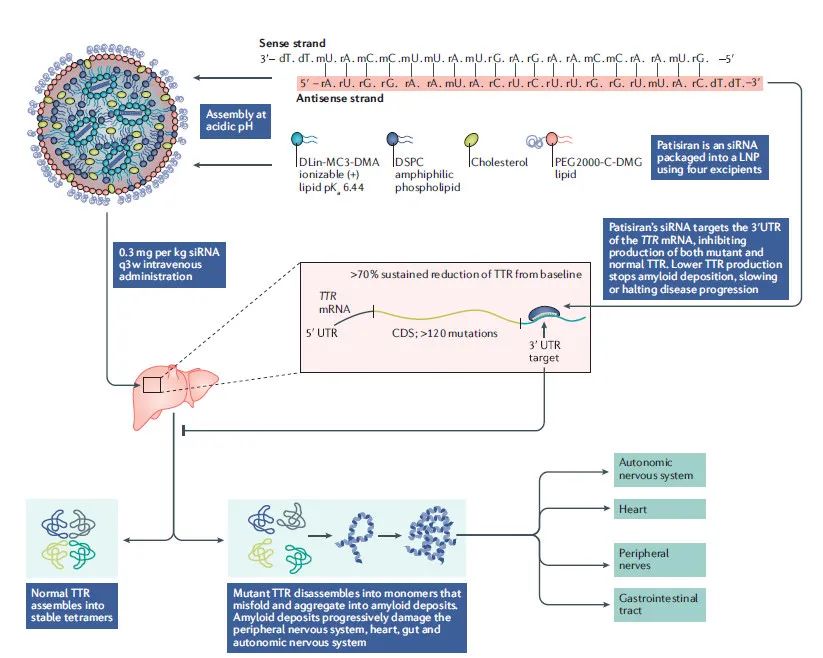
Alnylam自1990年进入核酸药物领域以来,目前有5款RNAi药物获批上市,包揽了获批上市的全部名额。其他公司包括安进、阿斯利康等,也通过收购等方式,加入了这个赛道竞争。
Onpattro(patisiran)
Alnylam首款RNAi药物,适用于遗传性转甲状腺素蛋白淀粉样变性(hATTR)引起的周围多发性神经疾病(polyneuropathy)成人患者。2018年获批,2021年营收4.75亿美元。详细:NEJM发布遗传性肝病RNAi疗法2期临床试验结果,降低致病蛋白83%
Givlaari(givosiran)
Alnylam上市的第二款RNAi药物,用于治疗急性肝卟啉症的成年患者,揭开ESC-GalNAc靶向修饰技术时代。详细:NEJM:Givosiran治疗急性间歇性卟啉症
Oxlumo(lumasiran)
Alnylam上市的第三款RNAi药物,适用于所有年龄段的1型原发性高草酸尿症(PH1)。详细:NEJM:Lumasiran,一种治疗原发性1型高草尿症的干扰RNA
Leqvio(inclisiran)
Alnylam和诺华合作开发,用于治疗成人原发性高胆固醇血症(杂合子家族性和非家族性)或混合型血脂异常,是全球首款降胆固醇(LDL-C)的siRNA疗法,给药方式为皮下注射。详细:NEJM:Inclisiran治疗家族性高胆固醇血症、无论年龄和性别,诺华靶向PCSK9的siRNA疗法均可在17个月内持续有效降低LDL-C
Amvuttra(vutrisiran)
今年6月FDA获批上市,每3个月皮下注射一次,治疗遗传性转甲状腺素蛋白介导(hATTR)淀粉样变性成人患者的1、2期多发性神经病。详细:FDA批准vutrisiran治疗成人遗传性转甲状腺素蛋白淀粉样变性伴多发性神经病(hATTR-PN),这是第5款siRNA药物
首个也是唯一FDA批准的能逆转神经损伤的、长效的RNAi治疗药物,可以看做Onpattro升级版,平均定价为463500美元/年,是2022年FDA获批最贵的药物。
Alnylam带着诺奖级RNAi技术的光环仿佛重新站在了风口之上,并正在迎来新传奇。然而即使是国外巨头在做RNAi创新药时也多次折戟,赫吉亚与复星医药旗下企业合作的首个国产乙肝GalNAc-siRNA药物于今年九月方才获批临床。
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言










#RNAi药物##Alnylam# #lumasiran#治疗#原发性高草酸尿症1型#
100