FDA拒绝批准vadadustat治疗CKD相关贫血
2022-04-03 Allan MedSci原创
研究表明,在非透析依赖患者的主要疗效和安全性终点方面,虽然 vadadustat 在主要疗效目标上取得了成功,但它未能证明在 MACE 方面的非劣效性。
在慢性肾脏病(chronic kidney disease,CKD)病程进展中,大约 50% 的 CKD 3期~CKD 5 期患者并发贫血,且血液透析患者合并贫血的比例更高。促红细胞生成素缺乏并非贫血发生的唯一原因,缺铁、氧化应激、胰岛素抵抗、药物等也会加重贫血的进展和降低机体造血系统对EPO的反应。
除了引起致残性症状以外,重度贫血可能影响非透析CKD患者和透析患者的心血管功能。对于非透析CKD患者,重度贫血可能引起CKD进展加快,包括进展为终末期肾病(end-stage kidney disease, ESKD)。
制药公司 Akebia Therapeutics 近日表示,FDA 就其申请口服 HIF-PH 抑制剂 vadadustat 治疗慢性肾脏病(CKD)引起的贫血发出了完整的回复信(CRL)。根据 Akebia 的说法,FDA 得出的结论是:申请中包含的数据不支持 vadadustat 对透析和非透析 CKD 患者的临床益处。
该公司的提交的文件包括 III 期 INNO2VATE 试验。研究表明,在透析依赖患者的主要疗效和安全性终点方面,vadadustat 均不劣于 Amgen 的 Aranesp(darbepoetin alfa),而安全性终点着眼于首次发生主要不良心血管事件 (MACE) 的时间。
提交的文件还包含 PRO2TECT 试验的结果,这是一项 vadadustat 与 Aranesp 的头对头研究。研究表明,在非透析依赖患者的主要疗效和安全性终点方面,虽然 vadadustat 在主要疗效目标上取得了成功,但它未能证明在 MACE 方面的非劣效性。
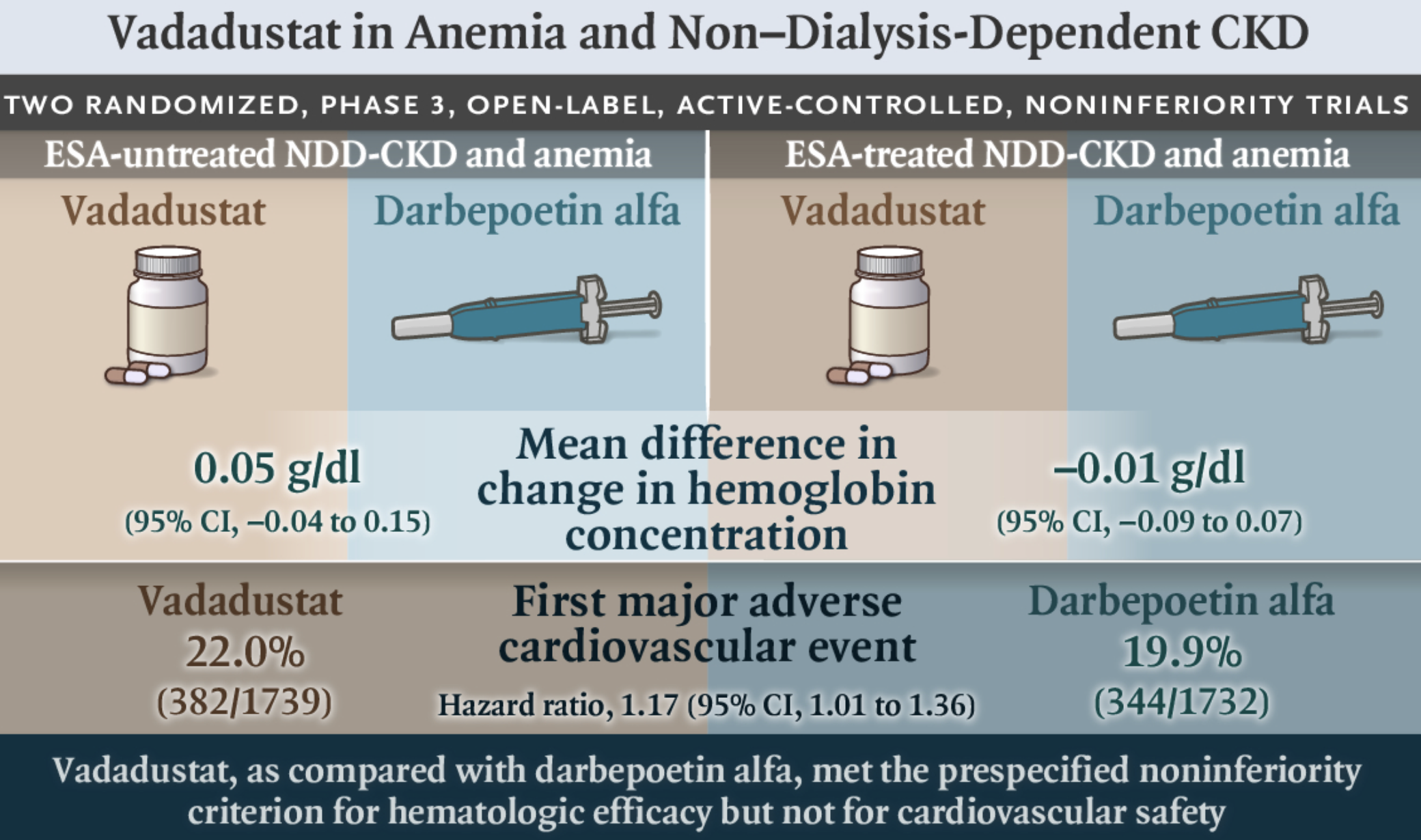
图1.PRO2TECT 试验设计(图片来源https://www.nejm.org/doi/full/10.1056/NEJMoa2035938)
根据 Akebia 的说法,FDA 的 CRL 强调了非透析人群的安全性挫折、透析患者血栓栓塞事件风险增加以及药物性肝损伤的风险。
无独有偶,阿斯利康的口服 HIF-PH 抑制剂 roxadustat 去年 8 月也遭遇了类似的命运,当时 FDA 在机构审查人员表示与该药物相关的“严重血栓栓塞事件的重要风险”后拒绝批准 roxadustat。然而,roxadustat 后来以 Evrenzo 的名义在欧洲获得批准,并且在日本也获得了批准。
原始出处:
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言







#CKD相关贫血#
55
#vadadustat#
50
vadadustat是继#罗沙司他#之后,第二被FDA拒绝,主要原因还是安全性问题。与EPO相比,确实方便,效果也相当好,提升红细胞也快,但是血栓,促进肿瘤等潜在风险,仍然难以消除,除非有长期观察(3年以上的结果)
110
#贫血#
110
#ADA#
62