ASCO 2020丨儿童肿瘤精准治疗获得新助力!优先级算法可行性佳
2020-06-03 陶然 健康界
2020年美国临床肿瘤学会(ASCO)年会已经拉开帷幕,这场学术盛宴可谓精彩纷呈,赢得了全世界肿瘤医生的瞩目。
2020年美国临床肿瘤学会(ASCO)年会已经拉开帷幕,这场学术盛宴可谓精彩纷呈,赢得了全世界肿瘤医生的瞩目。其中最受关注的重磅研究摘要(Late-breaking Abstract,LBA)于美国东部时间5月28日下午5点正式公布,共有2篇入选Oral Abstract Session,5篇LBA入选Plenary Session。快跟随小编的步伐,开启云年会模式,纵览这些重磅研究吧。
本期和大家分享的是入选Oral Abstract Session的一篇LBA——“儿童精准肿瘤学研究告知:临床结果和分子亚群的获益”(The pediatric precision oncology study INFORM: Clinical outcome and benefit for molecular subgroups),摘要号为LBA10503。
 图1 ASCO 2020入选的LBA研究(摘要号:LBA10503,图源:ASCO 2020官网)
图1 ASCO 2020入选的LBA研究(摘要号:LBA10503,图源:ASCO 2020官网)
研究背景
精准医学正在不断渗透临床实际工作中,靶向治疗具有巨大潜力并发挥着显著优势。难治、复发、进行性高危儿童肿瘤患者往往预后不良,一些儿童精准肿瘤学项目已经鉴定出某些可指导临床的分子变异,但其具体临床获益却是未知的,Cornelis Martinus van Tilburg等人为评估儿科精准肿瘤学在现实临床中的可行性,开展了这项INFORM研究。这篇摘要报道了儿童精准肿瘤学的现状,提出优先级算法可以识别靶向治疗获益人群。

图2 研究背景(图源:ASCO 2020官网)
研究方法
INFORM研究是一项收集临床数据和分子数据的前瞻性的、非干预性的、多中心的、跨国的可行性注册研究,纳入了难治/复发/进展性恶性疾病患者,包括初步诊断出的高风险对象。取其新鲜冷冻肿瘤标本(包括种系DNA)进行全外显子测序(whole-exome sequencing,WES)、低覆盖率的全基因组测序(low-coverage whole-genome sequencing,lcWGS)、RNA测序、RNA表达阵列和DNA甲基化分析。每周一次跨学科分子委员会根据从“非常高”到“非常低”的7步量表,根据变异的类型及其与个体的特定相关性,对变异进行审查和优先排序(在Worst等人2016年发表在Eur J Cancer的杂志中有描述)。
图3 研究方法(图源:ASCO 2020官网)
研究结果
到目前为止,共有1300多例患者入选。来自8个国家72个中心的525例患者完成随访并纳入本分析。受试者中位年龄为12.0岁(0~40岁),从提交到报告的平均周转时间为25.4天。中位PFS和中位OS分别为116天(95% CI 105~135)和289天(95% CI 250~335)天。每位患者的最高优先靶点分布情况为:非常高8.0%,高14.8%,中等20.3%,中间23.6%,临界14.4%,低2.5%,非常低1.0%,无可指导临床行为的靶点15.4%。
 图4 诊断和靶向优先级分布情况(图源:ASCO 2020官网)
图4 诊断和靶向优先级分布情况(图源:ASCO 2020官网)
149例患者根据已确定的靶点接受了靶向治疗,其中20例患者的中位PFS为204.5(95% CI 91.0~628.0),而其他505例患者的中位PFS为114天(95% CI 103~133)(P=0.0095)。OS没有显示临床相关的差异。探索性分析入组前后的疾病进展时间(TTP)比率显示,与所有其他患者(0.7)相比,按照非常优先的靶向治疗的患者具有更高的TTP比率(1.0)。
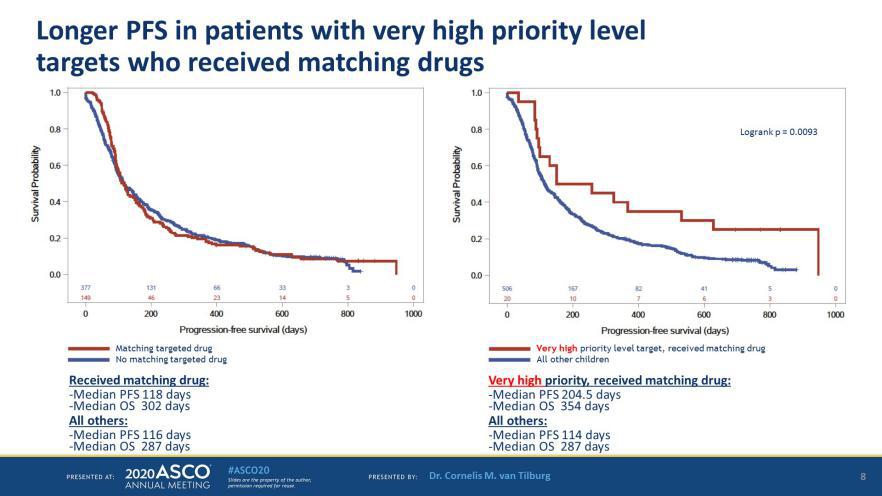
图5 根据非常高优先级靶点用药的患者PFS延长(图源:ASCO 2020官网)
另外,该研究中7.8%的患者发现了可能的易感综合征,其中一半是新诊断患者,甲基化分析为8%的中枢神经系统肿瘤提供了精准的诊断。
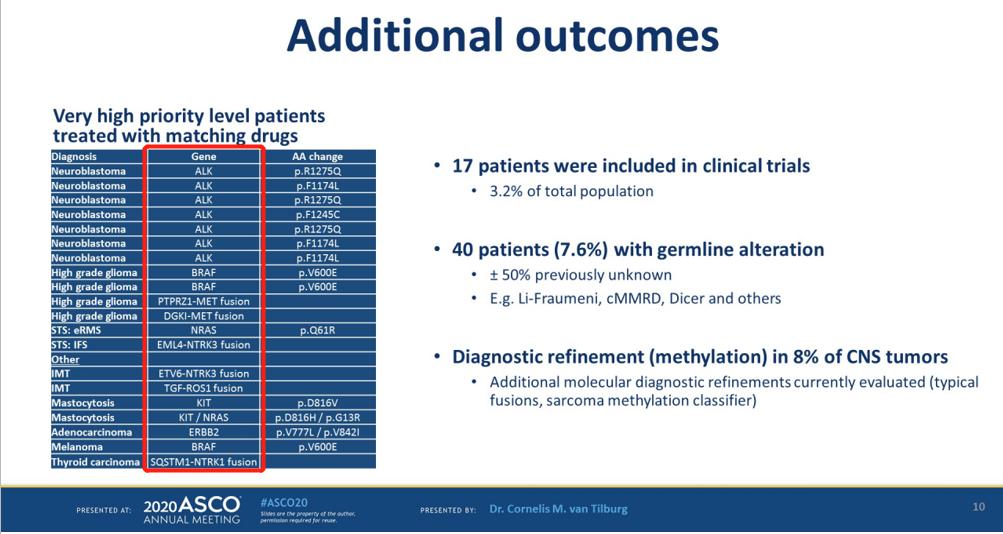
图6 其他结果(图源:ASCO 2020官网)
拓展思考
本试验证明儿童精准肿瘤学在现实世界中,多国背景下实施是可行的。优先化算级可识别从分子匹配靶向治疗中受益的亚组。不过,对于没有高优先级靶点的患者,进一步的分子和功能数据层应纳入未来的计划中。
2019年发表在JAMA上的一项研究(Molecular Profiling of Hard-to-Treat Childhood and Adolescent Cancers)曾验证了基因组测序能否促进患者肿瘤的分子谱分析以识别可操作和可靶向的改变。这是一项在加拿大魁北克进行的前瞻性基因组测序研究(TRICEPS),纳入了2014年4月至2018年1月,18岁或18岁以下诊断为难治性或复发性儿童和青少年癌症的62例受试者。
 图7 JAMA发表研究证实基因组测序的可行性(图源:JAMA官网)
图7 JAMA发表研究证实基因组测序的可行性(图源:JAMA官网)
该研究对匹配的正常肿瘤标本进行了WES和RNA序列测定,以确定单核苷酸变异、融合转录、差异基因表达和拷贝数改变。通过综合的分子分析,发现将包括RNA测序在内的多模态基因组测序纳入难治性或复发性儿童和青少年癌症管理中,在54例(87%)患者中识别出了潜在的可操作改变。确定了治疗这些患者所需的可操作和可靶向改变后,最终提出了有针对性和个性化的新治疗策略。
发表在JAMA的这篇研究同样证实将基因组测序纳入难以治疗的儿童和青少年癌症的治疗中似乎是可行的,分子图谱可以识别出对大多数患者临床获益的潜在可操作性改变,包括靶向治疗和诊断、预后和临床相关信息监测意义。
儿童癌症具有其特殊性,发病率低且入组临床试验患者有限,但儿童肿瘤存在的基因突变相对较少,因此综上可知对于儿童肿瘤来说,在精准医学的时代大潮下,基因治疗助力靶向治疗大势所趋。
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言











#可行性#
72
#ASC#
66
#精准治疗#
73
#ASCO 2020#
0
#儿童肿瘤#
76
#精准#
73