Nat Med:江泽飞团队报道特瑞普利单抗联合nab-紫杉醇 (nab-P) 对转移性或复发性三阴性乳腺癌展示良好疗效(TORCHLIGHT研究)
2024-01-09 iNature iNature 发表于加利福尼亚
乳腺癌是女性中最常见的癌症类型,2020年全球报告了230万新病例和68.5万例死亡。免疫检查点阻断联合化疗一线治疗晚期三阴性乳腺癌(TNBC)产生了不同的结果。
乳腺癌是女性中最常见的癌症类型,2020年全球报告了230万新病例和68.5万例死亡。免疫检查点阻断联合化疗一线治疗晚期三阴性乳腺癌(TNBC)产生了不同的结果。
2024年1月8日,中国人民解放军总医院江泽飞团队在Nature Medicine(IF=83)在线发表题为“Toripalimab plus nab-paclitaxel in metastatic or recurrent triple-negative breast cancer: a randomized phase 3 trial”的研究论文,该研究报道了一项特瑞普利单抗联合nab-紫杉醇治疗转移性或复发性三阴性乳腺癌的随机3期试验。
TORCHLIGHT是一项随机、双盲的3期临床试验,评估一线托帕利单抗和nab-紫杉醇(nab-P)的疗效和安全性(n = 353;实验组)与安慰剂和nab-p相比(n = 178;对照组)用于治疗转移性或复发性TNBC的女性。主要终点是PD-L1阳性和有意治疗人群的无进展生存期(PFS)。次要终点包括总生存期和安全性。总体而言,托利哌单抗组和安慰剂组分别有200名和100名患者患有PD-L1阳性TNBC。
其中这项结果发表在ASCO上,见:J Clin Oncol:一项随机、双盲、III 期试验-特瑞普利单抗或者安慰剂联合 nab-紫杉醇 (nab-P) 用于转移性或复发性三阴性乳腺癌 (TNBC) 患者,此次是更详细的结果发表。
在预先指定的期中分析中,通过盲法独立中心评价,实验组PD-L1阳性人群的PFS有统计学显著改善(中位PFS 8.4个月对5.6个月;风险比(HR) = 0.65, 95%可信区间(CI) 0.470 ~ 0.906, P = 0.0102)。中位总生存期分别为32.8个月和19.5个月(HR = 0.62, 95% CI 0.414-0.914, P = 0.0148)。在实验组和对照组中,治疗后出现的不良事件(AEs)(99.2%对98.9%)、≥3级治疗后出现的AEs(56.4%对54.3%)和致死性AEs(0.6%对3.4%)的发生率相似。在nab-P的基础上添加特瑞普利单抗可显著改善PD-L1阳性转移性或复发性TNBC患者的PFS,并具有可接受的安全性。
TNBC的特点是肿瘤细胞上缺乏ER、PR和HER2的表达,由于缺乏可操作的靶点,除了常规化疗外,TNBC的治疗选择有限。虽然TNBC仅占所有乳腺癌的15-20%,但它在乳腺癌亚型中预后最差。在免疫疗法出现之前,包括紫杉烷类、蒽环类药物和/或铂类药物在内的全身化疗是TNBC的主要一线治疗选择。然而,转移性TNBC3的中位总生存期(mOS)仅为9-12个月,5年生存率约为12%,这代表了一个关键的未满足的医疗需求。
免疫检查点PD-1途径抑制剂已经彻底改变了各种恶性肿瘤的治疗管理,包括TNBC。与其他乳腺癌亚型相比,TNBC具有相对较高的肿瘤突变负担(tumor mutational burden, TMB),这一特征与免疫治疗反应的改善有关。已知化疗(包括铂和紫杉烷)可诱导肿瘤细胞的免疫原性细胞死亡,并可与检查点阻断协同作用以改善免疫激活。几项大型随机3期试验已经评估了将PD-1/PD-L1阻断剂添加到化疗中用于TNBC的一线治疗,但结果不一。
在TORCHLIGHT研究中,研究人员比较了特瑞普利单抗与安慰剂联合nab-p一线或二线治疗转移性或复发性TNBC的疗效和安全性。在预先指定的中期PFS分析中,在PD-L1阳性人群(JS311 CPS≥1)中,与单用nab-紫杉醇相比,在nap -p中加入托帕利单抗显示出具有统计学意义和临床意义的PFS改善。在实验中,mPFS改善了2.8个月,疾病进展或死亡的风险降低了35%。描述性OS分析显示,PD-L1阳性患者的OS均有改善的趋势(mo为32.8 vs 19.5个月;HR = 0.62, 95% CI 0.414-0.914)和ITT人群(平均寿命33.1个月vs . 23.5个月;Hr = 0.69, 95% CI 0.513-0.932)。TORCHLIGHT研究的结果进一步验证了在化疗中加入PD-1检查点阻断治疗晚期TNBC的临床价值。
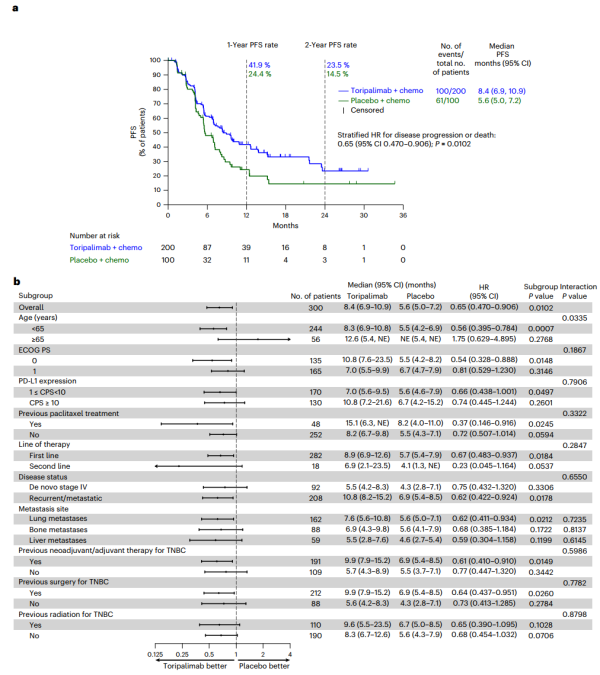
PD-L1+ TNBC人群的无进展生存期(图源自Nature Medicine )
该研究也存在着一定的局限性。该研究仅从中国招募患者;然而,推测其发现可以外推到西方患者,因为在IMpassion130和KEYNOTE-355研究的亚组分析中没有发现结果的种族差异,在其他跨不同适应症的多区域免疫化疗3期试验中也没有发现这种差异。总之,在nab-紫杉醇的基础上添加托帕利单抗可显著改善CPS≥1 PD-L1阳性转移性或复发性TNBC患者的PFS,同时保持可接受的安全性。ITT人群PFS的最终分析以及PD-L1阳性亚组和ITT人群OS的最终分析将在未来进行统计学检验。
原文链接:
Jiang, Z., Ouyang, Q., Sun, T. et al. Toripalimab plus nab-paclitaxel in metastatic or recurrent triple-negative breast cancer: a randomized phase 3 trial. Nat Med (2024). https://doi.org/10.1038/s41591-023-02677-x
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言












#三阴性乳腺癌# #江泽飞# #复发或转移性三阴性乳腺癌# #特瑞普利单抗# #Nab-紫杉醇#
0